
����Ŀ���±���Ԫ�����ڱ���һ���֣����ݱ��и�����10��Ԫ�أ���Ҫ������
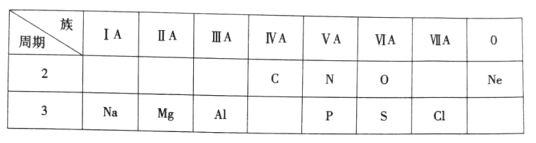
(1)þԪ��λ��Ԫ�����ڱ��е�___����_____�壻
(2)��������������������������_____��
(3)O��S��ȣ�ԭ�Ӱ뾶��С����____��
(4)���ʯ�����Ԫ����________��
(5)���ʵĻ�ѧ��������õ�Ԫ����______��
(6)Na��MgԪ����Ƚ����Խ�ǿ����_________
(7)NH3��PH3��ȣ����ȶ��Խ�������______
(8)H2SO4��H3PO4������Խ�ǿ����______
(9)Mg(OH)2��Al(OH)3�����������������������________
(10)���ʳʻ���ɫ���������Ԫ����_____���䵥�ʵ�ˮ��Һ��__(�������Ի���������)��
���𰸡�3 ��A N2 O C Ne Na PH3 H2SO4 Al(OH)3 Cl ����
��������
(1)þԪ�ص�ԭ������Ϊ12����������ӣ�����������Ϊ2��λ��Ԫ�����ڱ��е�3������A�壻
(2)����������������ռ78%���ǵ���������Ϊ21%��ϡ������0.94%����������0.03%��������̼0.03%���������������������N2��
(3)O��Sλ��ͬһ���壬ͬ����Ԫ�ش��ϵ��°뾶������O��S��ԭ�Ӱ뾶��С����O��
(4)���ʯ��̼Ԫ���γɵĵ��ʣ����Ԫ����C��
(5)ϡ���������������ã����ʵĻ�ѧ��������õ�Ԫ����Ne��
(6)Na��Mgλ��ͬһ���ڣ�ͬ����Ԫ�ش����ҽ���������ǿ��Na��MgԪ����Ƚ����Խ�ǿ����Na��
(7)N��Pλ��ͬһ���壬ͬ����Ԫ�ش��ϵ��·ǽ�������������̬�⻯����ȶ��Լ�����NH3��PH3��ȣ����ȶ��Խ�������PH3 ��
(8) P��Sλ��ͬһ���ڣ�ͬ����Ԫ�طǽ���������ǿ��H2SO4��H3PO4������Խ�ǿ����H2SO4��
(9)Mg(OH)2��Al(OH)3�������������������������Al(OH)3�������Ժ�ǿ�ᷴӦ��Ҳ���Ժ�ǿ�Ӧ��
(10)���ʳʻ���ɫ�����������������Ԫ����Cl��������ˮ��Һ����ˮ����������ʹ���������ʣ��䵥�ʵ�ˮ��Һ�����ԡ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ش��������⣺
(1)ij���۽���������9���۵��ӣ��۵��ӵ��ܼ�Ϊ3d����Ԫ��λ�����ڱ��еĵ������ڡ���______�塣
(2)�������(KOCN)�����Ԫ���У���һ������������______(��Ԫ�ط��š���ͬ)���縺����С����______�����������ӵĿռ�ṹ��______��C���ӻ���ʽΪ______��
(3)�Ҷ�������Mg2�������γ��ȶ���״���ӣ�[Mg(C2H8N2)2]2+����ṹ��ͼ��ʾ��
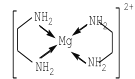
��û�״������þ���ӵ���λ��Ϊ______��
(4)��֪�����ӵ�����ΪNA��������п(M=97g/mol)������ͼ��ʾ��
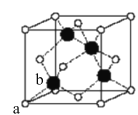
�侧���ⳤΪ��pm�������ܶ�Ϊ______g/cm3(�ú����Ĵ���ʽ��ʾ)�����ж���λ��a��S2-������������λ��b��Zn2+����֮��ľ���Ϊ______pm(�ú����Ĵ���ʽ��ʾ)��aλ�õ�S2-���Ӻ�bλ�õ�Zn2+���ӵķ�����������Ϊ��______��______��(��֪��1m=102cm=1012pm)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaBH4/H2O2ȼ�ϵ��(DBFC)��װ��ʾ��ͼ���£�����������ȷ����
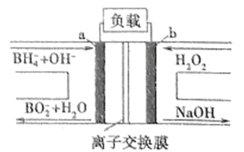
A.b��Ϊ����������������Ӧ
B.���Ӧѡ�������ӽ���Ĥ
C.�����ƶ����缫a�����ӽ���Ĥ���缫b
D.a���ĵ缫��ӦʽΪ![]() +8OH--8e-=
+8OH--8e-=![]() +6H2O
+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯���������������������Ź㷺��Ӧ�á�
(1)ij�о���ѧϰС�����������ͼ��ʾװ��̽�������ĸ�ʴ��������ձ���Һ���Ϊ����ʳ��ˮ��
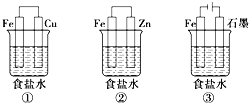
������ͬ�����£�����װ�������缫��ʴ������__(��װ�����)����װ����������ӦʽΪ__��
��Ϊ��ֹ����Fe����ʴ�����Բ�������___(��װ�����)װ��ԭ�����з�����
(2)ͨ����������﮵�������С�������ᡢ��������ͻ�����ɸ߱��ʳ�ŵ硢��ɫ�������ڶ��ŵ㡣������﮵�������������Ϊ�������ϵ�һ������Ӷ��ε�أ��ŵ�ʱ��������ӦʽΪM1-xFexPO4+e-+Li+=LiM1-xFexPO4����ԭ����ͼ��ʾ��
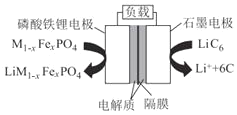
���ŵ�ʱ��������___�缫����������___�缫��������ӦʽΪ____��
���õ�ع���ʱLi+����___�缫�����ʱʯī�缫�ӵ�Դ��____����
���õ�ص��ܷ�Ӧ����ʽΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ģ�����������Ƽ����ȡNa2CO3������ʵ�鲽����ʵ�ֵ��ǣ� ��
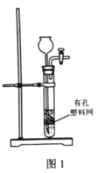

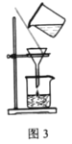
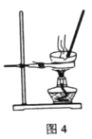
A.��ͼ1װ����ʯ��ʯ��ϡ�����Ʊ�CO2
B.��ͼ2װ�ó�ȥCO2�е�HCl
C.��ͼ3װ�ù������õ�NaHCO3����
D.��ͼ4װ�ü�������NaHCO3������Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3�������Ϊ2.0L�ĺ����ܱ������У���ӦCO2(g)+C(s)![]() 2CO(g) H��0�ֱ���һ���¶��´ﵽ��ѧƽ��״̬������˵����ȷ���ǣ� ��
2CO(g) H��0�ֱ���һ���¶��´ﵽ��ѧƽ��״̬������˵����ȷ���ǣ� ��
���� | �¶�/K | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | ||
n(CO2) | n(C) | n(CO) | n(CO) | ||
�� | 977 | 0.28 | 0.56 | 0 | 0.4 |
�� | 977 | 0.56 | 0.56 | 0 | x |
�� | 1250 | 0 | 0 | 0.56 | y |
A.�ﵽƽ��ʱ����������������C(s)������ƽ�������ƶ�
B.x=0.8��y��0.4
C.�ﵽƽ��ʱ���������е�CO��ת����С��![]()
D.����ʼʱ���������г���0.1molCO2��0.2molCO��������C(s)����Ӧ��������Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��л����˵����ȷ����
A. C8H10����������ͬ���칹����3��
B. ��ϩ�ᣨCH2=CHCOOH����ɽ���ᣨCH3CH=CHCH=CHCOOH����ͬϵ��
C. ��֬��һ��������ˮ��ɸ�֬������ͣ���Ϊ������Ӧ
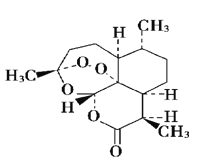
D. �������ǿ�ű����Чҩ���ṹ��ͼ��ʾ�������������������Ѽ���������ˮ���������ȷ¡���ͪ��,���������Ѵ�ֲ������ȡ, �ܹ�����ˮ�ⷴӦ,����ǿ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱ�����ֳ��������Ka���±���ʾ��
����� | H2C2O4 | CH3COOH | HCN | H2CO3 |
���볣����molL-1�� | K1=5.6��10-2 K2=5.4��10-3 | K=1.7��10-5 | K=6.2��10-10 | K1=4.2��10-7 K2=5.6��10-11 |
��1�����ᣨH2C2O4����һ��___������һԪ��������Ԫ��������Ԫ�������ᡣ25��ʱ��0.1molL-1��Na2C2O4��CH3COONa��NaCN��Na2CO3��Һ��pH�ɴ�С��˳����__��
��2��KHC2O4��Һ�����ԣ���10mL0.01molL-1��H2C2O4��Һ�μ�0.01molL-1KOH��ҺV(mL)���ش��������⣺
�ٵ�V<10mLʱ����Ӧ�����ӷ���ʽΪ___��
�ڵ�V=10mLʱ����Һ��![]() ��
��![]() ��H2C2O4��H+��Ũ���ɴ�С��˳��Ϊ__��
��H2C2O4��H+��Ũ���ɴ�С��˳��Ϊ__��
�۵�V=amLʱ����Һ������Ũ�������¹�ϵ��c(K+)=2c(![]() )+c(
)+c(![]() )����V=bmLʱ����Һ������Ũ�������¹�ϵ��c(K+)=c(
)����V=bmLʱ����Һ������Ũ�������¹�ϵ��c(K+)=c(![]() )+c(
)+c(![]() )+c(H2C2O4)����a__b������<����=������>����.
)+c(H2C2O4)����a__b������<����=������>����.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.10 mol��L-1NaOH��Һ�ζ�20 mL 0.10 mol��L-1HA��Һ����û����Һ��pH��lg![]() �Ĺ�ϵ��ͼ��ʾ������������ȷ����
�Ĺ�ϵ��ͼ��ʾ������������ȷ����
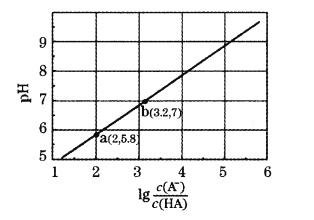
A.HAΪ���ᣬKa��������Ϊ10-3
B.b��ʱ����NaOH��Һ���������20 mL
C.��Һ�ĵ���������b>a
D.b����Һ�У�c(Na+)=c(A��)=(H+)=c(OH��)=10-7mol/L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com