
����Ŀ����1����֪ij�����ļ���ʽΪ![]() ��
��
����ϵͳ������������������___________________��
��������������ϩ����1molH2�ӳɵõ��ģ���ԭϩ���Ľṹ��___________�֡��������������칹����ͬ��
���������ڹ�����������������Ӧ�����ɵ�һ�ȴ��������__________�֡�
��2��ij�л���X��C��H��O����Ԫ����ɣ����ⶨ����Է�������Ϊ90��ȡ1.8gX�ڴ�������ȫȼ�գ��������Ⱥ�ͨ��Ũ����ͼ�ʯ�ң����߷ֱ�����1.08g��2.64g�����л���X�ķ���ʽΪ___________����֪�л���X����һ��һCOOH����1H-NMR ���Ϲ۲���ԭ�Ӹ������������壬ǿ��Ϊ3��1��1��l ����X �Ľṹ��ʽΪ_______________��
���𰸡� 2��2��3-�������� 3 5 C3H6O3 ![]()
����������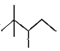 Ϊ2��2��3-�������飬�ʴ�Ϊ��2��2��3-�������飻
Ϊ2��2��3-�������飬�ʴ�Ϊ��2��2��3-�������飻
����Ϊϩ�������������ӳɷ�Ӧ����ȡ���Ʒ���ԭC=C˫������������������̼ԭ���Ͼ�����ԭ�ӵ�̼ԭ�Ӽ��Ƕ�Ӧϩ������̼̼˫����λ�ã�Ӧ��3��ϩ������ͼ��ʾ![]() ���ʴ�Ϊ��3��
���ʴ�Ϊ��3��
�۷����к���5�ֲ�ͬ��H�������ɵ�һ�ȴ��������5�֣��ʴ�Ϊ��5��
(2)���л���ķ���ʽΪCxHyOz���л��������Ϊ1.8g��Ũ�������ؼ�ˮ������Ϊ1.08g����ʯ�����ؼ�������̼������Ϊ2.64g��n(CxHyOz)= ![]() =0.02mol��n(H2O)=
=0.02mol��n(H2O)= ![]() =0.06mol��n(CO2)=
=0.06mol��n(CO2)= ![]() =0.06mol��������ԭ�ӡ�̼ԭ���غ㽨����ϵʽ��0.02x=0.06��0.02y=0.06��2�����x=3��y=6�����Է�Ӧ�����ʽΪC3H6O2������Ϊ�л��������Ϊ90�����л�����Oԭ����Ϊ
=0.06mol��������ԭ�ӡ�̼ԭ���غ㽨����ϵʽ��0.02x=0.06��0.02y=0.06��2�����x=3��y=6�����Է�Ӧ�����ʽΪC3H6O2������Ϊ�л��������Ϊ90�����л�����Oԭ����Ϊ![]() =3�����Ƶ��л������ʽΪC3H6O3�������л��ﺬ���Ȼ����Ҹ��л���ĺ˴Ź�������ͼ�г���4�����շ壬˵������4����ԭ�ӣ������Ϊ3��1��1��1������������ԭ�Ӹ���֮��Ϊ3��1��1��1��������ṹ��ʽΪ
=3�����Ƶ��л������ʽΪC3H6O3�������л��ﺬ���Ȼ����Ҹ��л���ĺ˴Ź�������ͼ�г���4�����շ壬˵������4����ԭ�ӣ������Ϊ3��1��1��1������������ԭ�Ӹ���֮��Ϊ3��1��1��1��������ṹ��ʽΪ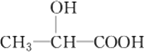 ���ʴ�Ϊ��C3H6O3��
���ʴ�Ϊ��C3H6O3��![]() ��
��


 �����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е��������ʲ����Ժ��ֱ�����ϣ�ֻҪ�����������ʵ���һ��������ȫȼ������O2���������ֲ������( )
A. C2H4��C2H6O B. C2H6��C2H6O C. C3H6��C2H4 D. C3H4��C2H6O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�������ʵ��װ�ã��ⶨ�����ǻ�ԭ����������ͭ���ú�ɫ���ʵ���ɡ�����˵������ȷ����

A. ��װ��a�е�Zn����CaCO3Ҳ���Ʊ�CO2����
B. ����ȥbװ�ã���ᵼ�¸����ʺ������ⶨ���ƫ��
C. ֻ�����װ��d��Ӧǰ��������Ϳ�ȷ�������ʵ����
D. װ��e�������Ƿ�ֹ�����е�H2O��CO2�Ƚ���װ��d��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪W��X��Y��ZΪ������Ԫ�أ�W��Zͬ���壬X��Y��Zͬ���ڣ�W����̬�⻯����ȶ��Դ���Z����̬�⻯���ȶ��ԣ�X��YΪ����Ԫ�أ�X�������ӵ�������С��Y�������ӵ������ԣ�����˵����ȷ����
A. X��Y��Z��W��ԭ�Ӱ뾶���μ�С
B. W��X�γɵĻ�������ֻ�����Ӽ�
C. W����̬�⻯��ķе�һ������Z����̬�⻯��ķе�
D. ��W��Y��ԭ���������5��������γɻ�����Ļ�ѧʽһ��ΪY2W3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ũ�ȹ�ϵ��ȷ���ǣ�������
A. 0.1mol/L��NH4HSO4��Һ�еμ�0.1mol/L��Ba��OH��2��Һ�������պ���ȫ��c��NH4+����c��OH-����c��SO42-����c��H+��
B. ����CO2ͨ��0.1mol/LNa2CO3��Һ����Һ���ԣ�����Һ�У� 2c��CO32-��+c��HCO3-��=0.1mol/L
C. 0.1mol/L��NaOH��Һ��0.2mol/L��HCN��Һ�������ϣ�������Һ�ʼ��ԣ�c��Na+����c��CN-����c��HCN����c��OH-����c��H+��
D. ��1L 1mol/L��KOH����Һ��ͨ��һ������Cl2��ǡ����ȫ��Ӧ��������ء�������غ��Ȼ��صĻ����Һ��c��K+��+c��H+��=6c��ClO3-��+2c��ClO-��+c��HClO��+c��OH-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���˵����ȷ���ǣ�������
A. HCl��NaOH��Ӧ���к��ȡ�H=��57.3 kJ/mol����H2SO4��Ba(OH)2��Ӧ���к��ȡ�H=2��(��57.3) kJ/mol
B. ��֪C2H5OH(l)��ȼ������1366.8 kJ/mol����C2H5OH(l)+3O2(g) �T 2CO2(g)+3H2O(g) ��Ӧ�ġ�H=��1366.8 kJ/mol
C. һ��������2SO2(g)+O2(g)![]() 2SO3(g) ��H1<0��2SO2(g)+O2(g)
2SO3(g) ��H1<0��2SO2(g)+O2(g)![]() 2SO3(l) ��H2<0�����H1����H2
2SO3(l) ��H2<0�����H1����H2
D. ��һ���¶Ⱥ�ѹǿ�£���0.5mol N2��1.5 mol H2�����ܱ������г�ַ�Ӧ����NH3��g�����ų�����19.3 kJ�������Ȼ�ѧ����ʽΪN2(g)+3H2(g)![]() 2NH3(g) ��H=��38.6kJ/mol
2NH3(g) ��H=��38.6kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��Ǧ���صĹ���ԭ��ʾ��ͼ������ܷ�Ӧʽ��Pb��PbO2��2H2SO4 ![]() 2PbSO4��2H2O��������˵����ȷ����
2PbSO4��2H2O��������˵����ȷ����

A. �ŵ�ʱ��PbO2������
B. ���ʱ������Ũ������
C. ���ʱ��BӦ���Դ����������
D. �ŵ�ʱ��������Ӧ��Pb��2e����SO![]() ��PbSO4
��PbSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش��������⣺
��1�����������У��پƾ� ���ۻ���KNO3 ��CaCO3 ������������Һ ��ͭ ��SO2
�������ڵ���ʵ���_________�����ţ���ͬ�������ڷǵ���ʵ���__________��
��2�����������ӵĽṹʾ��ͼ________________������������ά�����ʵĻ�ѧʽ_______��
��3����֪����������������NaOH��Һ�ɷ������·�Ӧ��3Cl2+6NaOH��5NaCl+NaClO3+3H2O
a��������淴Ӧ����ת�Ƶķ������Ŀ_______��
b�����Ϸ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ_________��
c������21.3g Cl2�μӷ�Ӧ��ת�Ƶĵ�����Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ������˵����ȷ���ǣ� ��
A. 5NH4NO3![]() 2HNO3��4N2����9H2O��Ӧ�У�����28gN2��ת�Ƶĵ�����ĿΪ3.75NA
2HNO3��4N2����9H2O��Ӧ�У�����28gN2��ת�Ƶĵ�����ĿΪ3.75NA
B. �����£�0.2mol��L-1��Na2SO4��Һ�к�Na+��ĿΪ0.4NA
C. ��״���£�NA��HF������ռ�����ԼΪ22.4L
D. �����£�0.2molFe������ˮ������Ӧ�����ɵ�H2������ĿΪ0.3NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com