
【题目】A、B、C、D是四中短周期元素,原子序数依次增大,且只有C为金属元素,A、C位于同一主族,B的最外层电子数为次外层的3倍,B、C的最外层电子数之和与D的最外层电子数相等,请回答下列问题:
(1)D元素在元素周期表中的位置____________,写出实验室制取D单质的化学方程式_____________。
(2)A、B、C形成的化合物所含化学键类型___________________。
(3)用电子式表示C、D构成化合物形成过程______________
(4)由元素B和D形成的单质或化合物能用于自来水消毒的是_________、_________。
【答案】(1)第三周期第ⅦA族 (1分,有错不给分)MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(2)离子键、共价键 (1分,只答出一种不给分)
(3)![]() ;
;
(4)O3、Cl2、ClO2中两种即给分。
【解析】试题分析:短周期元素A、B、C、D原子序数依次增大,B的最外层电子数是次外层的3倍,最外层电子数不超过8个,则次外层为K层,则B为O元素;B、C的最外层电子数之和与D的最外层电子数相等,B的最外层电子数为6,D为短周期元素,如果D是Cl元素,则C是Na元素,A、C是同一主族,则A是H元素;如果D是Ar元素,则C是Mg原子,A、C是同一主族,A为Be元素,不符合只有C是金属元素条件,故舍去;所以A、B、C、D分别是H、O、Na、Cl元素。(1)D是Cl元素。主族元素原子核外电子层数等于其周期数、最外层电子数等于其族序数,Cl原子核外有3个电子层、最外层电子数是7,所以位于第三周期第VIIA族;在实验室是用浓盐酸与MnO2混合加热的方法制取氯气,反应的方程式是:MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑;(2)A、B、C三种元素组成的常见化合物NaOH,该化合物是离子化合物,含有离子键、极性共价键;(3)C、D构成化合物是NaCl,用电子式表示该化合物形成过程是
MnCl2+2H2O+Cl2↑;(2)A、B、C三种元素组成的常见化合物NaOH,该化合物是离子化合物,含有离子键、极性共价键;(3)C、D构成化合物是NaCl,用电子式表示该化合物形成过程是![]() ;(4)由元素B和D形成的单质或化合物能用于自来水消毒的是O3、Cl2、ClO2等。
;(4)由元素B和D形成的单质或化合物能用于自来水消毒的是O3、Cl2、ClO2等。


科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成SO3的反应
C. Fe(SCN)3溶液中加入固体KSCN后颜色变深
D. 由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:

(1)定性比较:图甲可通过观察___________,定性比较得出结论。有同学提出将CuSO4改为CuCl2更合理,其理由是_____________。
(2)定量比较:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中进行反应:2SO2(g)+O2(g) ![]() 2SO3(g),已知反应进行到10秒时,SO2、O2、SO3的物质的量分别为0.2mol、0.1mol、0.2mol,则下列说法正确的是
2SO3(g),已知反应进行到10秒时,SO2、O2、SO3的物质的量分别为0.2mol、0.1mol、0.2mol,则下列说法正确的是
A .10秒时,用O2表示该反应的平均反应速率为0.01mol/(L·s)
B.当反应达到平衡时,SO3的物质的量可能为0.4mol
C.档SO2和O2的生成速率之比为2:1时,达到该反应限度
D.向容器内充入SO2,可以提高反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶须是由高纯度单晶生长而成的微纳米级的短纤维,工业应用的晶须主要是在人工控制条件下合成。
碳酸镁晶须(MgCO3·nH2O,n = 1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域。制取碳酸镁晶须的步骤如图:
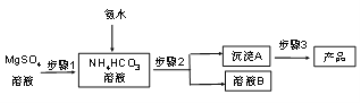
完成下列填空:
(1)步骤1必须将反应的温度控制在50℃,较好的加热方法是_______________________;氨水、硫酸镁、碳酸氢铵三者反应,除生成MgCO3·nH2O沉淀外,同时生成的产物还有______________________________________。
(2)步骤2是__________、洗涤,检验沉淀A已洗涤干净的方法是_____________________。
为测定碳酸镁晶须产品中n的值,某兴趣小组设计了如下装置,并进行了三次实验。(不考虑稀盐酸的挥发性)
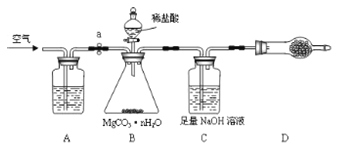
(3)装置A中盛放的溶液是_____________。装置D中盛放的固体是___________________,其作用是_________________________________。
(4)若三次实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,则n值为__________________(用含a的代数式表达)。
(5)下列选项中,会造成实验结果偏大的是____________。 (选填序号)
①实验开始,未先通空气,即称量装置C; ②B中反应结束后,没有继续通空气;
③缺少装置A; ④缺少装置D;
⑤装置B中稀盐酸的滴加速率过快; ⑥装置C中的NaOH溶液浓度过大。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生命的物质基础是组成细胞的元素和化合物,图中序号代表不同的化合物,面积不同代表含量不同,其中Ⅰ和Ⅱ代表两大类化合物。请据图分析下列叙述正确的是( )
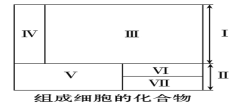
A. 若Ⅴ和Ⅵ分别代表蛋白质和脂质,则Ⅶ代表核酸
B. 上述物质中氧原子含量最高的化合物是Ⅱ
C. 医用生理盐水和糖溶液中的溶质分别属于Ⅳ和Ⅴ
D. 细胞干重和鲜重中含量最多的分别是Ⅴ和Ⅲ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的短周期元素,A元素气态氢化物的水溶液呈碱性,B为最活泼的非金属元素,C元素的原子的电子层数是最外层电子数的3倍,D元素最高化合价为+6价。
(1)A元素气态氢化物的电子式为_____,B在周期表中的位置____。
(2)DBn做制冷剂替代氟利昂,对臭氧层完全没有破坏作用,是一种很有发展潜力的制冷剂。该物质的摩尔质量为146g·mol-1,该物质的化学式为___。已知DBn 在温度高于45度时为气态。DBn属于____晶体。
(3)C与氢元素组成1:1的化合物,与水发生剧烈反应生成一种气体,写出该反应化学反应方程式_______。
(4)D元素的+4价含氧酸钠盐,该钠盐在空气中容易变质,设计实验方案证明该盐已经变质____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com