

| A. | 滤液A中的阳离子为Fe2+、Fe3+、H+ | B. | 样品中Fe元素的质量为2.24 g | ||
| C. | 样品中CuO的质量为4.0 g | D. | V=896 mL |
分析 氧化性:Fe3+>Cu2+>H+,铁离子优先反应,其次是氢原子与铁反应,由于滤液中不含铜离子,且有气体氢气生成,则滤渣3.2g为金属铜,物质的量为0.05mol,即合金样品中总共含有铜元素0.05mol;滤液A中不含铁离子,则最后灼烧得到的固体3.2g为Fe2O3,物质的量为0.02mol,铁元素的物质的量为0.04mol,据此进行解答.
解答 解:A.由于氧化性Fe3+>Cu2+>H+,铁离子优先反应,所以滤液中一定不存在铁离子,故A错误;
B.滤液A中含有亚铁离子和氢离子,加入足量氢氧化钠溶液后,过滤,最后灼烧得到的固体为氧化铁,3.2g氧化铁的物质的量为0.02mol,含有铁元素的物质的量为0.02mol×2=0.04mol,样品中所有铁元素都生成了氧化铁,所以样品中Fe元素的质量为:56g/mol×0.04mol=2.24g,故B正确;
C.由于生成了氢气、滤液中不含铜离子,滤渣3.2g为金属铜,铜元素的物质的量为0.05mol,若全部为氧化铜,氧化铜的质量为:80g/mol×0.05mol=4.0g,由于部分铜被氧化成氧化铜,则样品中氧化铜的质量一定小于4.0g,故C错误;
D.由于部分铁用于置换金属铜,则与氢离子反应生成氢气的铁的物质的量小于0.04mol,反应生成的气体的物质的量小于0.04mol,标况下生成的气体的体积一定小于:22.4mol/L×0.04mol=0.896L=896mL,故D错误;
故选B.
点评 本题考查了铁、铜单质及其氧化物的性质,题目难度中等,注意掌握铁、铜的单质及其化合物性质,明确离子的氧化性强弱是解题关键,试题培养了学生的分析、理解能力


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 只含有共价键的物质一定是共价化合物 | |
| C. | 离子化合物中可能含有极性共价键或非极性共价键 | |
| D. | 氦分子中含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +R2C$\stackrel{催化剂}{→}$
+R2C$\stackrel{催化剂}{→}$ (R为烷基)
(R为烷基)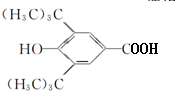 ;E中含有的官能团名称是羟基和醛基;
;E中含有的官能团名称是羟基和醛基; $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O;该反应类型为消去反应;
+H2O;该反应类型为消去反应; +CH3CH2CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3CH2CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$ +H2O;该反应类型为酯化反应;
+H2O;该反应类型为酯化反应;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol过氧化钠与足量水反应转移2NA个电子 | |
| B. | 24克03和标准状况下11.2L氮气含有相同的分子数 | |
| C. | 1.8克重水(D2O)中所含质子数为NA | |
| D. | 100 mL 1.5mol/L氯化镁溶液中含0.15 mol Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,C的化学式为Mg(OH)2
,C的化学式为Mg(OH)2查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向沸水中滴加饱和的氯化铁溶液制取胶体:Fe3++3H2O═Fe(OH)3↓+3H+ | |
| B. | 碳酸氢镁溶液中加入足量的氢氧化钠溶液:Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| C. | 硝酸铝溶液中加入过量的氨水:Al3++4NH3+2H2O═AlO2-+4NH4+ | |
| D. | 淀粉碘化钾试纸在潮湿空气中变蓝:4I-+O2+2H2O═2I2+4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量探究实验1的残留固体放入试管中,加入蒸馏水 | 试管外壁不发烫 | 固体中一定没有 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com