
| n |
| V |
| n |
| V |
| m |
| M |
| 2.33g |
| 233g/mol |
| 0.01mol |
| 0.1L |
| 1 |
| 2 |


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
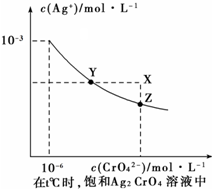 ��֪��t��ʱ��Ag2CrO4����ɫ���壩��ˮ�еij����ܽ�ƽ��������ͼ��ʾ�� t��ʱAgCl��Ksp=2��10-10������˵����ȷ���ǣ�������
��֪��t��ʱ��Ag2CrO4����ɫ���壩��ˮ�еij����ܽ�ƽ��������ͼ��ʾ�� t��ʱAgCl��Ksp=2��10-10������˵����ȷ���ǣ�������| A��t��ʱ��Y���Ӧ��Ksp��Ag2CrO4��Ϊ1��10-9 |
| B��t��ʱ��Ag2CrO4���ܽ�ȣ�mol/L��С��AgCl |
| C��t��ʱ����ʹ��Һ��Z�㵽X�㣬�ɲ�ȡ�ڱ���Ag2CrO4��Һ�м�������AgNO3����İ취ʵ�� |
| D��t��ʱ�����ó����ζ������ñ�AgNO3��Һ�ζ�KCl��Һ��Ũ��ʱ���ɵ��뼸��K2CrO4��Һ��ָʾ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��HClO�ĵ���ʽ��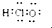 | ||
B��Mg2+�Ľṹʾ��ͼ��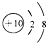 | ||
| C�����������Ľṹ��ʽ��CH3COOCCH3 | ||
D������16�����ӣ�16�����Ӻ�18�����ӵĵ���������
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CO2+ NaOH=NaHCO3 | ||||
B��Fe2O3+3H2
| ||||
| C��Cu+2 FeCl3=2FeCl2+Cu | ||||
| D��2F2+2H2O=4HF+O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������Ӧ���е������ɣ����Զ����û���Ӧ |
| B����Ӧ�ٺͷ�Ӧ���о�����Br2����Ԫ�ط����ı仯��ͬ |
| C����Ӧ���б������뱻��ԭ���ʵ����ʵ���֮��Ϊ6��1 |
| D������lmol��ԭ����Ӧ���������õ����ӵ����ʵ���Ϊ10mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2�� |
| B������������Һ����ϡ�����У�OH-+H+�TH2O |
| C��ʯ��ʯ����ϡ�����У�CaCO3+2H+=Ca2++CO2��+H2O |
| D��ͭƬ������������Һ�У�Cu+Ag+�TCu2++Ag |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ԭ������ͬ |
| B��������������ͬ |
| C��ͬ��ͬѹ�£����������ͬ |
| D��ͬ��ͬѹ�£�������ܶ���ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��12
| ||
B��12
| ||
C��
| ||
| D��bNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
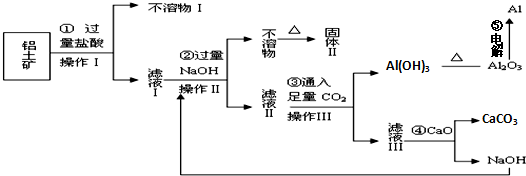
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com