碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容.
(1)已知2.00g的C
2H
2完全燃烧生成液态水和二氧化碳气体放出99.6kJ热量,写出表示C
2H
2燃烧热的热化学方程式
.
(2)利用上述反应设计燃料电池(电解质溶液为氢氧化钾溶液),写出电池负极的电极反应式
.
(3)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N
2(g)+CO
2(g).
某研究小组向一个容积不变的密闭真空容器(容器容积为3L,固体试样体积忽略不计)中加入NO和足量的活性炭,在恒温(T
1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如下:
n/mol
t/min |
NO |
N2 |
CO2 |
| 0 |
2.00 |
0 |
0 |
| 10 |
1.16 |
0.42 |
0.42 |
| 20 |
0.80 |
0.60 |
0.60 |
| 30 |
0.80 |
0.60 |
0.60 |
①10min~20min以v(NO)表示的反应速率为
.
②根据表中数据,计算T
1℃时该反应的平衡常数为
(保留两位小数).
③下列各项能判断该反应达到平衡状态的是
(填序号字母).
A.容器内压强保持不变 B. 2v(NO)
(正)=v(N
2)
(逆)C.容器内CO
2的体积分数不变 D.混合气体的密度保持不变
④一定温度下,随着NO的起始浓度增大,则NO的平衡转化率
(填“增大”、“不变”或“减小”).
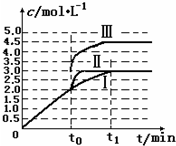
(4)在3L容积可变的密闭容器中发生反应H
2(g)+CO
2(g)═H
2O(g)+CO(g),恒温下c(CO)随反应时间t变化的曲线Ⅰ如图所示.若在t
0时分别改变一个条件,曲Ⅰ变成曲线Ⅱ和曲线Ⅲ.
①当曲线Ⅰ变成曲线Ⅱ时,改变的条件是
;
②当曲线Ⅰ变成曲线Ⅲ时,改变的条件及改变条件的变化量分别是
.

 碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容.
碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容.
