
��һ�ܱպ��ݵ������У����淴Ӧ3A(g) 3B(��)��C(��)�������仯��ͼ����ʾ�������ƽ����Է���������ʱ��ı仯��ͼ����ʾ��
3B(��)��C(��)�������仯��ͼ����ʾ�������ƽ����Է���������ʱ��ı仯��ͼ����ʾ��
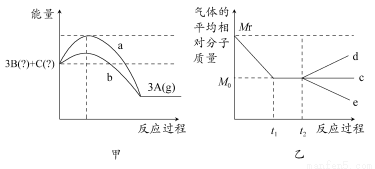
(1)��ͼ�����ж�3A(g) 3B(��)��C(��)������Ӧ��________��Ӧ(��������������������)��ʵ��a��ʵ��b��Ƚϣ����������ķ�Ӧ������________��
3B(��)��C(��)������Ӧ��________��Ӧ(��������������������)��ʵ��a��ʵ��b��Ƚϣ����������ķ�Ӧ������________��
(2)��ͼ�ҿ��Եó��й�B��C״̬�Ľ�����________��
����t2ʱ�������¶ȣ������ƽ����Է��������仯һ������________��(����c����d������e��)��
�����ı�ѹǿ�������ƽ����Է��������仯һ������c�ߣ���C���ʵ�״̬Ϊ________��
(3)���ƽ����¶Ȳ��䣬�������������һ������ƽ��ʱA��Ũ����ԭ����60%����B��________״̬��C��________״̬��
(4)���BΪ���壬CΪ���壬ȡ0.3 mol A��������1 L�����г�ַ�Ӧ��ƽ��ʱ���B��Ũ��Ϊ0.21 mol/L����ʹ��Ӧ���淴Ӧ��ʼ����ʼʱ�������м���0.3 mol B��ͬ�������£�Ҫʹƽ��ʱB��Ũ����Ϊ0.21 mol/L����C�����ʵ�����ȡֵ��ΧӦ����________��
(1)���ȣ�ʵ��b���˴�����(2)B��C��������һ��Ϊ���塡��e��������̬��(3)�����Һ�壻���� (4)n(C)>0.03 mol
��������ͼ���ǻ�ѧ��Ӧ�����������仯�Ĺ�ϵͼ����ȻB��C��������A�Ƿ��ȷ�Ӧ����3A(g) 3B(��)��C(��)����Ӧ�����ȷ�Ӧ��ʵ��b��Ӧ��Ҫ���������ͣ�����ʹ���˴�������ͼ�ҿ��Կ������ӷ�Ӧ��ʼ��ƽ��״̬����������ƽ����Է���������С�������ֿ��ܣ�һ������������������ˣ�B��C��Ϊ���壬һ�����������������ˣ�B����C��һ�������壬���ԣ�B��C��������һ��Ϊ���壬��t2ʱ�������¶ȣ�ƽ�������ƶ��������ƽ����Է���������С������ͼ��e�����ı�ѹǿ�������ƽ����Է����������䣬��÷�ӦΪһ�������������ķ�Ӧ��BΪ���壬CΪ�����塣���ƽ����¶Ȳ��䣬�������������һ������ƽ��ʱA��Ũ����ԭ����60%��˵��ƽ�������ƶ���������Ϊ������������ӵķ�Ӧ����BΪ�����壬CΪ���塣��Ϊ�Ǻ�������������Ҫʹƽ��ʱB��Ũ����ȣ�Ӧ�ü���ķ�Ӧ������൱��C�ǹ��壬ֻҪ�������з�Ӧ���輴�ɣ�ƽ��ʱC��Ӧ��0.03 mol������C�����ʵ���Ӧ�ô���0.03 mol��
3B(��)��C(��)����Ӧ�����ȷ�Ӧ��ʵ��b��Ӧ��Ҫ���������ͣ�����ʹ���˴�������ͼ�ҿ��Կ������ӷ�Ӧ��ʼ��ƽ��״̬����������ƽ����Է���������С�������ֿ��ܣ�һ������������������ˣ�B��C��Ϊ���壬һ�����������������ˣ�B����C��һ�������壬���ԣ�B��C��������һ��Ϊ���壬��t2ʱ�������¶ȣ�ƽ�������ƶ��������ƽ����Է���������С������ͼ��e�����ı�ѹǿ�������ƽ����Է����������䣬��÷�ӦΪһ�������������ķ�Ӧ��BΪ���壬CΪ�����塣���ƽ����¶Ȳ��䣬�������������һ������ƽ��ʱA��Ũ����ԭ����60%��˵��ƽ�������ƶ���������Ϊ������������ӵķ�Ӧ����BΪ�����壬CΪ���塣��Ϊ�Ǻ�������������Ҫʹƽ��ʱB��Ũ����ȣ�Ӧ�ü���ķ�Ӧ������൱��C�ǹ��壬ֻҪ�������з�Ӧ���輴�ɣ�ƽ��ʱC��Ӧ��0.03 mol������C�����ʵ���Ӧ�ô���0.03 mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 9-1 ��ʯȼ�����л���������ϰ���������棩 ���ͣ�ѡ����
��4��̼�����µ������������ж���ȷ����( )
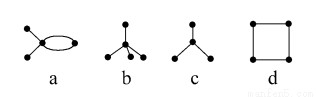
A��c��d��ͬ���칹��
B��b��c��ͬϵ��
C��a��d���ܷ����ӳɷ�Ӧ
D��ֻ��b��c�ܷ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 8-2 ��Һ���������ϰ���������棩 ���ͣ������
�����£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH���±���
ʵ���� | HB���ʵ���Ũ��(mol/L) | KOH���ʵ���Ũ��(mol/L) | �����Һ��pH |
�� | 0.2 | 0.2 | pH��a |
�� | c1 | 0.2 | pH��7 |
�� | 0.1 | 0.1 | pH>7 |
�� | 0.1 | 0.1 | pH��9 |
��ش��������⣺
(1)�������������ʵ���������Ӽ�����������������a(�����Һ��pH)��˵��HB��ǿ�ỹ������________��
(2)�������������ʵ�����������������������c1�Ƿ�һ������0.2 mol/L________��(����������������)�������Һ������Ũ��c(B��)��c(K��)�Ĵ�С��ϵ��________��
A��ǰ�ߴ� B�����ߴ�
C��������� D�����ж�
(3)�ӱ���ʵ����������HB��________��(����ǿ����������)���û����Һ������Ũ���ɴ�С��˳����________��
(4)����ʵ�����û����Һ����ˮ�������c(OH��)��________mol/L��д���û����Һ��������ʽ�ľ�ȷ���(���������Ƽ���)��c(K��)��c(B��)��_mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 8-1 ������ʵĵ���ƽ����ϰ���������棩 ���ͣ�ѡ����
ˮ�ĵ���ƽ����������ͼ��ʾ������˵����ȷ����(����)
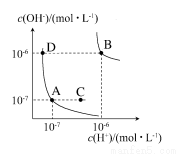
A��ͼ�ж�Ӧ����¶ȹ�ϵΪA>B
B��ˮ�ĵ��볣��KW��ֵ��С��ϵΪB>D
C���¶Ȳ��䣬��������NaOH��ʹ��Һ��C��䵽A��
D����B���Ӧ�¶��£���pH��2��H2SO4��pH��10��NaOH��Һ�������Ϻ���Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 8-1 ������ʵĵ���ƽ����ϰ���������棩 ���ͣ�ѡ����
���в����У���ʹ����ƽ��H2O H����OH�������ƶ�����Һ�����Ե���(����)
H����OH�������ƶ�����Һ�����Ե���(����)
A����ˮ�м���NaHSO4��Һ
B����ˮ�м���Al2(SO4)3��Һ
C����ˮ�м���Na2CO3��Һ
D����ˮ���ȵ�100��C��ʹpH��6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 7-3 ��ѧƽ����ƶ���ϰ���������棩 ���ͣ�ѡ����
��֪���淴Ӧ��X(s)��aY(g) bZ(g)����H����Ӧ�ﵽƽ��ʱ���¶ȡ�ѹǿ�Կ��淴Ӧ��Ӱ������ͼ��ʾ(ͼ��pΪѹǿ������p1>p2)�������й��ж���ȷ����(����)
bZ(g)����H����Ӧ�ﵽƽ��ʱ���¶ȡ�ѹǿ�Կ��淴Ӧ��Ӱ������ͼ��ʾ(ͼ��pΪѹǿ������p1>p2)�������й��ж���ȷ����(����)
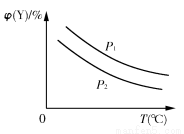
A�����淴Ӧ���ʱ���H<0
B����Ӧ�Ļ�ѧ������a<b
C���ÿ��淴Ӧ��ƽ�ⳣ��K��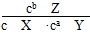
D���¶ȡ�ѹǿ���䣬��ʹ�ú��ʵĴ������������Y��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 7-3 ��ѧƽ����ƶ���ϰ���������棩 ���ͣ�ѡ����
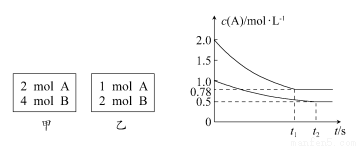
��ס��������ݻ���Ϊ1 L�ĺ��������У��ֱ����2 mol A,4 mol B��1 mol A,2 mol B����ͬ�����£��������з�Ӧ��A(g)��2B(g) xC(g)����H<0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ������˵����ȷ���� (����)
xC(g)����H<0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ������˵����ȷ���� (����)
A��x���ܵ���3
B����ƽ�����������г��뺤����ʹA��ת���ʽ���
C�����������������£�c(A)�ɴﵽ0.78 mol/L
D��������������ٳ���2 mol A,4 mol B��ƽ��ʱ��������c(A)����1.56 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 7-2 ��ѧ��Ӧ�ķ��������ϰ���������棩 ���ͣ�ѡ����
250��C��1.01��105Paʱ����Ӧ2N2O5(g)=4NO2(g)��O2(g)����H����56.76 kJ/mol���Է����е�ԭ����(����)
A�������ȷ�Ӧ B���Ƿ��ȷ�Ӧ C�����ؼ���Ӧ D������ЧӦ��������ЧӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 6-2 ԭ��ء������Ļ�ѧ��Դ��ϰ���������棩 ���ͣ�ѡ����
�߹���Ni/MH(M��ʾ����Ͻ�)����Ѿ����ڻ�϶����������ܷ�Ӧ����ʽ���£�
Ni(OH)2��M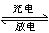 NiOOH��MH������������ȷ����(����)
NiOOH��MH������������ȷ����(����)
A���ŵ�ʱ����������Һ�ļ�����ǿ
B���ŵ�ʱ������ӦΪ��M��H2O��e��=MH��OH��
C�����ʱ������ӦΪ��NiOOH��H2O��e��=Ni(OH)2��OH��
D���ŵ�ʱÿת��1 mol���ӣ�������1 mol NiOOH������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com