
【题目】科学家通过密度泛函理论研究甲醇与水蒸气重整制氢反应机理时,得到甲醇在Pd(Ⅲ)表面发生解离时四个路径与相对能量关系如图所示,其中附在Pd(Ⅲ)表面的物种用*标注。下列说法错误的是
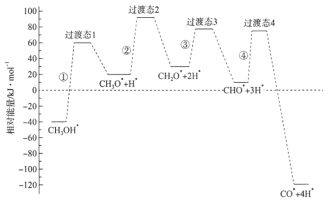
A.②中包含C—H键的断裂过程
B.该历程中能垒(反应活化能)最小的是③
C.该历程中制约反应速率的方程式为CH3O*+3H* CO*+4H*
D.由此历程可知:![]() △H<0
△H<0
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。磷酸铁锂锂离子电池充电时阳极反应式为:LiFePO4 -xLi+ -xe-→ xFePO4 +(1-x)LiFePO4。放电工作示意图如图。下列叙述不正确的是
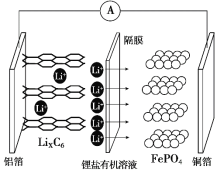
A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铝箔沿导线流向铜箔
C.放电时正极反应为:FePO4+xLi+ +xe-→xLiFePO4 +(1-x)FePO4
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分离和提纯是化学研究物质的基本方法。请选择分离提纯下列物质所用的装置(填字母序号):
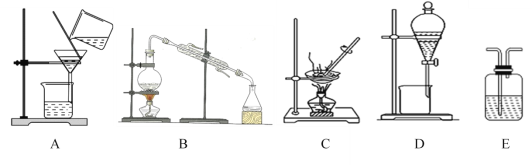
(1)除去粗食盐水中的泥沙___;
(2)用CCl4萃取碘水中的碘___;
(3)用自来水制取蒸馏水___;
(4)用酸性KMnO4溶液除去CO2中的SO2___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g) ![]() CH3OH(g) 反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
CH3OH(g) 反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
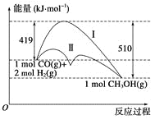
A.生成1mol CH3OH(g)时,该反应吸收的热量为91 kJ。
B.加入催化剂可以减少反应最终放出的热量
C.1mol CO(g)与2molH2(g)的总能量大于1mol CH3OH(g)的总能量
D.如果该反应生成CH3OH (l),则放出的能量会减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,电流表指针发生偏转,同时A极质量减少,B极上有气泡产生,C为电解质溶液,

下列说法错误的是
A. B极为原电池的正极
B. A、B、C可能分别为Zn、Cu、稀盐酸
C. C中阳离子向A极移动
D. A极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是人类最早使用的金属之一,其单质及化合物具有广泛的用途。
(1)基态铜原子核外有________对自旋相反的电子。
(2)青铜是铜与锡或铅等元素按一定比例熔铸而成的合金。第一电离能I1(Sn)____________I1(Pb)(填“大于”或“小于”)。
(3)新制的Cu(OH)2能够溶解于浓氨水中,反应的离子方程式是____________________________________;
(4)利用铜片表面催化反应,我国研究人员用六炔基苯为原料,在世界上首次通过化学方法获得全碳材料—石墨炔薄膜(结构片段如图所示),开辟了人工化学合成碳同素异形体的先例。石墨炔中碳原子_________________________的杂化方式。

(5)CuCl的盐酸溶液能吸收CO形成氯化羰基亚铜(I),可用于定量测定气体混合物中CO的含量。氯化羰基亚铜(I)中含___________σ键数目。
(6)Cu2O可用于半导体材料。
①Cu2O晶胞(如图所示)中,O原子的配位数为________________;a位置Cu+坐标为(0.25,0.25,0.75),则b位置Cu+坐标_______________________。
②Cu2S与Cu2O具有相似晶体结构,则两者的熔点是Cu2O比Cu2S的_________(填“高”或“低”),请解释原因___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
A.平衡时,v正(O2)=v逆(O2)必成立
B.关系式5v正(O2)=4v正(NO)总成立
C.用上述四种物质NH3、O2、NO、H2O表示的正反应速率的数值中,v正(H2O)最小
D.若投入4 mol NH3和5 mol O2,通过控制外界条件,必能生成4 mol NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室石蜡催化裂化的装置如图所示,关于实验操作或叙述错误的是( )

A.试管Ⅰ连的玻璃导管加长是为使气态石蜡冷凝回流
B.装置Ⅱ中冷水的作用是冷凝收集裂化油
C.酸性KMnO4溶液若倒吸可加快褪色速率
D.试管Ⅲ中溶液颜色变浅甚至褪色可说明有乙烯生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】还原法处理氮的氧化物是环境科学研究的热点课题。
I.氢气还原法。H2还原NO发生的反应为2NO(g)+2H2(g)![]() N2(g)+2H2O(g)。
N2(g)+2H2O(g)。
(1)已知几种化学键的键能数据如下:

2NO(g)+2H2(g)![]() N2(g)+2H2O(g) △H=__________kJ·mol-1
N2(g)+2H2O(g) △H=__________kJ·mol-1
(2)2NO(g)+2H2(g)![]() N2(g)+2H2O(g)的反应速率表达式为v=kc2(NO)·c(H2)(k是速率常数,只与温度有关)。科学研究发现上述反应分两步进行:
N2(g)+2H2O(g)的反应速率表达式为v=kc2(NO)·c(H2)(k是速率常数,只与温度有关)。科学研究发现上述反应分两步进行:
反应1(反应慢):2NO(g)+H2(g)![]() N2(g)+H2O2(g);
N2(g)+H2O2(g);
反应2(反应快):H2O2(g)+H2(g)![]() 2H2O(g)
2H2O(g)
上述两步反应中,活化能较大的是反应__________(填“1”或“2”)。c(NO)对总反应速率的影响程度__________c(H2)(填“大于”“小于”或“等于”)。
II.NH3还原法。在恒容密闭容器中充入NH3和NO2;在一定温度下发生反应: 8NH3(g)+6NO2(g)![]() 7N2(g)+12H2O(g)
7N2(g)+12H2O(g)
(3)下列表明该反应达到平衡状态的是__________(填字母)。
A 混合气体密度保持不变 B NO2和N2的消耗速率之比为6:7
C 混合气体中c(N2)=c(NO2) D 混合气体压强保持不变
III.CO还原法。利用高效催化剂处理汽车尾气中的NO和CO,发生反应: 2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H。在2L恒容密闭容器中充入2 mol CO和2 mol NO,测得NO的转化率与温度、时间的关系如图所示。
N2(g)+2CO2(g) △H。在2L恒容密闭容器中充入2 mol CO和2 mol NO,测得NO的转化率与温度、时间的关系如图所示。
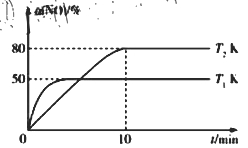
(4)下列说法正确的是_________(填字母)。
A 图像中,T1>T2 B 上述反应在高温下能自发进行
C 10min时,T2K下正、逆反应速率相等 D 增大NO的浓度,反应物的转化率增大
(5)T2K温度下,0-10min内用CO表示的平均反应速率v(CO)=_________mol/L-1·min-1;T1K温度下,上述反应的平衡常数K=_________L·mol-1。
(6)T1K温度下,向平衡后的容器内再加入2 mol N2和2 mol NO,则平衡_________(填“向右移动”“向左移动”或“不移动”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com