
【题目】下列化学用语表达正确的是( )
A.羟基的电子式:![]()
B.乙烯结构简式:CH2CH2
C.R2+离子核外有a个电子,b个中子,R原子表示为:![]() R
R
D.NaClO的电离方程式:NaClO=Na++Cl-+O2-
科目:高中化学 来源: 题型:
【题目】氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料、防腐等工业,它不溶于H2SO4、HNO3和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)4-nCln],随着环境酸度的改变n随之改变。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

(1)写出溶解过程中产生无色气体的化学式:_______。
(2)还原过程中发生的主要反应的离子方程式:______。
(3)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,在真空干燥机内于70℃ 干燥2h,冷却密封包装。70℃, 真空干燥、密封包装的原因是:______。
(4)滤液中主要成分是(NH4)2SO4,工业上用(NH4)2SO4与Al2(SO4)3制取铵明矾,铵明矾在食品,制革等方面有重要用途,写出铵明矾的化学式________。
(5)随着pH值减小[Cu2(OH)4-nCln]中Cu%_______。(填字母)
A.增大 B.不变 C.不能确定 D.减小
(6)如图是各反应物在最佳配比条件下,反应温度对CuCl产率影响。由图可知,溶液温度控制在60℃时,CuCl产率能达到94%,当温度高于65 时,CuCl产率会下降,从生成物的角度分析,其原因可能是______。
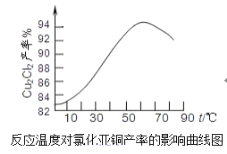
(7)以碳棒为电极电解CuCl2溶液也可得到CuCl,写出电解时阴极上发生的电极反应式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饮用水中的NO3对人类健康会产生危害,为了降低饮用水中NO3的浓度,可以在碱性条件下用铝粉将NO3还原为N2,其化学方程式为:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,被氧化的元素_________,还原产物是________。
(2)用“双线桥法”表示反应中电子转移的方向和数目:_______________。
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(3)反应中每生成标况下22.4L N2,转移_______mol电子。
(4)请配平下列离子方程式。
____Fe2++____H+ +____NO3=____Fe3+ +____N2O↑+____H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+ O2 (g)![]() 2SO3(g) ΔH<0
2SO3(g) ΔH<0
(1)降低温度,该反应K值______,二氧化硫转化率____,化学反应速度____ ,(以上均填增大、减小或不变)
(2)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是_____。
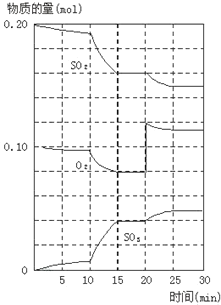
(3)据图判断,反应进行至20min时,曲线发生变化的原因_____(用文字表达)
(4)10min到15min的曲线变化的原因可能是____(填写编号)。
a.加了催化剂 b.缩小容器体积 c.降低温度 d.增加SO3的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象或事实可用同一原理解释的是( )
A. 浓硫酸和浓盐酸长期暴露在空气中浓度降低
B. ![]() 能使溴水和品红溶液褪色
能使溴水和品红溶液褪色
C. ![]() 和
和![]() 溶液使酸性高锰酸钾溶液的紫色褪去
溶液使酸性高锰酸钾溶液的紫色褪去
D. 新制的氨水、氯水放置时间较久而变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习小组研究钠的燃烧反应产物,取金属钠(表面已被氧化),吸干煤油,置于坩埚内,上方倒扣盛满O2集气瓶,加热一段时间,充分反应后观察到产物为白色固体和淡黄色固体的混合物,测得反应前后各物质的质量如下表:
质量/g | ||
反应前 | 坩埚 | 100 |
盛有金属钠的坩埚 | 105.4 | |
反应后 | 盛有固体产物的坩埚 | 107.4 |
请回答下列问题:
(1)根据实验现象,推测固体产物成分为___________________(填化学式)
(2)将产物全部溶于水,观察到有气泡生成,写出该反应的化学方程式为________。
(3)测得上述溶液中n(Na+)=0.2mol,通过计算证实加热过程中存在表面的Na2O转化为Na2O2。___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A.16gO2和O3的混合气体中含有的分子数为0.5NA
B.0.3molAgNO3受热完全分解(2AgNO3=2Ag+2NO2↑+O2↑),用排水法收集到气体的分子数为 0.25NA
C.0.5NA个氯气分子所占体积约是11.2L
D.2.3g金属钠在装有氧气的集气瓶中完全燃烧,转移的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时己知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。

下列说法不正确的是
A.元素甲比Al的最高价氧化物的水化物的碱性弱B.原子半径比较:甲>乙>Si
C.元素乙位于现行元素周期表第四周期第ⅣA族D.推测乙可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室中称取20gNaOH固体,配制500mL1mol·L-1的氢氧化钠溶液。
(1)该同学准备的实验用品有:托盘天平![]() 带砝码
带砝码![]() 、药匙、量筒、玻璃棒等,还缺少的玻璃仪器有__、__、___。
、药匙、量筒、玻璃棒等,还缺少的玻璃仪器有__、__、___。
(2)下列有关实验操作,正确的是__。(多选)
A.称量氢氧化钠固体时,应该放在称量纸上称量
B.某同学将称量的氢氧化钠固体溶解并冷却至室温,然后转移到容量瓶中
C.某同学在定容时,不小心加水超过刻度线,又将多余的液体吸出直至刻度线
D.某同学在溶解、转移完氢氧化钠溶液后,将溶解用的仪器洗涤2~3次,并将洗涤液转移到容量瓶中
(3)玻璃棒在该实验中的作用有①__,②___。
(4)若实验室遇到下列情况,对氢氧化钠溶液的物质的量浓度有何影响![]() 填“偏高”、“偏低”或“无影响”
填“偏高”、“偏低”或“无影响”![]()
①转移时,有少量的溶液洒落出容量瓶__。
②定容时,容量瓶中事先有洁净的蒸馏水,所配溶液的浓度___。
③定容时俯视溶液的凹液面___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com