
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A.16gO2和O3的混合气体中含有的分子数为0.5NA
B.0.3molAgNO3受热完全分解(2AgNO3=2Ag+2NO2↑+O2↑),用排水法收集到气体的分子数为 0.25NA
C.0.5NA个氯气分子所占体积约是11.2L
D.2.3g金属钠在装有氧气的集气瓶中完全燃烧,转移的电子数为0.1NA
【答案】D
【解析】
A.16gO2的物质的量是0.5mol,含有的分子数目是0.5NA;16gO3的物质的量是![]() mol,其中含有的分子数目是
mol,其中含有的分子数目是![]() NA,故16gO2和O3的混合气体中含有的分子数小于0.5NA,A错误;
NA,故16gO2和O3的混合气体中含有的分子数小于0.5NA,A错误;
B.根据方程式可知0.3molAgNO3受热完全分解,发生反应2AgNO3=2Ag+2NO2↑+O2↑,产生0.3molNO2、0.15molO2,用排水法收集气体时,会发生反应:4NO2+O2+2H2O=4HNO3,O2过量,最后剩余O2的物质的量是0.075mol,因此收集到气体的分子数为 0.075NA,B错误;
C.缺条件,不能确定气体的体积,C错误;
D.2.3gNa的物质的量是0.1mol,由于Na是+1价的金属,所以2.3g金属钠在装有氧气的集气瓶中完全燃烧,转移的电子数为0.1NA,D正确;
故合理选项是D。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】二氧化硒(Se)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。完成下列填空:
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1。写出Se和浓HNO3的反应方程式_______________________________________。
(2)已知:Se+2H2SO4(浓)![]() 2SO2↑+SeO2+2H2O
2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O![]() Se+2SO42-+4H+
Se+2SO42-+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是_________________________。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3![]() Se+I2+KNO3+H2O(未配平) ②I2+2Na2S2O3
Se+I2+KNO3+H2O(未配平) ②I2+2Na2S2O3![]() Na2S4O6+2NaI
Na2S4O6+2NaI
实验中,准确称量SeO2样品0.1500g,消耗0.2000 mol·L-1的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—铜空气燃料电池是低成本高效电池。该电池通过一种复杂的铜“腐蚀”现象产生电能,其中放电过程为2Li+Cu2O+H2O===2Cu+2Li++2OH-。下列说法不正确的是
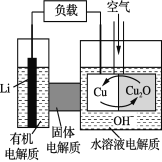
A. 放电时,Li+透过固体电解质向Cu极移动
B. 通空气时,铜被腐蚀,产生Cu2O
C. 放电时,正极的电极反应式为:Cu2O+2H+ +2 e- ===2Cu+H2O
D. 整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表达正确的是( )
A.羟基的电子式:![]()
B.乙烯结构简式:CH2CH2
C.R2+离子核外有a个电子,b个中子,R原子表示为:![]() R
R
D.NaClO的电离方程式:NaClO=Na++Cl-+O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组利用下面的装置进行实验,②、③中溶液均足量,操作和现象如下表。
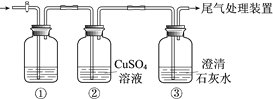
实验 | 操作 | 现象 |
Ⅰ | 向盛有Na2S溶液的①中持续通入CO2至过量 | ②中产生黑色沉淀,溶液的pH降低; ③中产生白色浑浊,该浑浊遇酸冒气泡 |
Ⅱ | 向盛有NaHCO3溶液的①中持续通入H2S气体至过量 | 现象同实验Ⅰ |
资料:CaS遇水完全水解
由上述实验得出的结论不正确的是
A. ③中白色浑浊是CaCO3
B. ②中溶液pH降低的原因是:H2S+Cu2+ == CuS↓+2H+
C. 实验Ⅰ①中CO2过量发生的反应是:CO2+H2O+ S2== CO32+ H2S
D. 由实验Ⅰ和Ⅱ不能比较H2CO3和H2S酸性的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①NaHCO3;②C2H5OH;③Cu;④H2O;⑤石灰乳;⑥CO;⑦Ba(OH)2;⑧盐酸;⑨H2CO3;⑩浓硝酸。
(1)属于电解质的是___(填写序号),属于非电解质的是___(填写序号)。
(2)⑨在水溶液中的电离方程式为___。
(3)⑤与⑧反应的离子方程式为___。
(4)向⑦的溶液中滴加①的溶液至Ba2+恰好完全沉淀,离子方程式为___。
(5)③与⑩反应的离子方程式如下,请配平方程式(在中填入系数,在横线上写上缺少的物质),并用“单线桥”标出电子转移的方向与数目。___
Cu+NO3-+ —Cu2++NO2↑+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是一种新型有机酰胺,在工业生产中有重要的作用,其合成路线如下:
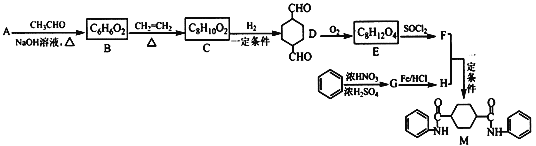
已知:①A是烃的含氧衍生物,相对分子质量为58,碳和氢的质量分数之和为44.8%,核磁共振氢谱显示为一组峰,可发生银镜反应,且5.8 g A完全发生反应生成0.4 mol银。
②R1-CHO+R2-CH2CHO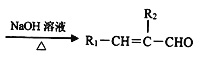
③R-COOH![]() R-COCl
R-COCl
④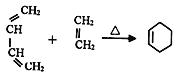
回答下列问题:
(1)A的名称______E的结构简式为____________;G的名称为__________。
(2)B中含有官能团的名称为_______________________。
(3)C→D、D→E的反应类型分别为_____________、_______________。
(4)写出 F+H→M的化学反应方程式_________________。
(5)芳香族化合物W有三个取代基,是C的同分异构体,能与FeCl3溶液发生显色反应。0.5 mol W可与足量的Na反应生成1 g H2,且核磁共振氢谱显示为五组峰,符合以上条件的W的同分异构体共有_______ 种,写出其中一种的结构简式____________。
(6)参照上述合成路线,以C2H4和HOCH2CH2OH为原料(无机试剂任选),设计制备![]() 的合成路线_____________。
的合成路线_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在溶液中可发生以下反应:①16H++10Z-+2![]() ===2X2++5Z2+8H2O,②2M2++R2===2M3++2R-,③2R-+Z2===R2+2Z-,由此判断下列说法错误的是( )
===2X2++5Z2+8H2O,②2M2++R2===2M3++2R-,③2R-+Z2===R2+2Z-,由此判断下列说法错误的是( )
A.氧化性强弱顺序为:![]() <Z2<R2<M3+
<Z2<R2<M3+
B.还原性强弱顺序为:X2+<Z-<R-<M2+
C.Z元素在反应①中被氧化,在③中被还原
D.常温下可发生反应2M2++Z2===2M3++2Z-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用图中所示的装置进行实验,实验现象和预测不一致的是 ( )
| ①中的物质 | ②中的物质 | 预测现象 | |
A | 浓氨水 | FeCl3溶液 | ②中有红褐色沉淀 | |
B | 浓氨水 | 浓盐酸 | ③中有白烟 | |
C | 饱和氯水 | Na2S溶液 | ②中生成淡黄色沉淀 | |
D | 饱和亚硫酸 | 蓝色石蕊试液 | ②中溶液先变红后褪色 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com