
(12分)对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在着一种定量关系:如25 ℃时,HA H++A-,则K=
H++A-,则K=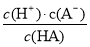 ,式中K为电离平衡常数,只与温度有关,c为平衡浓度。下表是几种弱酸的电离平衡常数(25 ℃)。
,式中K为电离平衡常数,只与温度有关,c为平衡浓度。下表是几种弱酸的电离平衡常数(25 ℃)。
酸 | 电离方程式 | 电离平衡常数K |
CH3COOH | CH3COOH H++CH3COO- | 1.75×10-5 |
H2CO3 | H2CO3 HCO3- | K1=4.4×10-7 K2=4.7×10-11 |
H2S | H2S HS- | K1=1.3×10-7 K2=7.1×10-15 |
H3PO4 | H3PO4 H2PO4- HPO42- | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
回答下列问题:
(1)K只与温度有关,当温度升高时,K值________(填“变大”、“变小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性相对强弱的关系是_____________________________________________________________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看成酸,其中酸性最强的是________,酸性最弱的是________。
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数,对于同一种多元弱酸的K1、K2、K3,总有: ,产生此现象的原因是________________________________________________________________________。
(1)变大 (2)K值越大,酸性越强 (3)H3PO4 HS- (4)当多元弱酸电离出1个H+后,便带一个单位负电荷,再电离时相当于在负电荷的束缚下电离出带正电荷的H+,故越来越难电离,K越来越小 (5) K1?K2?K3
【解析】
试题分析:(1)弱酸的电离是吸热反应,升高温度促进弱酸电离,所以电离平衡常数增大,故答案为:增大;
(2)同一温度下,酸的电离常数越大其电离程度越大,则酸性越强,故答案为:Ka值越大酸性越强;
(3)同一温度下,酸的电离常数越大其酸性越强,根据酸的电离常数知,酸性最强的是H3PO4,最弱的是HPO42-,故答案为:H3PO4;HPO42-;
(4)产生相同离子时抑制电解质的电离,多元弱酸电离时上一级电离产生的H+对下一级电离有抑制作用,所以其电离常数逐渐减小,故答案为:上一级电离产生的H+对下一级电离有抑制作用.
考点:弱电解质的电离平衡。


科目:高中化学 来源:2014-2015学年吉林省长春市新高三起点调研考试化学试卷(解析版) 题型:填空题
(13分)
(1)将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s) 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡气体总浓度(×10-3 mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
氨基甲酸铵分解反应的焓变ΔH 0(填“>”、“<”或“=”)。
可以判断该分解反应已经达到化学平衡的是 。(填字母)
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
根据表中数据,计算25.0℃时的分解平衡常数为 。
(2)25℃时,NH3·H2O电离常数Kb=1.8×10-5,Mg(OH)2的溶度积常数Ksp=1.8×10-11,计算0.5 mol/L氨水的pH约为 。(已知lg3≈0.5)在某氯化镁溶液中加入一定量的某浓度的氨水后,测得混合液PH=11,则此温度下残留在溶液中的c(Mg2+)= 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春外国语学校高二上学期期中化学试卷(解析版) 题型:选择题
你认为减少酸雨不可采用的措施是
A.煤脱硫再作燃料 B.开发新能源
C.把工厂烟囱升高 D.多用风能、氢能、核能等
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春外国语学校高一上学期期中化学试卷(解析版) 题型:选择题
下列分散系,不能产生丁达尔效应的是
A、稀豆浆 B、盐水 C、红墨水 D、Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春外国语学校高一上学期期中化学试卷(解析版) 题型:选择题
某气体的的质量为3.2g,含有的是3.01×1022个分子,则该气体的相对分子质量是
A、32 B、64 C、32 g /mol D、64 g /mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高二上学期期中考试化学试卷(解析版) 题型:选择题
现有可逆反应A(g)+2B(g)  nC(g) △H<0,在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图,其中结论正确的是
nC(g) △H<0,在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图,其中结论正确的是

A.p1>p2,n>3 B.p1<p2,n>3
C.p1<p2,n<3 D.p1>p2,n=3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高二上学期期中考试化学试卷(解析版) 题型:选择题
已知298K时,H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ?mol﹣1,推测含1mol HCl的稀溶液与含1mol NH3的稀溶液反应放出的热量
A.小于57.3 kJ B.等于57.3 kJ C.大于57.3kJ D.无法确定
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高二上学期模块一测试化学试卷(解析版) 题型:填空题
(共12分)
某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积KW= 。在此温度下,将 pH = a的 NaOH 溶液 Va L 与 pH = b的 H2SO4溶液 Vb L 混合。
(1)若所得混合液为中性,且 a= 12,b= 2,则 Va∶Vb= ;
(2)若所得混合液为中性,且 a+ b= 12,则 Va∶Vb= ;
(3)若所得混合液的 pH = 10,且 a= 12,b= 2,则 Va∶Vb= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com