
| ||
| ||


科目:高中化学 来源: 题型:
| A、Na+、Fe2+、Cl-、ClO- |
| B、Na+、Cu2+、SO42-、NO3- |
| C、Mg2+、NH4+、SO42-、Cl- |
| D、Ba2+、HCO3-、NO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
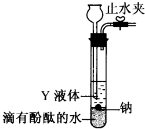
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
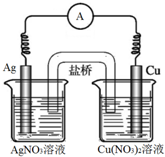 将反应Cu(s)+2Ag+(aq)?Cu2+(aq)+2Ag(s)设计成如下原电池,有关叙述正确的是( )
将反应Cu(s)+2Ag+(aq)?Cu2+(aq)+2Ag(s)设计成如下原电池,有关叙述正确的是( )| A、向硝酸银溶液中加入氯化钠固体,电流强度会减小 |
| B、向硝酸铜溶液中加入氢氧化钠固体,电流强度会减小 |
| C、将AgNO3溶液更换为Fe(NO3)3溶液,电流计指针偏转方向将相反 |
| D、当电流计指针为0时,该反应平衡常数K=0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
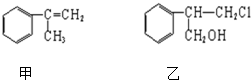
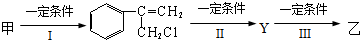
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金元素 |
| B、多环芳烃是强致癌物,能吸附在pm2.5的表面进入人体 |
| C、开发利用各种新能源,减少对化石燃料的依赖 |
| D、大力发展电动车,减少燃油汽车的尾气排放量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+22 kJ/mol |
| B、-66 kJ/mol |
| C、-11 kJ/mol |
| D、-33 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com