
| 84 |
| 12 |
| y |
| 4 |
| z |
| 2 |
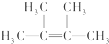 ;
;| 84 |
| 12 |
| y |
| 4 |
| z |
| 2 |
| 14 |
| 4 |
| 14 |
| 4 |
| 1 |
| 2 |
| 14 |
| 4 |
| 3 |
| 2 |
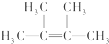 ,故答案为:
,故答案为: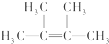 ;
; ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
| A、32He核聚变是化学变化 |
| B、32He和42He互为同位素 |
| C、32He原子核内含有3个中子 |
| D、32He原子核内含有3个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
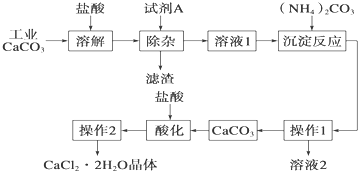
查看答案和解析>>
科目:高中化学 来源: 题型:
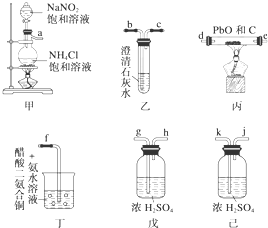 分析下列两则信息,然后回答有关问题:
分析下列两则信息,然后回答有关问题:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
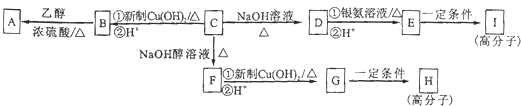
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | 该元素的一种核素无中子 |
| Y | 单质在氧气中燃烧产物是造成酸雨的罪魁祸首之一 |
| Z | 原子最外层有3个未成对电子,次外层只有一对成对电子 |
| L | 与Y同周期,比Y原子半径小 |
| M | +3价离子3d能级为半充满 |
查看答案和解析>>
科目:高中化学 来源: 题型:
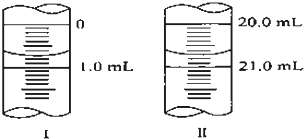 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
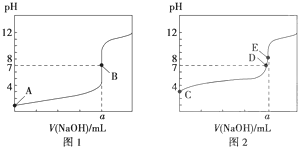
| A、滴定盐酸的曲线是图2 |
| B、达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl) |
| C、达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-) |
| D、当0mL<V(NaOH)<20.00mL时,对应混合液中各离子浓度大小顺序为c(A-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com