
【题目】下列说法错误的是
A. 铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
B. 钛及钛合金用于飞机、火箭、导弹、人造卫星和宇宙飞船等领域
C. 明矾可以用作净水剂除去悬浮于水中的泥沙
D. 单质硅是现代光学及光纤制品的基本原料
科目:高中化学 来源: 题型:
【题目】已知常温下,Ksp[Mg(OH)2]=1.8×10-11, Ksp[Fe(OH)3]=4.0×10-38。
(1)常温常压下,氢气的燃烧热为285.8 kJ·mol-1。则氢气燃烧的热化学方程式为__________
(2)用离子方程式表示重铬酸钾在溶液中存在的平衡:__________
(3)将浓度均为0.1 mol/L的硫酸铝溶液与小苏打溶液混合,反应的离子方程式为__________
(4)将浓度均为0.1 mol/L的硫代硫酸钠溶液与稀硫酸混合,反应的离子方程式为__________
(5)向Mg(OH) 2悬浊液中滴加2滴0.1 mol/L FeCl3溶液,反应的离子方程式为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料,在纺织、造纸、化工合成方面都有重要的用途。
(1)工业上电解饱和食盐水制取氯气:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,理论上每转移1mol电子,生成的氯气在标准状况下的体积为___L。工业上将生成的氯气通入石灰乳制取漂白粉,请写出该反应的化学方程式___________
2NaOH+H2↑+Cl2↑,理论上每转移1mol电子,生成的氯气在标准状况下的体积为___L。工业上将生成的氯气通入石灰乳制取漂白粉,请写出该反应的化学方程式___________
(2)实验室用常用MnO2与浓盐酸共热制氯气,试写出该反应的化学方程式_____________________,若用100mL12mol·L-1的浓盐酸与足量的MnO2反应,则生成的氯气在标准状况下的体积_____6.72L(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)获取铜和胆矾的操作流程如下:

已知:①部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
②B、C均为单一沉淀
请回答下列问题:
(1)已知Cu2O在酸性条件下发生自身氧化还原反应,写出离子反应方程式______________。
(2)为了加快反应I的速率,可以采取的措施是______________(写1点)。
(3)固体混合物A中的成分是__________________________。
(4)反应I完成后,铁元素的存在形式为_______________(填离子符号);写出生成该离子的离子方程式___________________________________。
(5)x对应的数值范围是_______________________。用NaClO调pH,生成沉淀B的反应的离子方程式为____________________________________。
(6)已知:Ksp[Al(OH)3]=1.1×10-33,当调节溶液的pH为5时,c(Al3+)=_________ molL-1
(7)洗涤CuSO4·5H2O粗产品不能用大量水洗,而用冰水洗涤.原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是
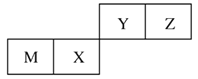
A. 原子半径Z<M
B. Y的最高价氧化物对应水化物的酸性比X的弱
C. X的最简单气态氢化物的热稳定性比Z的小
D. Z位于元素周期表中第2周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I 已知,CO 的毒性表现在 CO 与血红蛋白(Hb)结合成 Hb·CO,使血红蛋白失去输送 O2 功能。CO 进入血液后有如下平衡:CO+Hb·O2![]() O2+Hb·CO,已知在人体体温 37℃下,该平衡常数为 220。试回答:
O2+Hb·CO,已知在人体体温 37℃下,该平衡常数为 220。试回答:
(1)煤气中毒病人,可以通过进入高压氧舱的方法来救治,请用化学平衡的原理加以说明:
(2)抽烟时,进入肺部的空气中 c(CO)=10-6mol/L,c(O2 )=10-2mol/L,则 c(Hb·CO)为 c(Hb·O2)的 倍。
(3)已知当血液中c(Hb·CO)/c(Hb·O2)的比值大于 0.02 时,人的智力会很快受到损伤,为避免人的智力受到损伤,c(O2)与 c(CO)的比值应大于___________。
II 在某一温度条件下, Bodensteins 研究了反应:2HI(g) ![]() H2(g) +I2(g),气体混合物中 HI 的物质的量浓度 x(HI)与反应时间 t 的关系如下表:
H2(g) +I2(g),气体混合物中 HI 的物质的量浓度 x(HI)与反应时间 t 的关系如下表:

(4)根据上述实验结果,该反应的平衡常数K的计算式为_________。
(5)上述反应,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)×x(I2),其中k正、k逆为速率常数,则k逆为_________(以K和k正表示)。若k正=0.002·min-1,第一次实验时,当t=20min,v正=___________·min-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明的碱性溶液中,能大量共存的离子组是( )
A. Na+、H+、SO42﹣、HCO3﹣
B. Cu2+、K+、SO42﹣、NO3﹣
C. Na+、K+、Cl﹣、NO3﹣
D. Mg2+、K+、SO42﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中,溶液的pH大于7的是
A. 向NaCl溶液中滴加醋酸 B. 向KNO3溶液中滴加稀H2SO4
C. 向稀HCl溶液中滴加稀HNO3 D. 向NaOH溶液中滴加Na2CO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com