
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJmol﹣1表示。请认真观察下图,然后回答问题.
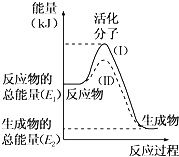
(1)图中所示反应是______(填“吸热”或“放热”)反应。
(2)已知拆开1mol H﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由1mol氢气和1mol碘反应生成HI会______(填“放出”或“吸收”)______ kJ的热量.在化学反应过程中,是将______ 转化为______。
(3)下列反应中,属于放热反应的是______,属于吸热反应的是______。
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳⑤Ba(OH)28H2O与NH4Cl反应 ⑥铁粉与稀盐酸反应
【答案】放热 放出 11 化学能 热能 ①②③⑥ ④⑤
【解析】
(1)生成物总能量低于反应物总能量为放热反应;
(2)断键吸热、成键放热;
(3)根据常见的吸热反应、放热反应回答;
(1)图中所示反应,生成物总能量低于反应物总能量,该反应为放热反应;
(2)1mol氢气和1mol碘反应生成2mol HI,断键吸收的热量为436kJ+151kJ=587 kJ,成键放出的热量是299kJ×2=598kJ,放出的热量大于吸收的热量,该反应放出598kJ -587 kJ =11kJ热量;
(3)①物质燃烧放热;②炸药爆炸放热;③酸碱中和反应放热;④二氧化碳通过炽热的碳吸热;⑤Ba(OH)28H2O与NH4Cl反应吸热;⑥铁粉与稀盐酸反应放热。所以属于放热反应的是①②③⑥,属于吸热反应的是④⑤。


科目:高中化学 来源: 题型:
【题目】某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。现进行如下图所示实验。下列有关说法正确的是

A. 步骤Ⅰ中减少的3 g固体一定是混合物
B. 步骤Ⅱ中质量减少的固体物质一定是Fe2O3
C. 根据上述步骤Ⅱ可以得出蓝色溶液中n(Cu2+)=0.02 mol
D. 根据步骤Ⅰ、Ⅱ可以判断X中氧化铁的质量分数为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了使Na2S溶液中![]() 的比值变小,可采取的措施是( )
的比值变小,可采取的措施是( )
①加适量盐酸
②加适量NaOH(s)
③加适量KOH(s)
④加适量KHS(s)
⑤加水
⑥通H2S(g)
⑦加热.
A.②③④ B.①②⑤⑥⑦ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用电解熔融氧化铝的方法制取金属铝。
(1)请写出反应的化学方程式_____________________________________________。
(2)现欲冶炼270吨铝,至少需要多少吨氧化铝?__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向20.00 mL 0.10 mol/L Na2CO3溶液中逐滴加入0.10 mol/L盐酸40.00 mL,所得溶液的pH与加入盐酸体积的关系如表所示:
溶液的pH | 加入盐酸的总体积 |
12 | V(HCl)=0 |
8 | V(HCl)=20.00 mL |
5 | V(HCl)=40.00 mL |
回答下列问题:
(1)20.00 mL 0.10 mol/L Na2CO3溶液中所有阳离子和阴离子的浓度有何关系?______ (用等式表示)。
(2)当V(HCl)=20.00 mL时,溶液呈碱性的原因是________(用离子方程式和必要的文字说明)此时溶液中c(H2CO3)____(填“>”、“<”或“=”)c(CO32—)。
(3)V(HCl)=40.00 mL时,得到H2CO3饱和溶液,且c(H2CO3)=4.0×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3—+H+的电离常数K1=_____。此时保持其他条件不变,继续加入0.1 mol/L盐酸10.00 mL,K1将_____(填“变大”、“变小”或“不变”)。
HCO3—+H+的电离常数K1=_____。此时保持其他条件不变,继续加入0.1 mol/L盐酸10.00 mL,K1将_____(填“变大”、“变小”或“不变”)。
(4)若向20 mL 0.10 mol/L Na2CO3溶液中加入BaCl2粉末3.94×10-7 g时开始产生沉淀BaCO3,则Ksp(Ba2CO3)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。如图为RFC工作原理示意图,下列有关说法正确的是
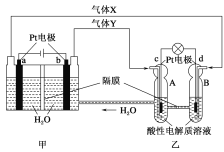
A. 图甲把化学能转化为电能,图乙把电能转化为化学能,水得到了循环使用
B. 当有0.1 mol电子转移时,a极产生0.56 L O2(标准状况下)
C. c极上发生的电极反应为O2+4H++4e-===2H2O
D. 图乙中电子从c极流向d极,提供电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. 氯气通入冷的氢氧化钠溶液中:Cl2 + 2OH = Cl + ClO + H2O
B. Fe与少量稀硝酸的反应:Fe + 4H+ + NO3 = Fe3+ + NO↑+ 2H2O
C. 碳酸钡溶于醋酸:BaCO3 + 2H+ = Ba2+ + H2O + CO2↑
D. 用石墨电极电解MgCl2 溶液:2Cl + 2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
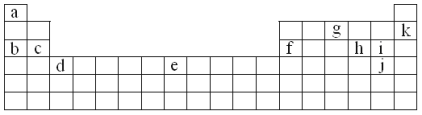
在上表中用字母代号回答下列问题:
(1)属于碱金属元素的有______________________;
(2)写出下列元素在周期表中的位置:c_______________;e_______________;
(3)X、Y、Z、T、V为5种短周期元素,X、Y、Z在周期表中位置如图所示。这3种元素原子序数之和是41,X和T在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄色固体)两种化合物。V单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使紫色石蕊溶液变红,则:
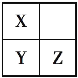
①5种元素的元素符号分别是X___________,Y________,Z________,T_______, V____。
②Y的原子结构示意图是____________________________________。
③T、X形成化合物T2X2的化学方程式为______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com