
【题目】下列有关烃说法叙述正确的是( )
A. 通式为CnH2n+2的烃一定是烷烃
B. 通式为CnH2n的烃一定是烯烃
C. 通式为C4H6的烃一定是炔烃
D. 相对分子质量为128的烃一定是烷烃
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】原电池与电解池在生活和生产中有着广泛应用。下列有关判断中错误的是( )
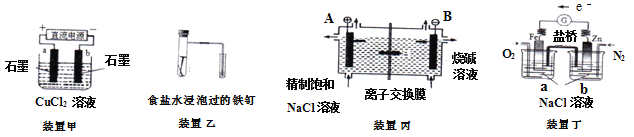
A. 装置甲研究的是电解CuCl2溶液,它将电能转化为化学能
B. 装置乙研究的是金属的吸氧腐蚀,Fe上的反应为Fe - 2e -- = Fe2+
C. 装置丙研究的是电解饱和食盐水,B电极发生的反应:2Cl- -2e-- = Cl2↑
D. 向装置丁烧杯a中加入少量K3[Fe(CN)6]溶液,没有蓝色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
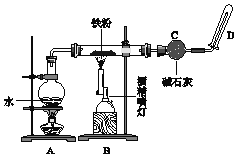
【题目】(1) 如下图实验装置,当有16.8g铁粉参加反应时,生成的气体在标准状况下的体积是__L。
(2) 向Cu和CuO组成的混合物中,加入100mL 6.0mol·L1稀硝酸溶液,恰好使混合物完全溶解,同时收集到标准状况下NO 2.24 L。请回答以下问题:
①原混合物中Cu和CuO的物质的量之比为______;
②假设反应后溶液的体积保持不变,所得溶液溶质的物质的量浓度为______mol·L1;
③若将生成的NO气体完全溶解,需要标准状况下的氧气的物质的量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下在一容积恒为2L的容器内发生反应:2A(g)+B(g)![]() 2C(g),已知起始投入4mol A(g) 和2mol B(g),经2s后测得C的浓度为0.6mol/L,并且2s后各组分浓度不再改变.下列说法正确的是( )
2C(g),已知起始投入4mol A(g) 和2mol B(g),经2s后测得C的浓度为0.6mol/L,并且2s后各组分浓度不再改变.下列说法正确的是( )
A. 2s内用物质A表示的平均反应速率为0.6mol/(Ls)
B. 2s内用物质B表示的平均反应速率为0.6mol/(Ls)
C. 2s后每有0.6mol的物质B生成,同时就有0.6mol物质C生成
D. 2s时物质B的浓度为0.7mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用工业冶炼硫酸铜(含有Fe2+、AsO2-、Ca2+等杂质)提纯制备电镀硫酸铜的生产流程如下:

已知:①Fe3+、Cu2+开始沉淀的pH分别2.7、5.4,完全沉淀的pH分别为3.7、6.4。
②Ksp[Cu(OH)2]=2×10-20
③AsO2-+H2O2+H+=H3AsO4, H3AsO4+Fe3+=FeAsO4↓+3H+
(1)溶解操作中需要配制含铜32 g·L-1的硫酸铜溶液1.0 L,需要称量冶炼级硫酸铜的质量至少为___________g。
(2)测定溶解液中的Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4溶液应使用
________(“酸式”或“碱式”)滴定管,其中反应离子方程式为:______________________。若要检验调节pH后溶液中的Fe3+已除尽的方法是___________________________。
(3)氧化后需要将溶液进行稀释及调节溶液的pH=5,则稀释后的溶液中铜离子浓度最大不能超过____________mol·L-1。
(4)固体Ⅰ的主要成分除 FeAsO4 、Fe(OH)3外还有__________________,由溶液Ⅰ获得CuSO4·H2O,需要经过________ 、____________、过滤、洗涤、干燥操作。
(5)利用以上电镀级硫酸铜作为电解质溶液,电解粗铜(含锌、银、铂杂质)制备纯铜,写出阳极发生的电极反应式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。为辨别真伪,可用下列哪一种试剂来鉴别( )
A.酚酞试液B.氯化钡溶液C.氢氧化钠溶液D.硝酸银溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于化学反应方向的确定不仅与焓变(ΔH)有关,也与温度(T)、熵变(ΔS)有关,实验证明,化学反应的方向应由ΔH-TΔS确定,若ΔH-TΔS<0,则自发进行,否则不能自发进行。下列说法中,正确的是( )
A.在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向
B.温度、压强一定时,熵增加的反应一定能自发进行
C.反应焓变是决定反应能否自发进行的唯一因素
D.固体的溶解过程只与焓变有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W、M、N 的原子序数依次增大,且原子最外层电子数之和为23。X 的原子半径比Y 的小,X 与W 同主族,Z 的最外层电子数是电子层数的3倍,M 是地壳中含量最高的金属元素。
(1)M的离子结构示意图____________;X、Y形成的含18电子的化合物的电子式____________;
用电子式表示由W、Z形成的只含离子键的化合物的形成过程______________________;
(2)Y、Z、M原子半径由大到小的顺序____________(用元素符号表示),Z的氢化物稳定性_____N的氢化物稳定性(填“>” “<”或 “=”)
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是_________(填化学式),此化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨气,相应的离子方程式为:___________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com