
����Ŀ����̬��X�ڱ�״���µ��ܶ�Ϊ1.16 g��L��1��D�ܷ���������Ӧ��EΪ������ϩ���й����ʵ�ת����ϵ����ͼ����ش�����������

(1)��Ӧ���ķ�Ӧ����Ϊ________��һ��������X�ܷ������������ķ�Ӧ�����ø߷��ӻ�����Ľṹ��ʽΪ
_________________��
(2)A��F�ڴ���������ֱ������G�Ļ�ѧ����ʽΪ
_______________________________________________________________________________��
(3)����˵����ȷ����________��
A��A��B��E����ʹ���Ը��������Һ��ɫ
B��G��ͬ���칹��������̼�����Ʒ�Ӧ����CO2�����������4��
C��F��G������NaOH��Һ��Ӧ���Ҷ���������
D��X�Ⱥ���F��H2��ӦҲ�����Ƶ�G
���𰸡� �ӳɷ�Ӧ ![]() CH2===CH2��CH3COOH
CH2===CH2��CH3COOH![]() CH3COOCH2CH3 CD
CH3COOCH2CH3 CD
����������X�ڱ�״���µ��ܶ�Ϊ1.16 g��L��1����X��Ħ������Ϊ��1.16 g��L��1��22.4 L��mol��1=26 g��mol��1������XΪCH![]() CH��AΪCH2=CH2��CΪCH3CH2OH����ΪEΪ������ϩ������BΪCH2=CHCl����ΪD�ܷ���������Ӧ������DΪCH3CHO��FΪCH3COOH��
CH��AΪCH2=CH2��CΪCH3CH2OH����ΪEΪ������ϩ������BΪCH2=CHCl����ΪD�ܷ���������Ӧ������DΪCH3CHO��FΪCH3COOH��
��1����ϩ��HCl��������ϩ���ڼӳɷ�Ӧ��CH![]() CH�����Ӿ۷�Ӧ����
CH�����Ӿ۷�Ӧ����![]() ����2������ԭ���غ���ϩ��������������·����ӳɷ�Ӧ����������������ѧ����ʽΪCH2=CH2��CH3COOH
����2������ԭ���غ���ϩ��������������·����ӳɷ�Ӧ����������������ѧ����ʽΪCH2=CH2��CH3COOH![]() CH3COOCH2CH3����3��AΪCH2=CH2��BΪCH2=CHCl������̼̼˫������ʹ���Ը��������Һ��ɫ��EΪ������ϩ������̼̼˫��������ʹ���Ը��������Һ��ɫ����A����CH3COOCH2CH3��ͬ���칹��������̼�����Ʒ�Ӧ����CO2���������Ӧ�����Ȼ�����CH3CH2CH2COOH��(CH3)2CHCOOH��2�֣���B����CH3COOH��CH3COOCH2CH3������NaOH��Һ��Ӧ���Ҷ�����CH3COONa����C��ȷ������ԭ���غ㣬CH
CH3COOCH2CH3����3��AΪCH2=CH2��BΪCH2=CHCl������̼̼˫������ʹ���Ը��������Һ��ɫ��EΪ������ϩ������̼̼˫��������ʹ���Ը��������Һ��ɫ����A����CH3COOCH2CH3��ͬ���칹��������̼�����Ʒ�Ӧ����CO2���������Ӧ�����Ȼ�����CH3CH2CH2COOH��(CH3)2CHCOOH��2�֣���B����CH3COOH��CH3COOCH2CH3������NaOH��Һ��Ӧ���Ҷ�����CH3COONa����C��ȷ������ԭ���غ㣬CH![]() CH�Ⱥ���CH3COOH��H2��ӦҲ�����Ƶ�CH3COOCH2CH3����D��ȷ�����ϣ�ѡCD��
CH�Ⱥ���CH3COOH��H2��ӦҲ�����Ƶ�CH3COOCH2CH3����D��ȷ�����ϣ�ѡCD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.pH=6��NaHSO3��Һ�У�c(SO32-)-c(H2SO3)=9.9��10-6molL-1
B.Ũ�Ⱦ�Ϊ0.1 molL-1��CuSO4��(NH4)2SO4�Ļ����Һ�У�c(NH4+)>c(SO42-)>c(Cu2+)>c(H+)
C.0.1 molL-1NaF��Һ�м���NH4Cl�����ԣ�c(HF)=c(NH3H2O)
D.0.100 molL-1��Na2S��Һ��ͨ��HCl���壬��c(Cl-)=0.100 molL-1(������Һ����ı仯��H2S�Ļӷ�)��c(OH-)-c(H+)=c(HS-)-c(S2-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�����������ͽ��۾���ȷ����

ѡ�� | ���� | ���� | ���� |
A | ����ʪ��ĺ�ɫʯ����ֽ�����Թܿ� | ��ֽ����ɫ | NH4Cl���Ȳ��ֽ� |
B | �������� | �²�Һ����ɫ��dz | NaOH��Һ�ɳ�ȥ�����屽�е�Br2 |
C | ������ | ϴ��ƿ����Һ��ɫ | ��������ϩ |
D | ��ͨ�� | B�����к�ɫ�������� | п�Ľ����Ա�ͭǿ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ����������ȼ�ϵ�صĹ���ԭ����ͼ���õ�ط�ӦΪ��Mg+ClO��+H2O�TMg��OH��2+Cl�������й�˵����ȷ���ǣ�������

A. ��ع���ʱ��C��Һ�е�������MgCl2
B. ��ع���ʱ������a������pH����������
C. ������Ӧʽ��ClO����2e��+H2O�TCl��+2 OH��
D. b�缫������ԭ��Ӧ��ÿת��0.1mol���ӣ�����������0.1mol Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Na+Ũ��Ϊ1.0mol/L��ij������Һ�У������ܺ���K+��Mg2+��Fe3+��Ba2+��Cl-��CO32-��SO32-��SiO32-��SO42-�����ӣ�ȡ����Һ100ml������ͼ����ʵ��(�����Լ�������������ȫ���ݳ�)������˵������ȷ����
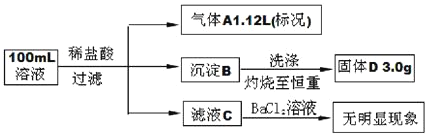
A.ԭ��Һ��һ��������Mg2+��Fe3+��Ba2+��SO42-
B.��100mlԭ��Һ�м�������BaCl2��Һ�����ٿ����ɳ���20.5g
C.Ϊȷ��ԭ��Һ���Ƿ���Cl-����ȡ��ҺC������AgNO3��ϡHNO3��Һ
D.ԭ��Һһ������K+��c(K+)����Ϊ1.5mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A�ķ�����Ϊ92������̼ԭ�Ӷ���ͬһƽ���ϡ�һ������A�Ʊ�ˮ����Ĺ������¡�
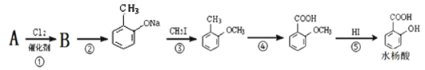
(1)��д����B����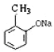 �ķ�Ӧ����ʽ��_________________________________��
�ķ�Ӧ����ʽ��_________________________________��
(2)�ںϳ���·�У���Ƶڢۺ͵ڢ���������Ӧ��Ŀ���ǡ�_____________________��
(3)����ˮ������ص�ת����ϵ���¡�
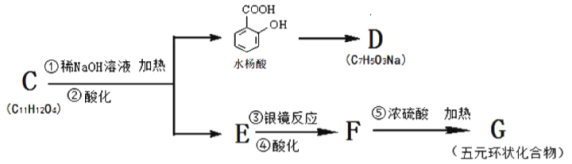
����һ����ѧ��Ӧ֤��ˮ�����������������Բ����____________________��
(4)�ٷ�Ӧ����Ϊ��_________��___________��
(5) G�Ľṹ��ʽΪ��___________�� ���������ơ�_____________��
(6)��д��ͬʱ��������Ҫ���ˮ���������ͬ���칹��Ľṹ��ʽ______________��
�ٵ���FeCl3��Һ��������ɫ��Ӧ��
���ܷ���������Ӧ��
�۱�����һ�ȴ��������֡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0��10mol��L��1NaOH��Һ�ֱ�ζ�20��00mLŨ�Ⱦ�Ϊ0��10 mol��L��1CH3COOH
��Һ��HCN��Һ���õζ���������ͼ������˵����ȷ����

A. �����͵�����ʾ��Һ�У�c��CH3COO������c��CN����
B. �����͵�����ʾ��Һ�У�c��Na������c��OH������c��CH3COO������c��H����
C. �����͵�����ʾ��Һ�У�c��CH3COO������c��CN������c��HCN����c��CH3COOH��
D. �����͵�����ʾ��Һ�ж��У�c��CH3COO������c��OH������c��CH3COOH����c��H����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳ��ݣ�Gelsemium��Ϊ�й��Ŵ��Ŵ�ҩ֮һ���ݼ���������Ѫ��������ִ��������Ǻ����ٿ�ֲ������٣����еĶ��غܶ࣬�����Ƿ�����������ֶ��صĽṹ��ʽ�������ƶ���ȷ���ǣ�������
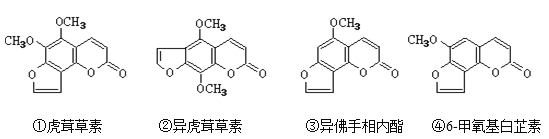
A.������������������Ȣ��ж�
B.�١��ܻ�Ϊͬϵ��
C.�١��ڡ��ۡ��ܾ���������������Һ��Ӧ
D.�����ʵ����ڡ��۷ֱ���������������ȫȼ�գ�ǰ�����������Ⱥ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ Ksp(AgCl)=1.0��10-12��Ksp(AgI)=1.0��10-16������˵����ȷ����
A.��AgCl������Һ�м�������ˮ��c(Ag+)�ȼ�С������
B.��0.01mol/L��AgNO3��Һ�У�����������Ũ�Ⱦ�Ϊ0.001mol/L��Cl-��I-�Ļ����Һ��ֻ����AgI����
C.�����£�AgCl������Ҫ��NaI��Һ�п�ʼת��ΪAgI��������NaI��Ũ�ȱ��벻����1.0��10-10mol/L
D.��10ml0.1mol/L AgNO3��Һ�еμ�1ml0.1mol/L��NaCl��Һ���а�ɫ�������ɣ��ٵμ�0.1mol/L��KI��Һ���л�ɫ�������ɣ�˵��Ksp(AgCl)> Ksp(AgI)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com