���㣺���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ��
ר�⣺
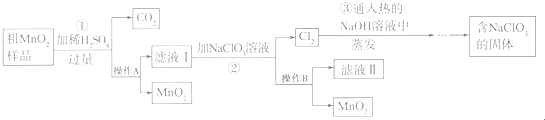
��������MnO
2�����н϶��MnO��MnCO
3����Ʒ�м��������ϡ���ᣬ����MnO
2���������ᣬ����Ʒ�е�MnO��MnCO
3�ֱ�����ᷴӦ���ɿ����Ե�MnSO
4�����˵���Һ��Ϊ��������Һ������NaClO
3������ӦΪ��5Mn
2++2ClO
3-+4H
2O=5MnO
2+Cl
2��+8H
+���ٹ��˵õ���Һ��Ͷ������̹��壬���������ȵ��������Ʒ�Ӧ���������Ʒ���ʽΪ��3Cl
2+6NaOH=NaClO
3+NaCl+3H
2O��
��1�����ݼ���ϴ��MnO
2�ķ�Һ���Ƿ�������жϣ�
��2�����ݵ�ʧ�����غ�������غ��д�����ӷ���ʽ��
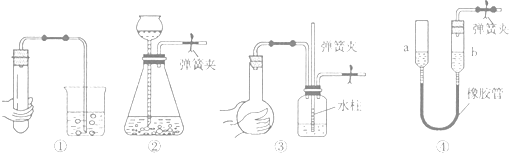
��3���������������������̨������Ȧ�����ƾ��ơ�������������
��4���������������ɵģ�����֮ǰ�ֻ��õ�������һ�������ѭ��ʹ����������
��5��MnO
2��������ʵ���ҷֽ��������������
��6�����������غ�ͻ�ѧ����ʽ���㣬CO
2�����ʵ���Ϊ
=0.03mol����MnCO
3�����ʵ���Ϊ0.03mol������Ϊ115g/mol��0.03mol=3.45g������MnO������Ϊ24.28g-18.35g-3.45g=2.48g��
���
�⣺��MnO
2�����н϶��MnO��MnCO
3����Ʒ�м��������ϡ���ᣬ����MnO
2���������ᣬ����Ʒ�е�MnO��MnCO
3�ֱ�����ᷴӦ���ɿ����Ե�MnSO
4�����˵���Һ��Ϊ��������Һ������NaClO
3������ӦΪ��5Mn
2++2ClO
3-+4H
2O=5MnO
2+Cl
2��+8H
+���ٹ��˵õ���Һ��Ͷ������̹��壬���������ȵ��������Ʒ�Ӧ���������Ʒ���ʽΪ��3Cl
2+6NaOH=NaClO
3+NaCl+3H
2O��
��1��������ˢ����õ�MnO
2�Ƿ�ϴ�Ӹɾ��ķ�����ȡ���һ��ϴ��Һ���Թ��У��μ��Ȼ�����Һ��������������֣�˵����ϴ�Ӹɾ����ʴ�Ϊ��ȡ���һ��ϴ��Һ���Թ��У��μ��Ȼ�����Һ��������������֣�˵����ϴ�Ӹɾ���
��2��MnSO
4Ҫת��ΪMnO
2����ʧȥ���ӣ�����Ҫ����NaClO
3�������������ݵ�ʧ�����غ������ƽ�����Է�Ӧ�Ļ�ѧ����ʽ�ǣ�5MnSO
4+2NaClO
3+4H
2O=5MnO
2+Cl
2��+Na
2SO
4+4H
2SO
4����˷�Ӧ�����ӷ���ʽ�ǣ�5Mn
2++2ClO
3-+4H
2O=5MnO
2+Cl
2��+8H
+���ʴ�Ϊ��5Mn
2++2ClO
3-+4H
2O=5MnO
2+Cl
2��+8H
+��
��3���ڢ������������������������������̨������Ȧ�����ƾ��ơ��������������ʴ�Ϊ���ƾ��ơ�������
��4�����������������������ƹ����ڵڢڲ��պ�Ҳ�õ���������Һ�����Կ�����ѭ��ʹ�õ�������NaClO
3���ʴ�Ϊ��NaClO
3��
��5��MnO
2��������ʵ���ҷֽ�������������ķ���ʽΪ��2KClO
32KCl+3O
2�����ʴ�Ϊ��2KClO
32KCl+3O
2����
��6�����������غ�ͻ�ѧ����ʽ���㣬CO
2�����ʵ���Ϊ
=0.03mol����MnCO
3�����ʵ���Ϊ0.03mol������Ϊ115g/mol��0.03mol=3.45g������MnO������Ϊ24.28g-18.35g-3.45g=2.48g���ʴ�Ϊ��2.48��
����������ͨ��MnO2���ᴿ�ۺϿ����˳����Ļ���ʵ�������������ԭ����ʽ����д��������жϼ��йؼ��㣬Ϊ��Ƶ���㣬���������з����Ļ�ѧ��Ӧ���������뷽��Ϊ���Ĺؼ������ط����������ƶ������Ŀ��飬��Ŀ�ѶȲ���