
【题目】大量的__________和__________扩散到大气中,被雨水吸收,当雨水的pH小于________时就形成了酸雨。根据形成酸雨的主要物质可将其分为硫酸型酸雨和硝酸型酸雨。 我国酸雨危害十分严重,是世界三大酸雨区之一,且主要为硫酸型酸雨。形成硫酸型酸雨主要是由于空气中二氧化硫含量超标。形成硫酸型酸雨发生的主要反应的化学方程式为
途径一:___________________________________、___________________________________;
途径二:___________________________________、___________________________________。
某校科技活动小组的同学们采集酸雨样品,每隔一段时间测定样品的pH,得到下列数据:
时间 | 开始 | 8h后 | 16h后 | 24h后 | 32h后 | 40h后 | 48h后 |
pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
根据上述材料回答下列问题:
酸雨放置时,pH发生变化的主要原因为_____________。
下列物品中,最易被酸雨腐蚀的是____________
A 铜制塑像 B 大理石雕刻 C 水泥路面 D 铝制窗框
【答案】SO2 氮的氧化物 5.6 SO2+H2OH2SO3 2H2SO3+O2=2H2SO4 ![]() SO3+H2O=H2SO4 酸雨样品中的H2SO3逐渐被氧化成H2SO4,使溶液的酸性增强; B
SO3+H2O=H2SO4 酸雨样品中的H2SO3逐渐被氧化成H2SO4,使溶液的酸性增强; B
【解析】
pH<5.6的雨水为酸雨,SO2和氮的氧化物在大气中,在空气、阳光等作用下发生一系列变化,遇雨时被雨水吸收形成酸雨。故答案为:SO2;氮的氧化物;5.6;
途径一:二氧化硫与雨水反应生成亚硫酸,亚硫酸被空气中的氧气氧化成硫酸,故答案为:SO2+H2OH2SO3;2H2SO3+O2=2H2SO4 ;
途径二:空气中的二氧化硫气体在粉尘做催化剂的条件下生成三氧化硫,三氧化硫再与雨水形成酸雨,故答案为:![]() ;SO3+H2O=H2SO4;
;SO3+H2O=H2SO4;
酸雨形成的主要原因是:大量燃烧化石燃料(煤和石油等),产生二氧化硫,随雨降落形成,酸雨样品中的H2SO3逐渐被氧化成H2SO4,使溶液的酸性增强,故答案为:酸雨样品中的H2SO3逐渐被氧化成H2SO4,使溶液的酸性增强;
A.铜的活泼性较差不和稀硫酸反应;B大理石雕刻主要成分是碳酸钙,易与稀硫酸反应;C 水泥路面属于硅酸盐产品,能被酸雨腐蚀,但不如大理石易被腐蚀;D铝制窗框含有的金属铝能与酸反应,但铝表面的氧化膜有保护作用;故答案为B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)![]() 2SO3(g)+Q(Q>0)。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,分析正确的是
2SO3(g)+Q(Q>0)。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,分析正确的是

A. 图Ⅰ研究的是t1时刻增大O2的浓度对反应速率的影响
B. 图Ⅱ研究的是t1时刻加入催化剂后对反应速率的影响
C. 图Ⅲ研究的是催化剂对平衡的影响,且甲的催化速率比乙高
D. 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25 ℃、101 kPa时,16 g CH4完全燃烧生成液态水时放出的热量是890.31 kJ,则CH4燃烧的热化学方程式是 。
(2)已知:C(s)+ O2(g)![]() CO2(g) ΔH=-437.3 kJmol-1
CO2(g) ΔH=-437.3 kJmol-1
H2(g)+ ![]() O2(g)
O2(g)![]() H2O(g) ΔH=-285.8 kJmol-1
H2O(g) ΔH=-285.8 kJmol-1
CO(g)+ ![]() O2(g)
O2(g)![]() CO2(g) ΔH=-283.0 kJmol-1
CO2(g) ΔH=-283.0 kJmol-1
则煤的气化主要反应的热化学方程式是
C(s)+ H2O(g)![]() CO(g)+ H2(g) ΔH= kJmol-1。
CO(g)+ H2(g) ΔH= kJmol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】交联聚合物P的结构片段如图所示。下列说法不正确的是(图中![]() 表示链延长)
表示链延长)

A. 聚合物P中有酯基,能水解
B. 聚合物P的合成反应为缩聚反应
C. 聚合物P的原料之一丙三醇可由油脂水解获得
D. 邻苯二甲酸和乙二醇在聚合过程中也可形成类似聚合物P的交联结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物m、n、P存在如下转化关系。下列说法正确的是

A. m、n不存在同分异构体,p存在多种同分异构体
B. m、n、p均能使酸性高锰酸钾溶液褪色
C. m、n、p中所有原子可能共面
D. 等质量的m、n、p,完全燃烧耗氧量不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请阅读下列材料,完成下面小题。
汽车彻底改变了我们生活,成为我们的不可或缺的交通工具之一。汽车尾气系统中的催化转化器,可有效降低尾气中的CO、NO和NO2等向大气的排放,在催化转化器的前半部发生的反应为2CO(g)+2NO(g)![]() 2CO2(g)+N2(g)。
2CO2(g)+N2(g)。
【1】上述催化器中发生的反应属于
A.复分解反应B.分解反应C.置换反应D.不属于四种基本反应
【2】关于反应2CO(g)+2NO(g)![]() 2CO2(g)+N2(g)中,下列说法正确的是
2CO2(g)+N2(g)中,下列说法正确的是
A.CO作氧化剂B.CO发生氧化反应
C.NO被氧化D.NO作还原剂
【3】已知汽车尾气处理反应能量过程如下图,下列说法正确的是

A.该反应为放热反应
B.该反应为吸热反应
C.形成N≡N化学键需要吸收热量
D.反应物的总能量小于生成物的总能量
【4】下列反应条件的改变对该反应速率的影响正确的是
A.升高温度能减慢反应速率
B.增大反应物浓度能减缓反应速率
C.达到平衡时,CO能100%转化为CO2
D.使用催化剂能加快该反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林(结构如图)是一种历史悠久的解热镇痛药,诞生于1899年3月6日。用于治感冒、发热、头痛、牙痛、关节痛、风湿病,还能抑制血小板聚集,用于预防和治疗缺血性心脏病、心绞痛、心肺梗塞、脑血栓形成,应用于血管形成术及旁路移植术也有效。

(1)阿司匹林水溶液呈_____(填“酸性”、“碱性”、“中性”)。
(2)阿司匹林分子中虚线框内官能团的名称______(填名称)。
(3)阿司匹林必须密闭干燥存储,以防止在酸性条件下与水发生_______ 生成乙酸和水杨酸( ![]() )
)
A.水解反应 B.加成反应 C.酯化反应
(4)向阿司匹林水溶液中滴加饱和NaHCO3溶液,实验现象为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,以钛铁矿(主要含FeTiO3,还含有Fe2O3 和Al2O3、SiO2等杂质)为原料制备二氧化钛并得到副产品绿矾(FeSO4·7H2O)的工艺流程如下图所示。
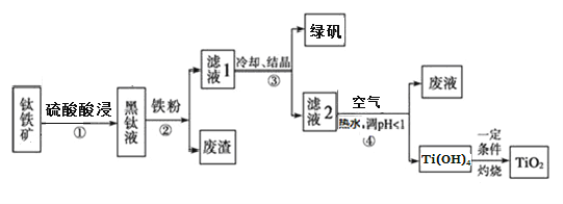
已知:TiO2+在一定条件下会发生水解。
回答下列问题:
(1)要提高酸浸时钛矿石的溶解速率,可行的措施是(写一条即可)_______________。黑钛液中生成的主要阳离子有TiO2+和Fe2+,步骤①主要反应的化学方程式是_________。
(2)步骤②中,加入铁粉的主要作用是_____,同时也会将部分TiO2+还原为Ti3+。
(3)向滤液2中通入空气的目的是______(用离子方程式表示)。
(4)请结合化学用语用化学平衡理论解释步骤④中加入热水稀释将TiO2+转化为Ti(OH)4 的原因:_________________。
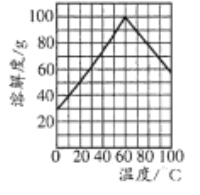
(5)副产品绿矾中含有杂质[Al2(SO4)3]。要将副产品进一步提纯,请结合右图的绿矾溶解度曲线完成提纯过程:将副产品溶于稀硫酸中,充分搅拌后,用NaOH溶液调节反应液的pH约为5,过滤沉淀后得到FeSO4溶液,______,过滤,用冰水洗涤,低温干燥,得到FeSO4·7H20晶体。
(6)用氧化还原滴定法测定制备得到的产品中TiO2的质量分数:在一定条件下,将一定量的产品溶解并将TiO2还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵[NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①滴定终点的现象是_______________。
②滴定分析时,称取TiO2试样0.2 g,消耗0.1 mol/L NH4Fe(SO4)2标准溶液24.00mL,则TiO2的质量分数为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,对CO、NOx的综合利用是科学家研究的热点。回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g) H1=+180.5kJ·mol-1
2CO(g)+O2(g)=2CO2(g) H2=-566kJ·mol-1
2NO(g)+O2(g)=2NO2(g) H3=-116.2kJ·mol-1
写出CO和NO2反应生成N2的热化学方程式:____。
(2)制备AlCl3的实际生产过程中,常加入足量的碳粉,反应后生成CO(g)。T℃时,向恒容密闭容器中加入3mol Al2O3(s)、8mol C(s)和3.3mol Cl2(g),发生反应。Cl2的浓度变化如图1所示;图2为20min后改变容器中条件,平衡体系的反应速率(v)随时间(t)的变化关系,且四个阶段都各改变一种不同的条件。
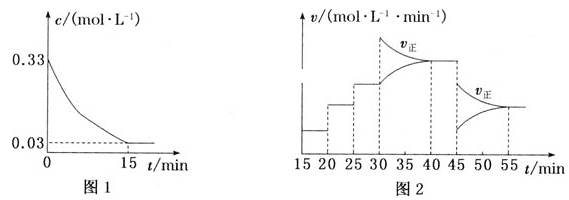
①容器中发生反应的化学方程式为___。
②0~15min内,该反应的平均速率v(CO)=___mol·L-1·min-1。
③T℃时,该反应的平衡常数K=___。
④15min时的平衡常数K(15)、44 min时的平衡常数K(44)与55min时的平衡常数K(55)的大小关系为____。
(3)N2O5在一定条件下可发生分解:2N2O5(g)![]() 4NO2(g)+O2(g)。一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是___(填标号)。
4NO2(g)+O2(g)。一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是___(填标号)。
A.容器中气体的密度不发生变化
B.NO2和O2的体积比保持不变
C.v正(NO2)=2v逆(N2O5)
D.气体的平均相对分子质量为43.2,且保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com