
【题目】某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。已知:
物质 | BaSO4 | BaCO3 | AgI | AgCl | |
溶解度/g(20℃) | 2.4×10-4 | 1.4×10-3 | 3.0×10-7 | 1.5×10-4 |
(1)探究BaCO3和BaSO4之间的转化
实验操作:
试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
实验Ⅰ | BaCl2 | Na2CO3 | Na2SO4 | …… |
实验Ⅱ | Na2SO4 | Na2CO3 | 有少量气泡产生,沉淀部分溶解 |
① 实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入盐酸后,______。
② 实验Ⅱ中加入稀盐酸后发生反应的离子方程式是______。
③ 实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:______。
(2)探究AgCl和AgI之间的转化
实验Ⅲ:
实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
装置 | 步骤 | 电压表读数 | |
| ⅰ.如图连接装置并加入试剂,闭合K | a | |
ⅱ.向B中滴入AgNO3(aq),至沉淀完全 | b | ||
ⅲ.再向B中投入一定量NaCl (s) | c | ||
ⅳ.重复ⅰ,再向B中加入与ⅲ等量NaCl(s) | a |
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
① 实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是______(填序号)。
a. AgNO3溶液 b. NaCl溶液 c. KI溶液
② 实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是______。
③ 结合信息,解释实验Ⅳ中b<a的原因:______。
④ 实验Ⅳ的现象能说明AgI转化为AgCl,理由是______。
(3)综合实验Ⅰ~Ⅳ,可得出结论: ______。
【答案】沉淀不溶解或无明显现象 BaCO3 + 2H+ === Ba2+ + CO2↑+ H2O BaSO4在溶液中存在BaSO4(s) ![]() Ba2+(aq) + SO42-(aq),当加入浓度较高的Na2CO3溶液,CO32-与Ba2+结合生成BaCO3沉淀,使上述平衡向右移动 b 2I- - 2e- === I2 由于生成AgI沉淀使B的溶液中c(I-)减小,I-还原性减弱 实验ⅳ表明Cl-本身对该原电池电压无影响,则c>b说明加入Cl-使c(I-)增大,证明发生了AgI + Cl-
Ba2+(aq) + SO42-(aq),当加入浓度较高的Na2CO3溶液,CO32-与Ba2+结合生成BaCO3沉淀,使上述平衡向右移动 b 2I- - 2e- === I2 由于生成AgI沉淀使B的溶液中c(I-)减小,I-还原性减弱 实验ⅳ表明Cl-本身对该原电池电压无影响,则c>b说明加入Cl-使c(I-)增大,证明发生了AgI + Cl- ![]() AgCl + I- 溶解度小的沉淀容易转化成溶解度更小的沉淀,反之则不易;溶解度差别越大,由溶解度小的沉淀转化为溶解度较大的沉淀越难实现
AgCl + I- 溶解度小的沉淀容易转化成溶解度更小的沉淀,反之则不易;溶解度差别越大,由溶解度小的沉淀转化为溶解度较大的沉淀越难实现
【解析】
①因为BaCO3能溶于盐酸,放出CO2气体,BaSO4不溶于盐酸,所以实验Ⅰ说明全部转化为BaSO4,依据的现象是加入盐酸后,沉淀不溶解或无明显现象。答案:沉淀不溶解或无明显现象。
② 实验Ⅱ是BaCl2中加入Na2SO4和Na2CO3产生BaSO4和BaCO3,再加入稀盐酸有少量气泡产生,沉淀部分溶解,是BaCO3和盐酸发生反应产生此现象,所以反应的离子方程式为:BaCO3 + 2H+ = Ba2+ + CO2↑+ H2O。答案:BaCO3 + 2H+ = Ba2+ + CO2↑+ H2O。
③ 由实验Ⅱ知A溶液为3滴0.1mol/LBaCl2,B为2mL0.1mol/L的Na2SO4溶液,根据Ba2++ SO42-= BaSO4![]() ,所以溶液中存在着BaSO4 (s)
,所以溶液中存在着BaSO4 (s) ![]() Ba2+(aq)+ SO42-(aq),当加入浓度较高的Na2CO3溶液,CO32-与Ba2+结合生成BaCO3沉淀,使上述平衡向右移动。所以BaSO4沉淀也可以转化为BaCO3沉淀。答案:BaSO4在溶液中存在BaSO4(s)
Ba2+(aq)+ SO42-(aq),当加入浓度较高的Na2CO3溶液,CO32-与Ba2+结合生成BaCO3沉淀,使上述平衡向右移动。所以BaSO4沉淀也可以转化为BaCO3沉淀。答案:BaSO4在溶液中存在BaSO4(s) ![]() Ba2+(aq)+ SO42-(aq),当加入浓度较高的Na2CO3溶液,CO32-与Ba2+结合生成BaCO3沉淀,使上述平衡向右移动。
Ba2+(aq)+ SO42-(aq),当加入浓度较高的Na2CO3溶液,CO32-与Ba2+结合生成BaCO3沉淀,使上述平衡向右移动。
(2)①甲溶液可以是NaCl溶液,滴入少量的AgNO3溶液后产生白色沉淀,再滴入KI溶液有黄色沉淀产生。说明有AgCl转化为AgI。故答案为:b。
② 实验Ⅳ的步骤ⅰ中,B中为0.01mol/L的KI溶液,A中为0.1mol/L的AgNO3溶液,Ag+具有氧化性,作原电池的正极,I—具有还原性,作原电池的负极,所以B中石墨上的电极反应式是2I- - 2e- = I2。答案:2I- - 2e- = I2。
③ 由于AgI的溶解度小于AgCl,B中加入AgNO3溶液后,产生了AgI沉淀,使B的溶液中c(I-)减小,I-还原性减弱,根据已知其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大,而离子的浓度越大,离子的氧化性(或还原性)强。 所以实验Ⅳ中b<a。答案:由于生成AgI沉淀使B的溶液中c(I-)减小,I-还原性减弱 。
④虽然AgI的溶解度小于AgCl,但实验Ⅳ中加入了NaCl(s),原电池的电压c>b,说明c(Cl-)的浓度增大,说明发生了AgI + Cl- ![]() AgCl + I-反应,平衡向右移动,c(I-)增大。答案:实验ⅳ表明Cl-本身对该原电池电压无影响,则c>b说明加入Cl-使c(I-)增大,证明发生了AgI + Cl-
AgCl + I-反应,平衡向右移动,c(I-)增大。答案:实验ⅳ表明Cl-本身对该原电池电压无影响,则c>b说明加入Cl-使c(I-)增大,证明发生了AgI + Cl- ![]() AgCl + I- 。
AgCl + I- 。
(3)综合实验Ⅰ~Ⅳ,可得出溶解度小的沉淀容易转化成溶解度更小的沉淀,反之则不易;溶解度差别越大,由溶解度小的沉淀转化为溶解度较大的沉淀越难实现。答案:溶解度小的沉淀容易转化成溶解度更小的沉淀,反之则不易;溶解度差别越大,由溶解度小的沉淀转化为溶解度较大的沉淀越难实现。


科目:高中化学 来源: 题型:
【题目】已知:pKa=lgKa,25℃时,H2SeO3 的 pKa1=1.34, pKa2=7.34。用 0.1molL1NaOH 溶 液滴定 20mL0.1molL1H2SeO3 溶液的滴定曲线如图所示(曲线上的数字为 pH)。下列说法不正 确的是

A. a 点所得溶液中:2c(H2SeO3)+c(SeO32)<0.1 molL1
B. b 点所得溶液中:c(H2SeO3)+c(H+)=c(SeO32)+c(OH)
C. c 点所得溶液中:c(Na+)<3c(HSeO3)
D. d 点所得溶液中:c(Na+)>c(SeO3)>c(HSeO3 )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。硫酸厂的酸性废水中砷(As)元素(主要以H3AsO3形式存在)含量极高,为控制砷的排放,某工厂采用化学沉淀法处理含砷废水。请回答以下问题:
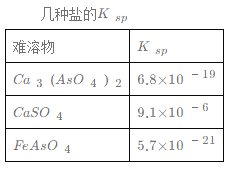
(1)若酸性废水中Fe3+的浓度为1.0×10-4 mol·L-1,则c(AsO43-)不超过 ____mol·L-1。
(2)工厂排放出的酸性废水中的三价砷(弱酸H3AsO3)不易沉降,可投入MnO2先将其氧化成五价砷 (弱酸H3AsO4),此时MnO2被还原为Mn2+,该反应的离子方程式为_________________。
(3)砷酸(H3AsO4)分步电离的平衡常数(25 ℃)为Ka1=5.6×10-3,Ka2=1.7×10-7,Ka3=4.0×10-12,第三步电离的平衡常数表达式为Ka3=_________,Na3AsO4第一步水解的离子方程式为AsO43-+H2O![]() HAsO42-+OH-,该步水解的平衡常数(25 ℃)为____。
HAsO42-+OH-,该步水解的平衡常数(25 ℃)为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、化学实验是化学学习的重要内容,根据你掌握的知识,完成下面内容。实验室需要配制0.1mol·L-1 NaOH溶液230mL,请回答下列问题:
(1)用天平称取______ g NaOH。配制过程中所需玻璃仪器除了胶头滴管和烧杯,还有_____、______ 。
(2)溶解NaOH后的溶液需冷却到室温后方能转移。若趁热转移会使溶液的浓度 _____(填“偏大”、或“偏小”,下同)
(3)有人认为,用这种方法只能配制0.1mol· L-1 的NaOH溶液,而无法得到0.1000mol· L-1 的NaOH溶液,你觉得他的理由是____________ 。
Ⅱ.氯气是一种重要的化工原料,自来水消毒、农药生产、药物合成都需要它。

(1)工业上通常采用电解法制氯气,请观察图1后回答下列问题:
通电后,b侧产生的气体用湿润的淀粉碘化钾试纸检验,现象是变蓝。化学方程式_____
(2)某学生设计如图2所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),回答下列问题:
①在A装置中制取氯气,请写出反应的化学方程式 ____________。
②漂白粉在U形管中产生,其化学方程式是 ____________。
③装置C的作用是__________。
(3)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应发生,可采取的措施是_______。
②试判断另一个副反应(用化学方程式表示)________,为避免此副反应的发生,可以在A与B之间连接一个装有_______ 的洗气瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬酸(用HR 表示)是一种高效除垢剂,现用一定浓度的柠檬酸溶液去除水垢,溶液中H3R、H2R-、HR2-、R3-的含量随pH的变化如图所示。下列说法正确的是

A. H3R的第二步电离常数Ka2(H3R)的数量级为10-4
B. pH=6时,c(R3-)=c(HR2-)>c(H+)>c(OH-)
C. Na2HR溶液中HR2-的水解程度大于电离程度
D. pH=4时,c(H+)=c(H2R-)+2c(HR2-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图装置进行实验(a、b电极均为Cu电极),实验开始观察到灵敏电流计的指针发生偏转。 下列有关说法正确的是

A. b极电极反应为Cu - 2e-=Cu2+B. 溶液中Cu2+穿过交换膜发生迁移
C. 电流计指针偏转幅度将保持不变D. 外电路转移的电子最多为0.02 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,HX溶液、HY溶液、HY和NaY的混合溶液,分别加水稀释,稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是

A. HX、HY均为一元强酸
B. 溶液中水的电离程度:a = b < c
C. 常温下,HY的电离常数Ka约为1.0×10-4
D. c点溶液:c(Na+)>c(Y-)>c(HY) >c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)X原子在第二电子层上只有一个空轨道,则X是__;其轨道表示式为__;R原子的3p轨道上只有一个未成对电子,则R原子可能是__、 ;Y原子的核电荷数为29,其电子排布式是__,其在元素周期表中的位置是__,是属于__区的元素。
(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:__、__、__。
(3)下列分子中若有手性原子,请用“*”标出其手性碳原子__。![]()
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)__。
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4__H2SO3;H3PO4__H3PO3。
(6)根据价层电子对互斥理论判断下列问题:
H2O中心原子的杂化方式为__杂化,分子的立体构型为__。
BF3分子中,中心原子的杂化方式为__杂化,分子的立体构型为__。
(7)H2O的沸点(100℃)比H2S的沸点(﹣61℃)高,这是由于________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(一) 现代铝的精炼研究方向是减低能耗。如图 :室温下通过电解在阴极沉积纯铝,A1Br3 在苯(简写 ArH)中可以生成[A12Br5ArH]+和 Br-。

(1)阳极的材料________;
(2)写出阴极沉积铝的电极方程式__________________________________________;
(二)邻硝基苯甲酸是重要的医院中间体,最新合成方法是邻硝基甲苯和高锰酸钾在相转移催化剂季铵盐(Q+X-)氧化、酸化合成,其原理如下:

相转移催化原理如下:

有关物质的物理性质如下表:
物质 | 邻硝基苯甲酸 | 高锰酸钾 | 苄基三乙基氯化铵(C6H5-CH2CH2)N(C2H5)3Cl | 聚乙二醇 | 四丁基溴化铵(C4H9)4NBr | NH4Cl |
水 | 难溶 | 易溶 | 可溶 | 任意比互溶溶 | 可溶 | 易溶 |
有机物 | 易溶 | 难溶 | 易溶 | 易溶 | 易溶 | 难溶 |
下列说法不合理的是________;
A.相转移催化剂作用主要决定于 Q+的物理化学性质
B.反应中为了防止温度剧烈升高,投料应该分批加入
C.Q+X-是通过增大反应接触面积提高反应速率
D.增大压强可以提高邻硝基甲苯氧化的反应限度
E.工业使用季铵盐(Q+X-)可以提高邻硝基苯甲酸产率
(2)四丁基溴化铵(C4H9)4NBr 萃取水中的高锰酸钾的方程式为:KMnO4(aq) +Q+X-(aq) →Q+ MnO4- (aq) +KX(aq),写出平衡常数 k 的表达式________________;设n(Q+X-):n(邻硝基甲苯)=x,理论证明当 x=5%邻硝基甲酸产率 y 得到最大值,请画出 y 随 x 变化的示意图________________ 。
(3)实验表明,当温度 100℃、反应时间 2.5h,n(KMnO4): n(邻硝基甲苯)=3:1,催化剂用量相同,Q+X-反应的催化效果如下:
相转移催化剂 | 苄基三乙基氯化铵 (C6H5-CH2CH2) N(C2H5)3Cl | 聚乙二醇 | 四丁基溴化铵 (C4H9)4NBr |
产率% | 46.7 | 20.0 | 53.1 |
苄基三乙基氯化铵比四丁基溴化铵催化效果差的原因_____________________________;工业生产不用聚乙二醇做催化剂的主要原因____________________________________ ;
(4)(C4H9)4NBr 为催化剂,邻硝基甲苯和高锰酸钾反应,测得溶液酸碱性对产率、反应时间影响如图 ,下列推测合理的是________。

A.溶液碱性强产率降低是因为季铵盐发生水解反应
B.pH=2 高锰酸钾一定发生副反应
C.选择 pH=7、适当升温可以提高产率
D.工业可以选择浓硝酸替代高锰酸钾做氧化剂,减缓对设备的腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com