
| ||
| A����Ϊ������H2SO4Ϊ���Һ |
| B����Ϊ������ŨNaOHΪ���Һ |
| C�����������ĵ缫��ӦΪFe+8OH--6e-�T4H2O+FeO42- |
| D����ʧȥ3 mol���ӿ����������õ�33.6 L���� |
| ||


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| ���ȼ�ѹ |
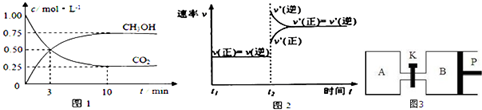
| ���� | CH3OH | CH3OCH3 | H2O |
| c/mol L -1 | 0.9 | 0.60 | 0.60 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
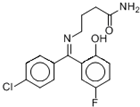
| A���÷�����1H�˴Ź���������12���� |
| B�������ڿ����е����ӱȻ������������� |
| C��1 mol���ӱ�������3 mol NaOH��Ӧ |
| D��һ�������£�1mol���ӱ��������2mol H2�����ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
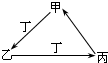 �ס��ҡ����������������У��ס��ҡ�����������ͬ��ij��Ԫ�أ�����֮���������ͼת����ϵ�������й����ʵ��ƶ���ȷ���ǣ�������
�ס��ҡ����������������У��ס��ҡ�����������ͬ��ij��Ԫ�أ�����֮���������ͼת����ϵ�������й����ʵ��ƶ���ȷ���ǣ�������| A������Ϊ��̿��������O2 |
| B������ΪFe��������Cl2 |
| C������ΪAlCl3��������NH3 |
| D������ΪNaHCO3��������HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ˮ�ĵ���̶��������ּ�С |
| B��c��CH3COOH����c��CH3COO?��֮��ʼ�ձ��ֲ��� |
| C����Һ����������ǿ����� |
| D�������백ˮ�����Ϊ10mLʱ��c��NH4+��=c��CH3COO?�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Һ��pHֵ����Ϊ1 |
| B��ˮ�ĵ����ܵ��ٽ� |
| C��ˮ�����ӻ�����С |
| D������Һ��pHֵһ��Ϊ13 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʱ��t/min | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
| P/P0 | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com