
【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
A | |||||||||||||||||
B | C | D | E | F | T | ||||||||||||
G | H | I | J | K | L | ||||||||||||
M | N | O | |||||||||||||||
试回答下列问题(注意:每问中的字母代号为上表中的字母代号,并非为元素符号)
(1)N的单质和水蒸气反应能生成固体X,则I的单质与X反应的化学方程式_______。
(2)D的气态氢化物的VSEPR模型的名称为_______。
(3)由A、C、D形成的ACD分子中,σ键和π键个数比= _______________。
(4)要证明太阳上是否含有R 元素,可采用的方法是__________________________。
(5)元素M的化合物(ME2L2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。回答问题:
①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是_________(填“极性”或“非极性”)分子。
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成原电池,则组成负极材料的元素的外围电子轨道表示式为______________________。
(6)往O2+溶液中加入氨水,形成蓝色沉淀,继续加入氨水,难溶物溶解变成蓝色透明溶液,写出沉淀溶解的离子方程式_____。
(7)若F 、K两种元素形成的化合物中中心原子的价电子全部参与成键,则该化合物的空间构型的名称为___。
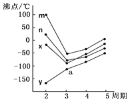
(8)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,则E的氢化物所在的折线是__(填m、n、x或y)。
(9)1183 K以下纯N晶体的基本结构单元如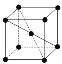 所示,1183 K以上转变为
所示,1183 K以上转变为 所示结构的基本结构单元。在1183 K以下的晶体中,空间利用率为____;在1183 K以上的晶体中,与N原子等距离且最近的N原子数为____,晶体堆积方式的名称为_____。
所示结构的基本结构单元。在1183 K以下的晶体中,空间利用率为____;在1183 K以上的晶体中,与N原子等距离且最近的N原子数为____,晶体堆积方式的名称为_____。
【答案】8Al+3Fe3O4![]() 4Al2O3+9Fe 四面体 1:1 对太阳光进行光谱分析 非极性
4Al2O3+9Fe 四面体 1:1 对太阳光进行光谱分析 非极性 ![]() Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2+ + 2OH- + 4H2O 正八面体 m
Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2+ + 2OH- + 4H2O 正八面体 m ![]() 或68% 12 面心立方最密堆积
或68% 12 面心立方最密堆积
【解析】
A为H,R为He,B为Li,C为C,D为N,E为O,F为F,T为Ne,G为Na,H为Mg,I为Al,J为Si,K为S,L为Cl,M为Cr,N为Fe,O为Cu。
(1)Fe的单质和水蒸气反应能生成固体Fe3O4,则Al与Fe3O4反应生成Fe和Al2O3,其化学方程式8Al+3Fe3O4 ![]() 4Al2O3+9Fe;故答案为:8Al+3Fe3O4
4Al2O3+9Fe;故答案为:8Al+3Fe3O4 ![]() 4Al2O3+9Fe。
4Al2O3+9Fe。
(2)D的气态氢化物NH3的价层电子对数为![]() ,VSEPR模型的名称为四面体形;故答案为:四面体形。
,VSEPR模型的名称为四面体形;故答案为:四面体形。
(3)由A、C、D形成的ACD分子HCN,其结构为H—C≡N,σ键和π键个数比为1:1;故答案为:1:1。
(4)要证明太阳上是否含有He元素,可采用的方法是对太阳光进行光谱分析;故答案为:对太阳光进行光谱分析。
(5)①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,CCl4、CS2是非极性分子,根据相似相溶原理得出ME2L2是非极性分子;故答案为:非极性。
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成Cu—Al—浓硝酸原电池,则组成负极材料是铜,其外围电子轨道表示式为![]() ;故答案为:
;故答案为:![]() 。
。
(6)往Cu2+溶液中加入氨水,形成蓝色沉淀,继续加入氨水,难溶物溶解变成蓝色透明溶液,发生的是氢氧化铜和氨水反应生成四氨合铜子、氢氧根和水,其沉淀溶解的离子方程式Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2+ + 2OH- + 4H2O;故答案为:Cu(OH)2+ 4NH3·H2O = [Cu(NH3)4]2+ + 2OH- + 4H2O。
(7)若F、K两种元素形成的化合物中中心原子的价电子全部参与成键则形成SF6,则该化合物的空间构型的名称为正八面体;故答案为:正八面体。
(8)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,沸点最高的是H2O,因此m为H2O,n为HF,x为NH3,y为CH4,则E的氢化物为H2O,其所在的折线是m;故答案为:m。
(9)在1183 K以下的晶体中,则该晶体为体心立方,设原子半径为r,根据体对角线为4r,则晶胞参数为![]() ,则空间利用率为
,则空间利用率为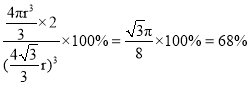 ;在1183 K以上的晶体中,晶体堆积方式为面心立方最密堆积,与N原子等距离且最近的N原子数为12;故答案为:
;在1183 K以上的晶体中,晶体堆积方式为面心立方最密堆积,与N原子等距离且最近的N原子数为12;故答案为:![]() 或68%;12;面心立方最密堆积。
或68%;12;面心立方最密堆积。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】乙二酸(HOOC-COOH)俗称草酸。草酸晶体的化学式为H2C2O4·2H2O,草酸在100℃时开始升华,157℃时大量升华,并开始分解产生CO、CO2和H2O,草酸蒸气在低温下可冷凝为固体;草酸是一种二元弱酸但酸性比碳酸强,具有还原性能使酸性高锰酸钾溶液褪色,草酸钙难溶于水,回答下列问题:
(1)写出草酸晶体受热分解的化学方程式___。
(2)可用下列装罝验证草酸晶体的分解产物(草酸晶体分解装置、夹待装置及连接导管均略去)。
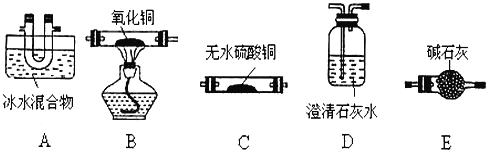
①装置的连接顺序为:___、___DEDE___、___。
②A装置的作用是___,检验产物中有CO的实验现象是___。
③写出整套装置存在不合理之处___。
(3)下列叙述能说明草酸具有弱酸性的是___。
a.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
b.测定草酸钠(Na2C2O4)溶液的pH
c.等体积等浓度的草酸溶液和稀硫酸,稀硫酸消耗碱的能力强
d.pH=2的草酸溶液和稀硫酸,分别稀释100倍后前者pH小
e.将草酸晶体加入Na2CO3溶液中,有CO2放出
(4)已知:NH3·H2ONH4++OH-,Kb=1.85×10-5
H2C2O4H++HC2O4-,Ka1=5.4×10-2
HC2O4-H++C2O42-,Ka2=5.4×10-5
则(NH4)2C2O4溶液的pH___7(填“>”或“<”或“=”)。
(5)可用0.10mol/L酸性KMnO4标准溶液来滴定未知浓度的草酸溶液。
①确定过程中发生反成的离子方程式为___;
②滴定过程中操作滴定管的图示正确的是___。
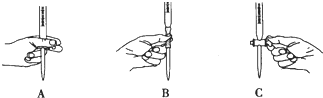
③每次准确量取25.00mL草酸溶液,滴定三次分别消耗0.10mol/L酸性KMnO4标准溶液的体积是20.00mL、19.80mL、20.20mL,则该草酸溶液的物质的量浓度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)难溶物PbSO4溶于CH3COONH4溶液可制得易溶于水的(CH3COO)2Pb,发生的反应为PbSO4+2CH3COONH4=CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是___(填“强”或“弱”)电解质。
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是___元酸(填“一”、“二”或“三”)。
(3)工业上制玻璃和水泥需用到的共同原料是___ (填名称)。
(4)Fe(OH)3胶体可用作净水剂,取少量Fe(OH)3胶体于试管中,向试管中逐渐滴加稀盐酸至过量,产生的现象为___。
(5)已知:5NH4NO3![]() 2HNO3+4N2↑+9H2O,则该反应中氧化产物与还原产物的质量比为___。
2HNO3+4N2↑+9H2O,则该反应中氧化产物与还原产物的质量比为___。
(6)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C进行解毒。下列叙述正确的是___ (填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+氧化为Fe2+ D.亚硝酸盐是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列浓度关系正确的是
A.0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全:c (NH4+)>c (OH-)>c (SO42-)>c (H+)
B.0.1 mol/L的KOH溶液中通入标准状况下的CO2气体3.36 L,所得溶液中:c (K+)+c (H+)=c (CO32-)+c (HCO3-)+c (OH-)
C.0.1 mol/L的NaOH溶液与0.2 mol/L的HCN溶液等体积混合,所得溶液呈碱性:c (HCN)>c (Na+)>c (CN-)>c (OH-)>c (H+)
D.pH相同的NaOH溶液、CH3COONa溶液、Na2CO3溶液、NaHCO3溶液的浓度:c (NaOH)<c (CH3COONa)<c (NaHCO3)<c (Na2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是( )
A. 向0.10mol·L-1NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-)
B. 向0.10mol·L-1NaHSO3溶液中通入NH3:c(Na+)>c(NH4+)>c(SO32-)
C. 0.10mol·L-1Na2SO3溶液通入SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)]
D. 0.10mol·L-1CH3COONa溶液中通入HCl:c(Na+)>c(CH3COOH)=c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中列出了25C、101kPa时一些物质的燃烧热数据
物质 | CH4 | C2H2 | H2 |
燃烧热/( kJ·mol-1) | 890.3 | 1299.6 | 285.8 |
已知键能:C—H键:413.4 kJ·mol-1、H—H键:436 kJ·mol-1,乙炔的结构是为H—C![]() C—H则下列叙述正确的是( )
C—H则下列叙述正确的是( )
A.2H2(g) + 2O2(g) = 2H2O(g) ΔH = -571.6 kJ·mol-1
B.CH4和C2H2中所含化学键完全相同
C.2CH4(g) = C2H2(g) + 3H2(g) ΔH = -376.4 kJ·mol-1
D.C![]() C键能为796 kJ·mol-1
C键能为796 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确且解释合理的是
说法 | 解释 | |
A | 一定温度压强下,2 g H2 和 4 g H2 完全燃烧,后者 燃烧热的数值大 | 4 g H2 放出热量多 |
B | 2SO2(g)+O2(g) 平衡后再加入 SO2,Q 增大 | 平衡右移,放出热量增多 |
C | 向等物质的量浓度的 NaI 和 KBr 混合液中滴加 AgNO3 溶液,先生成黄色 AgI 沉淀 | Ksp(AgI)<Ksp(AgBr) |
D | 等物质的量浓度 Na2CO3 的 pH 大于 CH3COONa | H2CO3 的酸性比 CH3COOH 强 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.同一可逆反应使用不同的催化剂时,高效催化剂可增大平衡转化率
B.已知反应H2O(g) +SO2(g)= H2SO3 (l),该过程熵值增大
C.同温同压下,H2(g) + Cl2(g) =2HCl(g)在光照和点燃条件下的ΔH不同
D.已知2H2O(l) =2H2(g) + O2(g) ΔH = +571.6 kJ·mol-1,则氢气燃烧热为285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
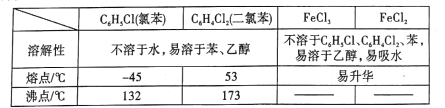
(1)用H2还原无水FeCl3制取FeCl2。有关装置如图1所示:
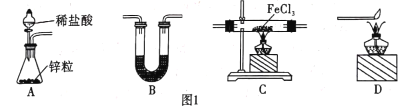
①H2还原无水FeCl3制取FeCl2的化学方程式为________ 。
②B中盛放的试剂是____,按气流由左到右的方向,上述仪器的连接顺序为 ____(填字母,装置可多次使用)。
③该制备装置的缺点为______。
(2)利用反应![]() ,制取无水FeCl2并测定FeCl3的转化率。按图2装置,在三颈烧瓶中放入32.5 g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。
,制取无水FeCl2并测定FeCl3的转化率。按图2装置,在三颈烧瓶中放入32.5 g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。
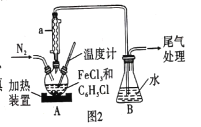
①仪器a的作用是 _______。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是____(填名称),回收滤液中C6H5Cl的操作方法是____。
③在反应开始之前先通一段时间N2的目的是 ____,在反应完成后继续通一段时间N2的作用是____
④反应后将锥形瓶中溶液配成250 mL,量取25. 00 mL所配溶液,用0.40 mol·L-1 NaOH溶液滴定,重复上述操作3次,达到滴定终点时消耗NaOH溶液的体积分别为19. 50 mL、20. 50 mL、19. 70 mL,则氯化铁的转化率为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com