
【题目】参考下列图表和有关要求回答问题:
(1)图Ⅰ是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是___(填“增大”“减小”或“不变”,下同),ΔH的变化是__。请写出NO2和CO反应的热化学方程式:__。

(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0kJ·mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44kJ·mol-1
则甲醇燃烧生成液态水的热化学方程式:___。
(3)下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能/kJ·mol-1 | a | b | c | x |
已知1mol白磷(P4)完全燃烧放热为dkJ,白磷及其完全燃烧的产物结构如图Ⅱ所示,则表中x=___kJ·mol-1(用含有a、b、c、d的代数式表示)。

【答案】减小 不变 NO2(g)+CO(g)=CO2(g)+NO(g) ΔH=-234kJ·mol-1 CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(l) ΔH=-764.7kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=-764.7kJ·mol-1 ![]()
【解析】
加入催化剂能降低反应所需的活化能,但是不改变反应物的总能量和生成物的总能量,由图可知,1molNO2和1molCO反应生成CO2和NO放出热量368-134=234kJ,根据热化学方程式书写原则进行书写;
依据热化学方程式,利用盖斯定律即化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关,进行计算;
白磷燃烧的方程式为![]() ,结合1mol白磷中含有6molP-P,1molO2中含有1molO-O,1molP4O10中含有12mol P-O、4mol P=O分析;
,结合1mol白磷中含有6molP-P,1molO2中含有1molO-O,1molP4O10中含有12mol P-O、4mol P=O分析;
化学反应中旧键断裂需要吸收能量,新键形成需要放出能量,结合化学反应中的反应热△H=反应物总键能-生成物总键能分析。
(1)加入催化剂能降低反应所需的活化能,则E1和E2都减小,催化剂不能改变反应物的总能量和生成物的总能量之差,即反应热不改变,所以催化剂对反应热无影响,由图可知,1molNO2和1molCO反应生成CO2和NO放出热量368-134=234kJ,反应热化学方程式为![]() ;故答案为:减小;不变;
;故答案为:减小;不变;
![]() ;
;
(2)![]() ①
①
![]() ②
②
![]() ③
③
依据盖斯定律,②×3-①×2+③×2得:![]()
![]() (3)加入催化剂能降低反应所需的活化能,则E1和E2都减小,催化剂不能改变反应物的总能量和生成物的总能量之差,即反应热不改变,所以催化剂对反应热无影响,所以
(3)加入催化剂能降低反应所需的活化能,则E1和E2都减小,催化剂不能改变反应物的总能量和生成物的总能量之差,即反应热不改变,所以催化剂对反应热无影响,所以![]() ,解得
,解得![]() 。
。
故答案为![]() 。
。


科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅的冶炼大致过程如下:
①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O2![]() 2PbO+2SO2;
2PbO+2SO2;
③制粗铅:PbO +C![]() Pb +CO↑;PbO+CO
Pb +CO↑;PbO+CO![]() Pb+CO2。
Pb+CO2。
下列说法错误的是( )
A.浮选法富集方铅矿的过程,属于物理变化
B.将lmolPbS冶炼成Pb,理论上至少需要12g碳
C.方铅矿焙烧反应中,PbS是还原剂,还原产物只有PbO
D.焙烧过程中,每生成lmolPbO转移6mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在高温下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)元素名称:A______;B______;C______;D______。
(2)D元素位于周期表中______周期______族。
(3)写出AB2与C2B2反应的化学方程式______。
(4)画出B的原子结构简图______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用NaOH固体配制250 mL 1.25 mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250 mL 1.25 mol/L的NaOH溶液
应称取NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它玻璃仪器 |
__________ | __________ | __________ |
(2)容量瓶上需标有以下五项中的__________;
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)__________;
A、用30 mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水(约30 mL),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是__________,溶液注入容量瓶前需恢复到室温,这是因为__________
(5)下列配制的溶液浓度偏低的是(_____)
A.称量NaOH时,砝码错放在左盘
B.向容量瓶中转移溶液时(实验步骤②)不慎有液滴洒在容量瓶外面
C.加蒸馏水时不慎超过了刻度线
D.定容时俯视刻度线
E.配制前,容量瓶中有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①标准状况下,1体积水中最多能溶解500体积的HCl;②饱和NaCl溶液的浓度约为5.00mol/L 。将448L(标准状况下)HCl气体溶于1L水中,所得溶液A的密度为1.20g·cm-3,则溶液A中HCl的物质的量浓度为__________。(本题计算结果均取三位有效数字)
(1)若使1L饱和NaCl溶液中的Cl-浓度与溶液A中的Cl-浓度相等,则在1L饱和NaCl溶液中还应溶解__________L标准状况下的HCl气体(溶液体积变化忽略不计)。
(2)若将10.0mL溶液A稀释成500mL溶液B,则溶液B中HCl的物质的量浓度为__________。
(3)在溶液B的配制过程中,使用前必须检查是否漏液的仪器是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120℃时,将0.1 mol 氢气、2.8 g一氧化碳和0.05 mol 氮气的混合气体与足量氧气充分燃烧后,立即将所得混合气体通过足量的过氧化钠粉末,固体质量增加
A.2.8 gB.3.0 gC.7.2 gD.5.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0.02mol·L-1CuSO4溶液中匀速滴加1mol·L-1氨水,先观察到有浅蓝色沉淀[Cu2(OH)2SO4]生成,后沉淀溶解,逐渐变为深蓝色溶液。该实验过程体系的pH和电导率随时间的变化如图所示。下列说法正确的是
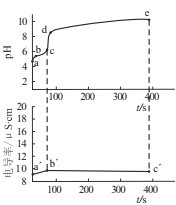
A.c(Cu2+):a点=b点
B.bc段生成浅蓝色沉淀的反应为![]()
C.d点时:![]()
D.导电能力:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.Cl2通入水中制氯水:![]()
B.NO2通入水中制硝酸:![]()
C.![]() NaAlO2溶液中通入过量CO2:
NaAlO2溶液中通入过量CO2:![]()
D.![]() AgNO3溶液中加入过量浓氨水:
AgNO3溶液中加入过量浓氨水:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com