
【题目】下列装置或操作不能达到目的的是( )
A.装置①验证温度对反应2NO2(g)N2O4(g)平衡移动的影响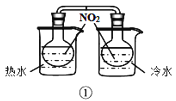
B.装置②验证增大反应物浓度对平衡的影响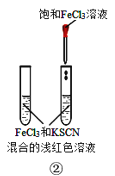
C.装置③测定中和热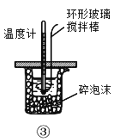
D.装置④比较Cu2+、Fe3+对H2O2分解速率的影响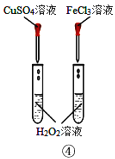
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.已知常温下,在NaHSO3溶液中c(H2SO3)<c(![]() ),且H2SO3的电离平衡常数为K1=1.5×10-2,K2=1.1×10-7;氨水的电离平衡常数为K=1.8×10-5;回答下列问题:
),且H2SO3的电离平衡常数为K1=1.5×10-2,K2=1.1×10-7;氨水的电离平衡常数为K=1.8×10-5;回答下列问题:
(1)等物质的量浓度的下列五种溶液:①NH3·H2O ②(NH4)2SO3 ③KHSO3 ④K2SO3 ⑤H2SO3溶液中水的电离程度由大到小排列顺序为____________(填序号)。
(2)NaHSO3可以将碘盐中的KIO3还原为碘单质,试写出此反应的离子方程式:_________________________________________。
Ⅱ.(1)在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显________(填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=_____________。
(2)已知H2CO3的第二级电离常数K2=5.6×10-11,HClO的电离常数K=3.0×10-8,写出下列条件下所发生反应的离子方程式:
①少量Cl2通入到过量的Na2CO3溶液中:___________________________________。
②Cl2与Na2CO3按物质的量之比1∶1恰好反应:_______________________。
③少量CO2通入到过量的NaClO溶液中:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
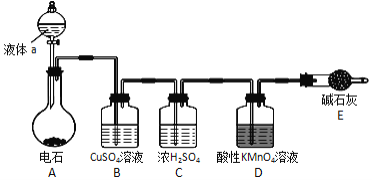
(1)写出实验室制取乙炔的化学方程式:____;
(2)实验室制取乙炔时,分液漏斗中的液体a通常是____;
(3)装置D中的现象是:___;
(4)若D装置中药品为溴水,其生成四溴代物的反应方程式为:____;
(5)工业上常用乙炔、饱和食盐水等物质作原料来合成聚氯乙烯,请写出相关方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+3B(g)2C(g)+2D(g),其中反应速率最快的是( )
A.v(D)=0.30mol·L-1·s-1B.v(A)=0.50mol·L-1·s-1
C.v(B)=0.60mol·L-1·s-1D.v(C)=0.50mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程中,熵变小于0的是
A.H2O(s)→H2O(l)→H2O(g)
B.N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
C.NaOH(s)=Na+(aq)+OH-(aq)
D.2NaHCO3(s)![]() Na2CO3(s)+CO2(g)+H2O(g)
Na2CO3(s)+CO2(g)+H2O(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W形成的最高价氧化物分别为甲、乙、丙。x、y2、z、w分别为X、Y、Z、W的单质,丁是化合物。其转化关系如图所示,下列判断正确的是( )

A.反应①、②属于氧化还原反应,③属于非氧化还原反应
B.Y的离子半径比Z的离子半径小
C.反应③可以证明X的非金属性强于W
D.一定条件下,x与甲反应生成丁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有![]() 某气体(由双原子分子构成),其摩尔质量为
某气体(由双原子分子构成),其摩尔质量为![]() ,阿伏加德罗常数用
,阿伏加德罗常数用![]() 表示,试求
表示,试求
①该气体在标准状况下的体积为____![]() 。
。
②该气体所含原子数为____。
(2)用双线桥表示铜与浓硫酸反应的电子转移方向和数目:__________________

当有![]() 被还原时,转移电子的物质的量为____
被还原时,转移电子的物质的量为____![]() ,生成标准状况下
,生成标准状况下![]() 的体积为___
的体积为___![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向20mL0.1mol·L-1的醋酸溶液中不断滴加0.1mol·L-1的NaOH溶液,溶液的pH变化曲线如图所示,在滴定过程中,下列关于溶液中微粒浓度大小关系的描述不正确的是( )

A.a点时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.b点时:c(Na+)>c(CH3COO-)
C.c点时:c(OH-)=c(CH3COOH)+c(H+)
D.d点时:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用闪锌矿(主要成分为ZnS,还含有Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:

(1)滤渣A经CS2提取后可获得一种淡黄色副产品,其化学式为____。
(2)浸取过程中Fe2(SO4)3的作用是________ (氧化剂或还原剂)。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为_________。该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是________。
(4)置换法除重金属离子所用物质C为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com