
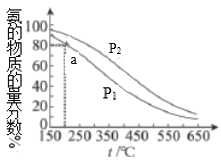
【题目】将物质的量之比为1:3的氮气和氢气充入恒容密闭容器中,测定不同温度、压强下平衡混合物中氨的物质的量分数,结果如图所示。下列说法不正确的是( )
A.![]()
B.该反应![]()
C.![]() 点,
点,![]() 的转化率为
的转化率为![]()
D.合成氨工业实现了人工固氮
【答案】C
【解析】
物质的量之比为1:3的氮气和氢气充入恒容密闭容器中,发生反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
A. 根据氮气与氢气的反应方程式,反应前后气体分子数发生改变,温度相同,压强增大,平衡正向移动,氨的物质的量分数增大,所以根据图可知,![]() ,A正确;
,A正确;
B. 根据图可知,温度升高,氨的物质的量分数减小,所以该反应的正反应为放热反应,![]() ,B正确;
,B正确;
C. ![]() 点,
点,![]() 的物质的量分数为
的物质的量分数为![]() ,则设开始投的氮气的物质的量为1 mol,氢气的物质的量为3 mol,转化的氮气为x mol,根据三段式:
,则设开始投的氮气的物质的量为1 mol,氢气的物质的量为3 mol,转化的氮气为x mol,根据三段式:
N2 (g) + 3H2 (g) ![]() 2NH3 (g)
2NH3 (g)
始![]()
转 ![]()
平![]()
则![]() ,
,![]() ,所以
,所以![]() 的转化率为:
的转化率为: ,C错误;
,C错误;
D. 人工固氮就是利用氮气和氢气反应生成氨气的原理,所以合成氨工业实现了人工固氮,D正确;故答案为:C。


 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】以下是元素周期表中前18号某种金属元素对应的单质及其化合物之间的转化关系(“→”所指的转化都是一步完成)。
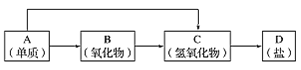
(1)若B为呼吸面具中的供氧剂,其供氧时每生成1molO2,反应过程中转移的电子数为_____,A与FeCl3溶液反应的离子方程式________________________。
(2)写出一个“C→D”转化的化学方程式_________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.将标况下22.4 mL HCl气体溶于1 L水可配成浓度为1![]() 10-3mol·L-1的盐酸
10-3mol·L-1的盐酸
B.一定条件下,1 mol Fe与1 mol Cl2充分反应,Fe失去的电子数目为3NA
C.标准状况下,22.4 L H2O所含的水分子数目为NA
D.500 mL 1 mol·L-1 MgCl2溶液中所含有Cl-浓度为2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=13,则在该温度下,将100 mL 0.10 mol/L的稀硫酸与100 mL 0.40 mol/L的NaOH溶液混合后,溶液的pH为(已知:忽略混合时体积的变化;lg2=0.30;lg3=0.48)
A. 11.52 B. 11.70
C. 11.82 D. 12.00
查看答案和解析>>
科目:高中化学 来源: 题型:
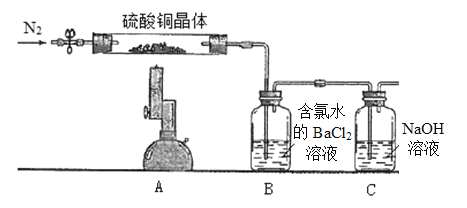
【题目】Ⅰ.为探究硫酸铜晶体(CuSO4·xH2O)受热分解后所得产物,设计实验装置如图所示,部分实验现象为:A中蓝色晶体逐渐变成白色粉末,继续加热最终变成黑色;B中产生白色沉淀;D中溶液变成红色。(洗气瓶中试剂均足量)

(1)分析推测该硫酸铜晶体最终分解产物可能有_______________________________。
(2)D中的反应分两步进行,写出第一步反应的离子方程式_____________________。
II.测定硫酸铜晶体(CuSO4·xH2O)中结晶水x的值,实验装置和过程如下:取硫酸铜晶体7.23 g置于硬质试管中,先通N2排除体系内空气,酒精喷灯高温加热充分,待A中蓝色晶体最终变成黑色,停止加热,再次鼓入N2至装置冷却到室温。(洗气瓶中试剂均足量)
(1)取B中白色沉淀经过滤洗涤干燥称量得固体6.99 g,经计算可得CuSO4·xH2O中x=__________,再次鼓入N2的目的是____________________。
(2)某同学提出,要测定晶体中结晶水x的值,也可将B装置用装有浓硫酸的洗气瓶替换,最终测浓硫酸增重即可计算得到结果,评价该同学的方案是否可行?(如果不可行,请说明理由)_____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50 mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示,且每一段只对应一个反应。下列说法正确的是( )

A. 开始时产生的气体为H2
B. AB段发生的反应为置换反应
C. 参加反应铁粉的总质量m2=5.6 g
D. 所用混合溶液中c(HNO3)=0.5 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铬常用于提升特种合金的性能。工业上以铬铁矿(主要成份为FeO·Cr2O3,含有少量Al2O3)为原料制备金属铬的流程如下图。下列说法不正确的是( )
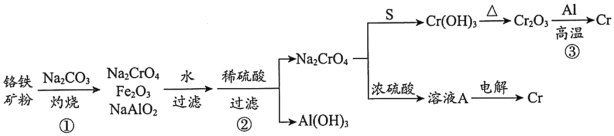
A.①中需持续吹入空气作氧化剂B.②中需加入过量稀硫酸
C.③中发生了置换反应D.溶液A为橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在12g某二价金属的硫酸盐中,含有0 4mol氧原子,此硫酸盐的摩尔质量为_________g/mol。
(2)质量分数为49%的硫酸溶液,密度为1.8g/cm3,则物质的量浓度为__________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)K2Cr2O7是橙红色晶体,K2CrO4是黄色晶体,若将K2Cr2O7配成一定浓度的溶液,当达到平衡时,溶液的颜色在橙色和黄色之间,试回答:
①写出有关的离子方程式____。
②向盛有2mL的上述K2Cr2O7溶液的试管中滴入10滴2mol·L-1的NaOH溶液,试管中溶液呈___色。
③向已加入NaOH溶液的②溶液中再加入过量稀H2SO4,则溶液呈___色。
④向原溶液中逐渐加入足量Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡____(填“向左移动”或“向右移动”),溶液颜色将___。
(2)现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
①升高温度时,平衡向___反应方向移动,正反应为____(填“吸热”或“放热”)反应,平衡时B、C的浓度之比![]() 将____。(填“增大”“减小”或“不变”,下同)。
将____。(填“增大”“减小”或“不变”,下同)。
②减小压强时平衡向___反应方向移动, A的质量分数___,且m+n__p(填“>”或“<”)。
③若容积不变加入B,则B的转化率____,A的转化率____。
④若加入催化剂,平衡时气体混合物的总物质的量____。
⑤恒温恒容时,通入氦气,A的质量分数____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com