
某一元有机酸HA的溶液中,若未电离的HA分子个数与溶液中的离子个数比为a:b,则HA的电离度(即转化率)是( )
|
| A. |
| B. |
| C. |
| D. |
|
| 弱电解质在水溶液中的电离平衡.. | |
| 专题: | 电离平衡与溶液的pH专题. |
| 分析: | 在溶液中存在HA⇌H++A﹣,则若未电离的HA分子个数与溶液中的离子个数比为a:b,设分别为amol、bmol,则总的HA为amol+ |
| 解答: | 解:溶液中存在HA⇌H++A﹣,则若未电离的HA分子个数与溶液中的离子个数比为a:b,设分别为amol、bmol,则总的HA为amol+ 则HA的电离度为 故选A. |
| 点评: | 本题考查弱电解质的电离,侧重学生的分析能力和计算能力的考查,注意把握电离度的计算公式的运用,难度不大. |


科目:高中化学 来源: 题型:
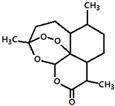
2011年9月23日,中国科学家屠呦呦获得了美国拉斯克医学奖的临床医学奖,获奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”。下图是青蒿素的结构,则有关青蒿素的说法中不正确的是:
A.青蒿素分子式为C15H22O5
B.青蒿素有—O—O—键具有较强的氧化性
C.青蒿素易溶于水、乙醇、苯
D.青蒿素在碱性条件下易发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
300mL某浓度的NaOH溶液中含有60g溶质,现欲配制1mol/L NaOH溶液,应取原溶液与蒸馏水的体积比约为( )
A.1∶4 B.1∶5 C.2∶1 D.2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质全部是弱电解质的是( )
A.H2SiO3 H2S CO2 B.MgSO4 CH3COOH CH3CH2OH
C.H2SO3 BaSO4 CH4 D.H2O NH3•H2O H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
在NH3•H2O⇌NH4++OH﹣形成的平衡中,要使NH3•H2O的电离程度及c(OH﹣)都增大,可采取的措施是( )
|
| A. | 通入HCl | B. | 加少量NaOH固体 |
|
| C. | 加少量氯化铵固体 | D. | 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)⇌nY(g);△H=Q kJ/mol.反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
| /L积体气温体c(Y)/mol•L﹣1度/℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是( )
|
| A. | m>n |
|
| B. | Q<0 |
|
| C. | 温度不变,压强增大,Y的质量分数减少 |
|
| D. | 体积不变,温度升高,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)肼(N2H4)是发射航天飞船常用的高能燃料.将NH3和NaClO按一定物质的量比混合反应,生成肼、NaCl和水,该反应的化学方程式是 2NH3+NaClO=N2H4+NaCl+H2O .
(2)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量气体,并放出大量热.已知:H2O(l) H2O(g)△H=+44kJ/mol.12.8g液态肼与足量过氧化氢反应生成氮气和水蒸气,放出256.65kJ的热量.
①请写出液态肼与过氧化氢反应生成液态水的热化学方程式 .
②则16g 液态肼与足量过氧化氢反应生成液态水时放出的热量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列条件下,两种气体所含的原子数一定相等的是( )
A.同质量、不同密度的N2和CO B.同温度、同体积的H2和N2
C.同体积、同密度的C2H6和NO D.同压强、同体积的N2O和CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com