
【题目】硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取t其工艺流程如图1所示. 
(1)为提高锌灰的浸取率,可采用的方法是(填序号).
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是(写化学式).
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S.
①检验ZnS固体是否洗涤干净的方法是 ,
②Na2S可由等物质的量的Na2S04和CH4在高温、催化剂条件下制取.化学反应方程式为
③已知Na2SO4 . 10H2O及Na2SO4的溶解度随温度变化曲线如图2.从滤液中得到Na2SO4.10H2O的操作方法是
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL,物质的量浓度为c mol/L的Na2SO4溶液.则理论上所用锌灰中含有锌元素的质量为 .
【答案】
(1)①②③⑤
(2)Fe(OH)3
(3)Zn(或锌)
(4)取最后一次洗涤液少许于试管,滴加几滴BaCl2溶液,若出现浑浊则未洗净,反之则已洗净;Na2S04+CH4 ![]() Na2S+2H2O+CO2;蒸发浓缩,降温结晶,过滤
Na2S+2H2O+CO2;蒸发浓缩,降温结晶,过滤
(5)65(Vc﹣b﹣d)g
【解析】解:锌灰与硫酸反应得含有镉离子、锌离子、铁离子、亚铁离子等的溶液,加入双氧水将二价铁离子氧化为三价铁离子,用碳酸锌调节平衡pH使Fe(OH)3完全沉淀,过滤后得到含有镉离子、锌离子的滤液Ⅰ,和滤渣为Fe(OH)3 , 步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为锌,过滤后得溶液Ⅱ为硫酸锌溶液,硫酸锌溶液中加入硫化钠可得硫酸钠和硫化锌,(1)搅拌、适当升温、将废渣碾细成粉末、搅拌、多次浸取等都可提高锌灰的浸取率,故选①②③⑤;(2)根据上面的分析可知,步骤Ⅱ所得滤渣中的物质是Fe(OH)3 ,
所以答案是:Fe(OH)3;(3)根据上面的分析可知,试剂b应为锌,
所以答案是:Zn(或锌);(4)①ZnS固体是从硫酸钠溶液中析出的,所以检验ZnS固体是否洗涤干净的方法是取最后一次洗涤液少许于试管,滴加几滴BaCl2溶液,若出现浑浊则未洗净,反之则已洗净,
所以答案是:取最后一次洗涤液少许于试管,滴加几滴BaCl2溶液,若出现浑浊则未洗净,反之则已洗净;②等物质的量的Na2S04和CH4在高温、催化剂条件下生成Na2S,根据元素守恒可知,该化学反应方程式为Na2S04+CH4 ![]() Na2S+2H2O+CO2 ,
Na2S+2H2O+CO2 ,
所以答案是:Na2S04+CH4 ![]() Na2S+2H2O+CO2;③根据溶解度随温度变化曲线可知,从滤液中得到Na2SO4.10H2O的操作方法是蒸发浓缩,降温结晶,过滤,
Na2S+2H2O+CO2;③根据溶解度随温度变化曲线可知,从滤液中得到Na2SO4.10H2O的操作方法是蒸发浓缩,降温结晶,过滤,
所以答案是:蒸发浓缩,降温结晶,过滤; (5)步骤Ⅲ所得Cd为d mol,则用于置换镉的锌的物质的量为d mol,硫酸钠的物质的量为VL×c mol/L=cVmol,所以硫酸锌的物质的量为cVmol,根据锌元素守恒可知,样品中锌元素的物质的量为cVmol﹣d mol﹣b mol,所以锌灰中含有锌元素的质量为65g/mol×(cVmol﹣d mol﹣b mol)=65(Vc﹣b﹣d)g,
所以答案是:65(Vc﹣b﹣d)g.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为ρ g/ml,质量分数为w,物质浓度为cmol/L,则下列关系中不正确的是( )
A.ρ= ![]()
B.W= ![]()
C.W= ![]()
D.C= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某药物具有抗痉挛作用,制备该药物其中一步反应为: 
下列说法不正确的是( )
A.a中参加反应的官能团是羧基
B.生活中b可作燃料和溶剂
C.c极易溶于水
D.该反应类型为取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下.NH4Cl溶液加水稀释, ![]() 增大
增大
B.0.1mol/LNa2CO3溶液加热后,溶液的pH减小
C.室温下稀释O.lmol/LCH3COOH溶液,溶液的导电能力减弱,因此溶液中所有离子浓度均减小
D.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进Fe3+水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含大量Fe2+、Al3+、Fe3+、Na+、Cl﹣、SO ![]() 离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是( )
离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是( )
A.Na+、Fe2+
B.Al3+、SO ![]()
C.Fe3+、SO ![]()
D.Al3+、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) ![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
(1)反应的ΔH________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如图所示。在0~60 s时段,反应速率v(N2O4)为________mol·L-1·s-1;反应的平衡常数K1为_____________。

(2)100 ℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。T______100 ℃(填“大于”或“小于”),判断理由是____________________________________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物.某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究: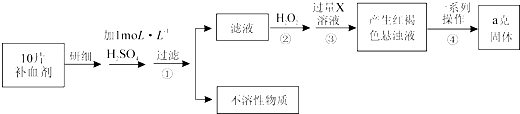
请回答下列问题:
(1)Ⅰ.①实验时用10molL﹣1的浓硫酸,配制100mL 1molL﹣1 H2SO4溶液,所需浓硫酸的体积为mL;②下列操作中,容量瓶所具备的功能有(填序号);
A.配制一定体积准确浓度的标准溶液 B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体 D.用来溶解固体溶质
③在下列配制过程示意图中,有错误的是(填写序号);
④下列说法正确的
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
(2)Ⅱ.①步骤②加入过量H2O2后,溶液中主要存在的金属阳离子是;②从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:a. , b.洗涤,c.灼烧,d.冷却
③若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯气的实验装置能达到实验目的或实验效果的是( ) 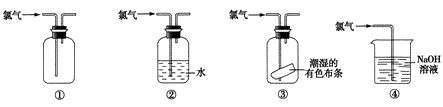
①可用于氯气的收集
②可用于除去氯气中少量的氯化氢气体
③可证明氯气具有漂白性
④可用于实验室氯气的尾气吸收.
A.①②
B.①③
C.②③
D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com