
【题目】已知有机物A、B、C、D、E、F、G有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为C9H10O2,试回答下列有关问题:
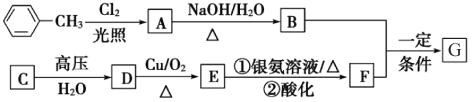
⑴指出下列反应的反应类型:C转化为D:_________。
⑵写出A中官能团的名称:_________。
⑶写出下列反应的化学方程式:
D生成E的化学方程式:_________;E与银氨溶液反应的化学方程式_________;B和F生成G的化学方程式:_________。
⑷写出符合下列条件的G的同分异构体的结构简式:_________。
①能与FeCl3发生显色反应
②能与新制的银氨溶液反应产生光亮的银镜
③核磁共振氢谱显示有四种不同化学环境氢
【答案】加成反应 氯原子 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH3CHO+2Ag(NH3)2OH→CH3COONH4+3NH3+2Ag↓+H2O CH3COOH+
2CH3CHO+2H2O CH3CHO+2Ag(NH3)2OH→CH3COONH4+3NH3+2Ag↓+H2O CH3COOH+![]() +H2O
+H2O 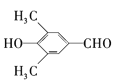 、
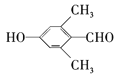
、
【解析】
C的产量可用来衡量一个国家的石油化工发展水平,C为乙烯,乙烯和水高压下反应生成乙醇D,乙醇催化氧化生成乙醛E,乙醛发生银镜反应、酸化得到乙酸F,甲苯和氯气光照发生取代反应得到A(![]() ),A发生水解反应生成B(
),A发生水解反应生成B(![]() ),B和乙酸发生酯化反应生成G(C9H10O2),
),B和乙酸发生酯化反应生成G(C9H10O2),
⑴根据分析可知,C转化为D是乙烯加成反应生成乙醇;故答案为:加成反应。
⑵A(![]() )中官能团的名称:氯原子;故答案为:氯原子。
)中官能团的名称:氯原子;故答案为:氯原子。
⑶D生成E是乙醇催化氧化变为乙醛的反应,其化学方程式:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;E与银氨溶液反应的化学方程式CH3CHO+2Ag(NH3)2OH →CH3COONH4 + 3NH3+2Ag↓+H2O;B和F生成G的化学方程式:CH3COOH+
2CH3CHO+2H2O;E与银氨溶液反应的化学方程式CH3CHO+2Ag(NH3)2OH →CH3COONH4 + 3NH3+2Ag↓+H2O;B和F生成G的化学方程式:CH3COOH+![]()
![]()
![]() +H2O;故答案为:2CH3CH2OH+O2
+H2O;故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;CH3CHO+2Ag(NH3)2OH →CH3COONH4 + 3NH3+2Ag↓+H2O;CH3COOH+
2CH3CHO+2H2O;CH3CHO+2Ag(NH3)2OH →CH3COONH4 + 3NH3+2Ag↓+H2O;CH3COOH+![]()
![]()
![]() +H2O。
+H2O。
⑷①能与FeCl3发生显色反应,说明含酚羟基,②能与新制的银氨溶液反应产生光亮的银镜,说明含有醛基,③核磁共振氢谱显示有四种不同化学环境氢,因此同分异构体为 、
、 ;故答案为:
;故答案为:  、
、 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】如图所示的装置中发生反应2A2(g)+B2(g)2C(g)△H=﹣a kJ/mol(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向容积相同的A、B容器中分别都充入2mol A2和1mol B2气体.两容器分别在500℃达平衡时,A中C的浓度为c1 mol/L,放出热量b kJ,B中C的浓度为c2 mol/L,放出热量c kJ.下列说法中正确的是( )
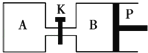
A.500℃达平衡时有:c1>c2
B.500℃达平衡时有:a>b>c
C.达平衡后打开K,容器B的体积将减小
D.此反应的平衡常数随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。下列说法正确的是
![]()
A. Y的原子半径比X的大
B. Q的最高价氧化物的水化物的酸性比Z的强
C. X、Y和氢3种元素形成的化合物中都只有共价键
D. Q的单质具有半导体的性质,Q与Z可形成化合物QZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾天气是一种大气污染状态,雾霾的源头多种多样,比如汽车尾气、工业排放、建筑扬尘、垃圾焚烧,甚至火山喷发等。
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化。
①已知部分化学键的键能如下
分子式/结构式 | NO/N≡O | CO/C≡O | CO2/O=C=O | N2/N≡N |
化学键 | N≡O | C≡O | C=O | N≡N |
键能( kJ/mol) | 632 | 1072 | 750 | 946 |
请完成汽车尾气净化中NO(g)和CO(g)发生反应的热化学方程式
2NO(g)+2CO( g) ![]() N2( g)+2CO2(g) △H=_____kJ·mol-1
N2( g)+2CO2(g) △H=_____kJ·mol-1
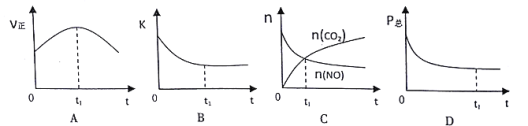
②若上述反应在恒温、恒容的密闭体系中进行,并在t1时刻达到平衡状态,则下列示意图符合题意的是 ____(填选项序号)。(下图中V正、K、n、P总分别表示正反应速率、平衡常数、物质的量和总压强)
(2)在t1℃下,向体积为10 L的恒容密闭容器中通入NO和CO,测得不同时间NO和CO的物质的量如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/×10-2mol | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
n(CO)/×10-1 mol | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
t1℃时该反应的平衡常数K= ___,既能增大反应速率又能使平衡正向移动的措施是_____。(写出一种即可)
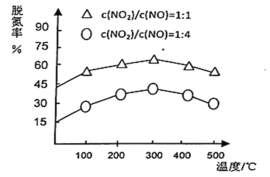
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。在氨气足量的情况下,不同c(NO2)/C(NO)、不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请回答温度对脱氮率的影响________,给出合理的解释:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应![]() 在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.保持容器体积不变,增加H2O(g)的量
B.保持容器体积不变,充入氦气使体系压强增大
C.将容器的体积缩小一半
D.保持容器压强不变,充入氦气使容器体积变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家发明了一种安全可充电的柔性水系钠离子电池,可用生理盐水或细胞培养基为电解质,电池放电的总反应式为:Na0.44MnO2+NaTi2(PO4)3=Na0.44-xMnO2+Na1+xTi2(PO4)3,其工作原理如下图。
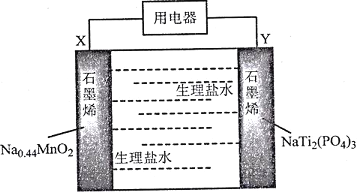
下列说法错误的是
A. 放电时,Cl-向X极移动
B. 该电池充电时Y极应该与电源的正极相连
C. 充电时,阴极反应为:NaTi2(PO4)3+xNa++xe-=Na1+ xTi2( PO4)3
D. 该电池可能作为可植入人体的电子医疗设备的电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的转化系统原理示意图。下列说法正确的是

A. 好氧微生物反应器中反应为:NH4++2O2==NO3-+2H++H2O
B. B极电势比A极电势低
C. A极的电极反应式CH3COO-+8e-+2H2O==2CO2+7H+
D. 当电路中通过1mol电子时,理论上总共生成2.24LN2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为![]() ,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,D为既能溶于强酸又能溶于强碱的白色胶状物质,X为常见的无色液体。反应生成的水均已略去。它们有如下图所示的关系。
,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,D为既能溶于强酸又能溶于强碱的白色胶状物质,X为常见的无色液体。反应生成的水均已略去。它们有如下图所示的关系。
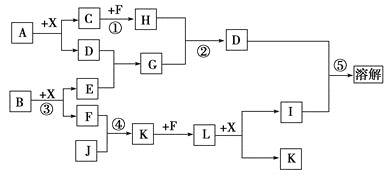
(1)写出A的化学式:________
(2)写出 B的电子式______________
(3)反应![]() 中每生成
中每生成![]() ,转移电子的数目为________
,转移电子的数目为________![]() 用
用![]() 表示阿伏加德罗常数
表示阿伏加德罗常数![]()
(4)反应![]() 的化学方程式为:______________________________
的化学方程式为:______________________________
(5)写出H不足时反应![]() 的离子方程式_______________________________________
的离子方程式_______________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com