
【题目】空气中CO2浓度的持续走高引起人们的高度重视。一些科学家认为,人类不仅要努力减少CO2的排放,还要尽快想办法清除空气中过多的CO2。为此,他们设想了一系列“捕捉”和“封存” CO2的方法。
方法Ⅰ:一些科学家利用太阳能加热的反应器“捕捉”空气中的CO2,如图所示。
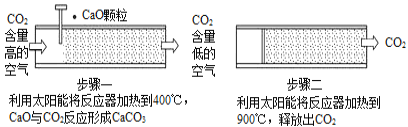
(1)步骤一中的CaO俗称____________。
(2)步骤二中发生反应的化学方程式是____________,该反应____________(填“是”或“不是”)步骤一中反应的逆反应。
方法Ⅱ:另一些科学家利用NaOH溶液的喷淋“捕捉”空气中的CO2,如图所示。
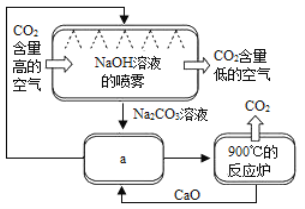
(1)NaOH溶液喷成雾状是为了_________________。
(2)上图a环节中,物质分离的基本操作是__________。
(3)为了尽量减少成本,在整个流程中,循环利用的物质有CaO和____________。
(4)下列溶液中,同样能用于“捕捉”二氧化碳的是____________。
A.KNO3溶液 B.CaCl2溶液 C.CuSO4溶液 D.Na2CO3溶液
(5)“捕捉”到的二氧化碳,一部分可以用于生产;一部分则设想注入深海中“封存”起来。但过多的二氧化碳会导致海水水质的变化,最终殃及海洋生物,其原因是_____(用化学方程式表示)。
【答案】生石灰 CaCO3![]() CaO+CO2 不是 增大反应物的接触面积(或提高反应速率;或提高吸收效率;或充分反应;或更好地、有效地吸收) 过滤 NaOH D CO2+H2O
CaO+CO2 不是 增大反应物的接触面积(或提高反应速率;或提高吸收效率;或充分反应;或更好地、有效地吸收) 过滤 NaOH D CO2+H2O![]() H2CO3或H2CO3
H2CO3或H2CO3![]() H++HCO3-
H++HCO3-
【解析】
方法Ⅰ:(1)CaO是生石灰的俗称。
(2)步骤二中发生碳酸钙的分解反应,该反应与步骤一中反应的温度分别为400℃和900℃。
方法Ⅱ:(1)NaOH溶液吸收二氧化碳气体时,只有相接触才能发生反应,喷成雾状是为了二者接触的充分。
(2)a环节中,是固体与液体物质发生分离。
(3)在整个流程中,循环利用的物质有CaO和氢氧化钠。
(4)能用于“捕捉”二氧化碳的是溶液应能与CO2反应。
(5)过多的二氧化碳会导致海水水质的变化,最终殃及海洋生物,其原因是二氧化碳溶于水后产生影响海洋生物生存环境的物质。
方法Ⅰ:(1)CaO俗称生石灰。答案为:生石灰;
(2)步骤二中发生碳酸钙的分解反应,方程式为CaCO3![]() CaO+CO2↑,该反应与步骤一中反应的温度不同,所以该反应不是步骤一中反应的逆反应。答案为:CaCO3
CaO+CO2↑,该反应与步骤一中反应的温度不同,所以该反应不是步骤一中反应的逆反应。答案为:CaCO3![]() CaO+CO2↑;不是;
CaO+CO2↑;不是;
方法Ⅱ:(1)NaOH溶液吸收二氧化碳气体时,只有相接触才能发生反应,喷成雾状是为了增大反应物的接触面积(或提高反应速率;或提高吸收效率;或充分反应;或更好地、有效地吸收)。答案为:增大反应物的接触面积(或提高反应速率;或提高吸收效率;或充分反应;或更好地、有效地吸收);
(2)a环节中,物质分离的基本操作是过滤。答案为:过滤;
(3)吸收CO2时发生反应CO2+2NaOH=Na2CO3+H2O,Na2CO3溶液中加入CaO后发生的反应为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,则在整个流程中,循环利用的物质有CaO和NaOH。答案为:NaOH;
(4)KNO3溶液、CaCl2溶液、CuSO4溶液与二氧化碳都不反应,只有Na2CO3溶液能吸收二氧化碳,发生反应为CO2+2NaOH=Na2CO3+H2O,所以能用于“捕捉”二氧化碳的是D。答案为:D;
(5)过多的二氧化碳会导致海水水质的变化,最终殃及海洋生物,其原因是二氧化碳溶于水后产生影响海洋生物生存环境的物质,反应方程式为CO2+H2O![]() H2CO3或H2CO3
H2CO3或H2CO3![]() H++HCO3-。答案为:CO2+H2O
H++HCO3-。答案为:CO2+H2O![]() H2CO3或H2CO3
H2CO3或H2CO3![]() H++HCO3-。
H++HCO3-。


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】有下列四种物质的溶液:①Na2CO3 ②Al2(SO4)3 ③CH3COOH ④NaHCO3。
(1)写出①溶液的电荷守恒:____________。
(2)常温下,0.1 mol·L-1④溶液的pH大于8,则溶液中c(H2CO3)_____c(CO32-)(填“>”、“=”或“<”),原因是_______(用离子方程式和必要的文字说明)。
(3)常温下0.1 mol/L的③溶液加水稀释过程中,下列表达式的数据一定变大的是_________。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
(4)用②和④的溶液可以制作泡沫灭火剂,其原理为:________________(用离子方程式解释)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸氨柔比星是临床主要用于治疗癌症的药物。F是合成盐酸氨柔比星的三种中间体之一,其合成路线如下:

⑴化合物D的分子式为C12H14O2,请写出D的结构简式:______。
⑵写出同时满足下列条件的B的一种同分异构体的结构简式:_____。
Ⅰ.能发生银镜反应,且能与FeCl3溶液发生显色反应;
Ⅱ.分子中含有4种不同化学环境的氢。
⑶请写出以 为原料制备
为原料制备![]() 的合成路线(无机试剂任选)。合成路线流程例见本题题干。____________________
的合成路线(无机试剂任选)。合成路线流程例见本题题干。____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(如图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,已知0-t1时,原电池的负极是Al片,反应过程中有红棕色气体产生。下列说法不正确的是

A. 0-t1时,正极的电极反应式为:2H++ NO3- - e-=NO2+ H2O
B. 0-t1时,溶液中的H+ 向Cu电极移动
C. t1时,负极的电极反应式为:Cu–2e-= Cu2+
D. t1时,原电池中电子流动方向发生改变是因为Al在浓硝酸中钝化,氧化膜阻碍了Al的进一步反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钾离子电池的工作原理如图所示,下列说法正确的是
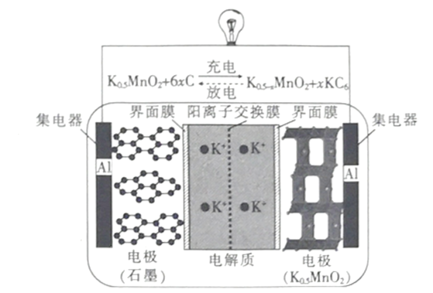
A.放电时,负极的电极反应式 :KC6 –e- =K ++6C
B.充电时,阳极的电极反应式 :K0.5-xMnO2+xK++ xe-=K0.5MnO2
C.放电时,K+ 通过阳离子交换膜向石墨电极移动
D.若仅把钾离子换成锂离子,当负极减少的质量相同时,钾离子电池转移的电子数比锂离子电池的多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年10月27日,国际清洁能源会议(ICCE2019)在北京开幕。一碳化学成为这次会议的重要议程。甲醇、甲醛(HCHO) 等一碳化合物在化工 、医药,能源等方面都有着广泛的应用。
(1)甲醇脱氢法可制备甲醛(反应体系中各物质均为气态),反应生成 1mol HCHO过程中能量变化如图1。

已知:CO2(g)+3H2(g)=CH3OH(g) +H2O(g) △H=-49.5kJ mo1-1,则反应CO2(g)+2H2(g)= HCHO(g) +H2O(g) △H= ___________kJ mo1-1。
(2)氧化剂可处理甲醛污染,结合图2分析春季(水温约为15℃)应急处理被甲醛污染的水源应选择的试剂为__________(填化学式)。

(3)纳米二氧化钛催化剂可用于工业上合成甲醇,CO2(g)+2H2(g)![]() CH3OH(g) △H=akJmo1-1
CH3OH(g) △H=akJmo1-1
①按![]() =2,投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应测定CO的平衡转化率与温度、压强的关系如图3所示。则a _____(填“>”或“<”)0;压强p1、p2、p3由小到大的关系是__________________。
=2,投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应测定CO的平衡转化率与温度、压强的关系如图3所示。则a _____(填“>”或“<”)0;压强p1、p2、p3由小到大的关系是__________________。

②在温度为T1℃,向某恒容密闭容器中充入 H2和CO发生上述反应,起始时c(H2)=c(CO)=2.0 mo1L-1。达到平衡时,CO的转化率为图3中的 M 点对应的转化率,则在该温度下,对应的N 点的平衡常数为__________(保留3 位有效数字)。
(4)工业上利用CH4(CO和H2)与水蒸气在一定条件下制取 H2:CH4(g) +H2O(g)![]() CO(g)+3H2(g) △H=+203kJmo1-1,该中反应的逆反应速率及表达式为v逆=kc(CO)c3(H2),k 为速率常数,在某温度下测得实验数据如表所示,
CO(g)+3H2(g) △H=+203kJmo1-1,该中反应的逆反应速率及表达式为v逆=kc(CO)c3(H2),k 为速率常数,在某温度下测得实验数据如表所示,
CO浓度(mo1L-1) | H2浓度(mo1L-1) | 逆反应速率(mo1L-1min-1) |
0.1 | c1 | 8.0 |
c2 | c1 | 16.0 |
c2 | 0.15 | 6.75 |
由上还数据可得该温度下,c2=____________,该反应的逆反应速率常数 k=______L3mo1-3min-1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示:
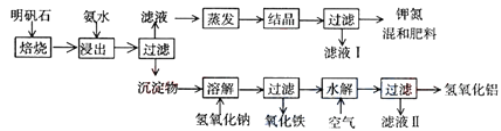
根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500mL稀氨水(每升含有39.20g氨)需要取浓氨水(每升含有251.28g氨)__________mL,用规格为_______mL量筒量取。
(2)写出溶解步骤中反应得到的溶质为_________________(写化学式)
(3)为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,请完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量______溶液,产生白色沉淀。
②___________、__________、_________(依次填写实验操作名称)。
③冷却、称重。
(4)若试样为mg,沉淀的物质的量为nmol,则试样中K2SO4的物质的量为:___________mol(用含有m、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示的实验装置制取乙酸乙酯。回答以下问题:
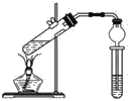
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是先向试管中加入一定量的________,然后边振荡边缓缓加入________,冷却后再加入一定量的________,轻轻振荡使之混合均匀。
(2)浓硫酸的作用是__________________________
(3)饱和碳酸钠溶液的作用是__________________________
(4)生成的乙酸乙酯,其密度比水________(填“大”或“小”),有________味。
(5)与书中采用的实验装置的不同之处是本实验采用了球形干燥管代替了长导管,并将干燥管的末端插入了饱和碳酸钠溶液中。在此处球形干燥管的作用有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二砷(As2O3)可用于治疗急性早幼粒白血病。利用某酸性含砷废水(含![]() 、H+、
、H+、![]() )可提取三氧化二砷,提取工艺流程如下:
)可提取三氧化二砷,提取工艺流程如下:
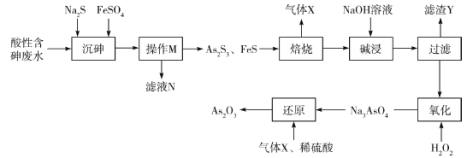
已知:①常温下,![]() ;
;![]() 。
。
②As2O3+6NaOH=2Na3AsO3+3H2O。
③As2S3易溶于过量的Na2S溶液中,故加入FeSO4的目的是除去过量的S2-。
回答下列问题:
(1)操作M的名称是________,滤液N中含有的阳离子有Fe2+、H+、________。
(2)“焙烧”操作中,As2S3参与反应的化学方程式为____________。
(3)“碱浸”的目的是_____________,“滤渣Y”的主要成分是_____________(写化学式)。
(4)“氧化”中发生反应的离子方程式为___________________。
(5)该流程中可循环使用的物质是_________(写化学式),某次“还原”过程中制得了1.98kgAs2O3,则消耗标准状况下该物质的体积是________L。
(6)溶液中金属离子的除去方法之一是Na2S沉降法。常温下,若某溶液中含Fe2+、Ag+,且浓度均为0.1mol·L-1,则向该溶液中滴加稀Na2S溶液时,先生成的沉淀是________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com