
【题目】工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素。霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾。
(1)NOx和SO2在空气中存在下列平衡:
2NO(g)+ O2(g) 2NO2(g) △H= -112 kJ·mol-1,
2SO2(g)+ O2 (g) 2SO3(g) △H= -196 kJ·mol-1;
SO2通常在NO2的存在下,进一步被氧化,生成SO3。写出NO2和SO2反应的热化学方程式为________________________________。
(2)烟气中的SO2可以用NaOH溶液吸收,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示。(电极材料为石墨)

①图中a极要连接电源的_______(填“正”或“负”)极,C口流出的物质是_______。
②SO32-放电的电极反应式为_____________________________________。
(3)常温下,烟气中SO2被NaOH溶液吸收可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是_____________________________________(写出主要反应的离子方程式),该溶液中c(Na+)_________ 2c(SO32-)+ c(HSO3-)(填“>”“<”或“=”);
②常温下,0.1mol/L的NaHSO3溶液的pH=6,则c(SO32-)- c(H2SO3)= _________ mol/L(填写准确数值)。
【答案】 NO2(g)+SO2(g)SO3(g)+ NO(g)△H= -42 kJmol-1 负 硫酸 SO32--2e- + H2O =SO42-+ 2H+ SO32- + H2O HSO3- + OH - > 9.9×10-7
【解析】(1)根据盖斯定律来求解,正反应如果是吸热反应,温度越高K值越大;
(2)在图中由于Na+向a极区域移动,根据同种电荷相互排斥,异种电荷相互吸引的原则,a要连接电源的负极,b要连接电源的正极,在阳极上SO32-变为SO42-;
(3)①溶液中SO32-水解,导致溶液显碱性,然后根据电荷守恒分析;②常温下,亚硫酸氢钠呈酸性,说明亚硫酸氢根离子的电离程度大于水解程度,根据物料守恒和电荷守恒计算。
(1)①根据盖斯定律来求解,2NO(g)+O2(g)2NO2(g)△H=-112kJmol-1 ①;2SO2(g)+O2(g)2SO3(g)△H=-196kJmol-1②,根据盖斯定律,将(②-①)÷2得:NO2(g)+SO2(g)=SO3(g)+NO(g)△H=-42kJmol-1,故答案为:NO2(g)+SO2(g)=SO3(g)+NO(g) △H=-42 kJmol-1;
(2)①在图中由于Na+向a极区域移动,根据同种电荷相互排斥,异种电荷相互吸引的原则,a要连接电源的负极,b要连接电源的正极,在阳极上SO32-变为SO42-,C口流出的物质是硫酸,故答案为:负;硫酸;
②在阳极上SO32-变为SO42-,SO32-放电的电极反应式为:SO32-+H2O=SO42-+2H+,故答案为:SO32-+H2O=SO42-+2H+;
(3)①溶液中SO32-水解:SO32-+H2OHSO3-+OH-,破坏水的电离平衡,导致溶液显碱性,根据电荷守恒,溶液中c(H+)+c(Na+)=2c(SO32-)+c(HSO3-)+c(OH-),因为c(H+)<c(OH-),故c(Na+)>2c(SO32-)+c(HSO3-),故答案为:SO32-+H2OHSO3-+OH-;>;
②常温下,亚硫酸氢钠呈酸性,说明亚硫酸氢根离子的电离程度大于水解程度,根据物料守恒得c(Na+)=c(H2SO3)+c(HSO3-)+c(SO32-)①,根据电荷守恒得c(Na+)+c(H+) =c(OH-)+c(HSO3-)+2c(SO32-)②,将方程式①代入②得,c(H2SO3)+c(H+) =c(OH-)+c(SO32-),所以c(SO32-)-c(H2SO3)=c(H+)-c(OH-)=(10-6-10-8)molL-1 =9.9×10-7molL-1,故答案为:9.9×10-7mol。


科目:高中化学 来源: 题型:
【题目】如下图甲、乙两个容器中,分别加入0.1 mol·L-1的NaCl溶液与0.1 mol·L-1的AgNO3溶液后,以Pt为电极进行电解时,在A、B、C、D各电极上生成物的物质的量之比为( )
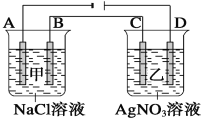
A. 2∶2∶4∶1
B. 2∶3∶4∶1
C. 1∶4∶2∶2
D. 1∶1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘循环工艺不仅能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下:

下列说法正确的是
A. 分离器中的物质分离操作为过滤
B. 膜反应器中,增大压强有利于提高HI的分解速率和平衡转化率
C. 该工艺中I2和HI的相互转化体现了“碘循环”
D. 碘循环工艺的总反应为2SO2+4H2O+I2 == H2+2H2SO4+ 2HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 用碳酸氢钠溶液检验水杨酸中的羧基: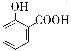 +2HCO3-→
+2HCO3-→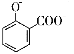 +2H2O+2CO2↑
+2H2O+2CO2↑
B. 在NaHCO3溶液中加入过量Ba(OH)2溶液:HCO3—+Ba2++OH—= BaCO3↓+H2O
C. 向Mg(HCO3)2溶液中加入过量NaOH溶液,产生白色沉淀:Mg2++2HCO3-+2OH- = MgCO3↓+2H2O
D. 用高锰酸钾溶液滴定草酸:2MnO4-+16H++5C2O42- = 2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无机化合物的二聚分子结构如图,该分子中A、B两种元素都是第三周期的元素,分子中所有原子最外层都达到8电子稳定结构。关于该化合物的说法不正确的是( )
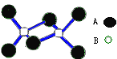
A. 化学式是Al2Cl6
B. 不存在离子键和非极性共价键
C. 在固态时所形成的晶体是分子晶体
D. 是离子化合物,在熔融状态下能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
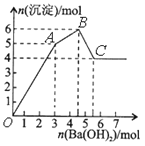
【题目】向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成的pH列于下表(已知:偏铝酸钡易溶于水)。以下推断正确的是
氢氧化物 | 溶液pH | |
开始沉淀 | 沉淀完全 | |
Fe(OH)3 | 2.3 | 3.4 |
Al(OH)3 | 3.3 | 5.2 |
A. OA段产生的沉淀为BaSO4和Fe(OH)3
B. 据图计算原溶液中c(Cl-)=c(SO42-)
C. AB段可能发生的反应是:2SO42-+ 2Ba2++ Al3++3OH-=2BaSO4↓+Al(OH)3↓
D. C点溶液呈碱性是因为AlO2-水解,离子方程式为:AlO2-+2H2O=Al(OH)3+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1,Na2O2(s)+CO2(g)===Na2CO3(s)+![]() O2(g) ΔH=-226 kJ·mol-1,根据以上热化学方程式判断,下列说法正确的是( )。
O2(g) ΔH=-226 kJ·mol-1,根据以上热化学方程式判断,下列说法正确的是( )。
A. CO的燃烧热为283 kJ
B. 下图可表示由CO生成CO2的反应过程和能量关系
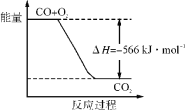
C. 2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-452 kJ·mol-1
D. CO(g)与Na2O2(s)反应放出509 kJ热量时,转移电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A.硫是一种不溶于水的淡黄色固体
B.硫与金属反应时作氧化剂,与非金属反应时作还原剂
C.硫与铁反应时生成硫化铁
D.硫在自然界中仅以化合态存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com