
����Ŀ��ú����Ҫ����Դ��Ҳ������������Ʒ����Ҫԭ�ϡ�������ѧ֪ʶ������������⣺
(1)ú��ת����������ú������������Һ��������ú��Һ�������ַ�Ϊ________��________��
(2)��úȼ��ǰ���ú������������ú��ij����������ԭ��ΪFeS2![]() Fe2����SO42��
Fe2����SO42��![]() Fe3��������������Ϊ�������������ü����ĵ�һ����Ӧ�����ӷ���ʽΪ_______________________���ڶ�����Ӧ�����ӷ���ʽΪ________________��
Fe3��������������Ϊ�������������ü����ĵ�һ����Ӧ�����ӷ���ʽΪ_______________________���ڶ�����Ӧ�����ӷ���ʽΪ________________��
(3)��ҵú����õ��IJ�Ʒ�н�̿��________��
(4)��ҵ����Ҫ���ð��������������ᣬ��ͼ�ǰ��������백������������������ȵĹ�ϵ������ֱ�߱�ʾ��Ӧ������ֵ�����߱�ʾ����ʵ����������������ʴﵽ100%��������r[n(O2)/n(NH3)]��________��ʵ������Ҫ��rֵά����1.7��2.2֮�䣬ԭ����__________________________________________��
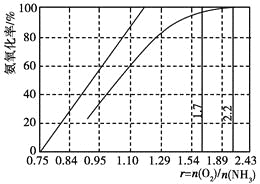
���𰸡�ֱ��Һ������ ���Һ������ 2FeS2��7O2��2H2O![]() 4H����2Fe2����4SO42�� 4Fe2����O2��4H��
4H����2Fe2����4SO42�� 4Fe2����O2��4H��![]() 4Fe3����2H2O ��¯ú�����ְ�ˮ��ú���� 1.25 O2̫�ٲ�����NH3��ת����rֵΪ2.2ʱNH3�������ѽ�100%
4Fe3����2H2O ��¯ú�����ְ�ˮ��ú���� 1.25 O2̫�ٲ�����NH3��ת����rֵΪ2.2ʱNH3�������ѽ�100%
��������
(1)ú��Һ����ֱ��Һ���ͼ��Һ����
(2)�ڵ�һ��ΪFeS2�����������±���������������Fe2����SO42�����ڶ���ΪFe2������������ΪFe3����
(3)��ҵú����õ��IJ�Ʒ�н�̿����¯ú�����ְ�ˮ��ú���͡�
(4)���ݷ�Ӧ����ʽ����r[n(O2)/n(NH3)]������ֵ������ʵ����������ҵ��rֵά����1.7��2.2֮���ԭ��
(1)ú��Һ����ֱ��Һ���ͼ��Һ�����ʴ�Ϊֱ��Һ�����������Һ��������
(2)�ڵ�һ��ΪFeS2�����������±���������������Fe2����SO42�����ڶ���ΪFe2������������ΪFe3�����ʴ�Ϊ2FeS2��7O2��2H2O![]() 4H����2Fe2����4SO42����4Fe2����O2��4H��
4H����2Fe2����4SO42����4Fe2����O2��4H��![]() 4Fe3����2H2O��
4Fe3����2H2O��
(3)��ҵú����õ��IJ�Ʒ�н�̿����¯ú�����ְ�ˮ��ú���͡�
(4)���ݷ�Ӧ����ʽ��֪�����������Ʊ�����ʱ�ķ�Ӧ��4NH3��5O2=4NO��6H2O���ʵ��������ʴﵽ100%��������n(O2)/n(NH3)��5/4��1.25��ʵ��������Ҫ��������ֵά����1.7��2.2֮�䣬ԭ����O2̫�ٲ�����NH3��ת�������Ҷ�ͼ��֪����ֵΪ2.2ʱNH3�������ѽ�100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�CH3COOH��NH3��H2O�ĵ��볣����Ϊ1.8��10��5����20 mLŨ�Ⱦ�Ϊ0.1 mol/L NaOH��NH3��H2O�Ļ��Һ�еμӵ����ʵ���Ũ�ȵ�CH3COOH��Һ�����û��Һ�ĵ����������CH3COOH��Һ�������V���Ĺ�ϵ��ͼ��ʾ������˵������ȷ����

A. a=20��b=40������Һ�����Դ���A��B����֮��
B. B����Һ�У�c(CH3COO��)��c(Na��)��c(NH![]() ��
��
C. ��֪lg3��0.5����C���pH��5
D. A��B��C�����У�B����Һ��ˮ�ĵ���̶����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���10 mL0.1 mol/L��HR��Һ����μ���0.1 mol/L�İ�ˮ��������ҺpH�����������仯��ͼ�����з�����ȷ���ǣ� ��

A. ������Һ�е�����Ũ���ܺʹ�С��ϵ��d>c > b > a
B. ������,R-��ˮ��ƽ�ⳣ��������Ϊ10 -9
C. a���b����Һ�У�ˮ�ĵ���̶����
D. d�����Һ��,��Ũ�ȹ�ϵ��c(R-)+2c(HR)=c(NH3H2O)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪һ���¶���CuS���ܶȻ�����Ϊ4.0��10��36���ֽ�0.1 mol CuSO4����100 mL 1.0 mol��L��1Na2S��Һ�У���ֽ��跴Ӧ(��������Һ����仯)��������˵������ȷ����(����)
A.��Ӧ����Һ��pH�ȷ�Ӧǰ��Һ��pHС
B.��Ӧ����Һ�в�����Cu2����S2��
C.��Ӧ����Һ��c(Cu2��)��c(S2��)��ԼΪ2.0��10��16mol��L��1
D.����CuSˮ��Һ�м���Na2S��Һ��Ksp(CuS)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Fe(OH)3��Ksp��2.79��10��39��Al(OH)3��Ksp��1.3��10��31���ֽ�20 mL 0.05 mol/L FeCl3��20 mL 0.05 mol/L AlCl3��ϣ�������Һ����μ���0.10 mol/L NaOH��Һ���ⶨ��Һ��pH�仯��ͼ��ʾ��������˵������ȷ����(����)
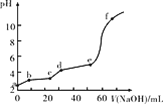
A.a�㴦��Al3��ˮ��̶ȱ�Fe3��ˮ��̶ȴ�
B.bc����Ҫ����Fe(OH)3����
C.de����Ҫ��Ӧ��Al3����3OH��=Al(OH)3��
D.��f��������Һ��ͨ������CO2����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��F�Ǽ�ͥ�г������л��E��ʯ�ͻ�����չˮƽ�ı�־��F��һ�ֳ����ĸ߷��Ӳ��ϡ���������ת����ϵ�ش��������⣺

(1)�����ޡ������ߵ����Ʒֱ�Ϊ________��________��
(2)���������зе���ߵ���________��
A ���� B ú��
C ���� D ����
(3)�ڢ١���������ȡ����Ӧ����________��ԭ��������Ϊ100%�ķ�Ӧ��________��(�����)
(4)д���ṹ��ʽ��A________��F________��
(5)д����Ӧ�۵����ӷ���ʽ��___________��
(6)��Ϊ��ͥ�г���������F���������Ǵ����˼���ķ��㣬ͬʱҲ����˻�����Ⱦ��������Ⱦ��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ij��Ԫ��H2XO4��ˮ�е����������H2XO4=H++HXO4-��HXO4-![]() H++XO42-�������£���20mL0.1molL-1NaHXO4��Һ�еμ�cmolL-1NaOH��Һ����Һ�¶�����Һ�����ϵ��ͼ��ʾ������˵��������ǣ� ��
H++XO42-�������£���20mL0.1molL-1NaHXO4��Һ�еμ�cmolL-1NaOH��Һ����Һ�¶�����Һ�����ϵ��ͼ��ʾ������˵��������ǣ� ��
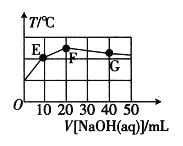
A.��NaOH��Һ��pH=13
B.�μӹ����У�ˮ�ĵ���̶��ȱ���С
C.F����Һ��c(OH-)>c(HXO4-)
D.G����Һ��c(Na+)=3c(H2XO4)+3c(HXO4-)+3c(XO42-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ���У�a��b���Ƕ��Ե缫��ͨ��һ��ʱ���b��������Һ����ɫ������˵���в���ȷ����( )
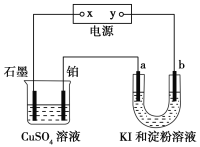
A��x��������y�Ǹ��� B��a������������b������I2
C��a����Pt�缫�������ݲ��� D��U�ι�����Һ�ļ�����ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.ijС����CoCl2��6H2O���������⡢Һ�����Ȼ�粒���Ϊԭ�ϣ��ڻ���̿���£��ϳ��˳Ȼ�ɫ����X��Ϊȷ������ɣ���������ʵ�飺
�ٰ��IJⶨ����ȷ��ȡwgX��������ˮ�ܽ⣬ע��Բ����ƿ�У�Ȼ����μ�������10%NaOH��Һ��ͨ��ˮ����������Ʒ��Һ�еİ�ȫ����������V1mL c1mol��L-1��������Һ���ա�����������ȡ�½���ƿ����c2mol��L-1 NaOH����Һ�ζ���ʣ��HCl�����յ�ʱ����V2mLNaOH��Һ��
���ȵIJⶨ��ȷ��ȡ��ƷX�����Һ����AgNO3����Һ�ζ���K2CrO4��ҺΪָʾ����������ש��ɫ����������ʧΪ�յ㣨Ag2CrO4Ϊש��ɫ����
�ش��������⣺
��1����NaOH����Һ�ζ���ʣ��HClʱ��Ӧʹ��___ʽ�ζ��ܣ��õζ�ʵ���ʹ�õ�ָʾ��Ϊ___���ﵽ�ζ��յ������Ϊ___��
��2����Ʒ�а���������������ʽΪ___��
��3���ζ��յ�ʱ������Һ��c(Ag+)=2.0��10-5mol��L-1 ��c(CrO42-)Ϊ___mol��L-1������֪��Ksp(Ag2CrO4)=1.12��10-12����
��.��֪
������ | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp����ֵ | 10-17 | 10-17 | 10-39 |
��4�����÷ϵ�ص�пƤ������ˮ������п����ȥ���������������䷽���ǣ�����ϡ�����˫��ˮ���ܽ⣬����Ϊ___����___����pHΪ___��������λ��Ч���֣������պ���ȫ����������Ũ��С��1��10-5mol/Lʱ��������Ϊ�����ӳ�����ȫ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com