
【题目】类比![]() 比较
比较![]() 是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观实际。下列说法正确的是
是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观实际。下列说法正确的是![]()
A.![]() 能水解:
能水解:![]() ,则
,则![]() 也能水解:
也能水解:![]()
B.![]() 与Cu加热反应生成CuO,则S与Cu加热反应生成CuS
与Cu加热反应生成CuO,则S与Cu加热反应生成CuS
C.根据化合价![]() 可表示为
可表示为![]() ,则
,则![]() 也可表示为
也可表示为![]()
D.![]() 通入
通入![]() 溶液中不产生沉淀,则
溶液中不产生沉淀,则![]() 通入
通入![]() 溶液中也不产生沉淀
溶液中也不产生沉淀
科目:高中化学 来源: 题型:
【题目】锌是一种常用金属,工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO 等)湿法制取金属锌的流程如图所示,回答下列问题。

已知:Fe的活泼性强于Ni。
(1)ZnFe2O4可写成ZnOFe2O3,则ZnFe2O4与H2SO4反应的化学方程式___。
(2)“净化Ⅰ”操作分为两步:
①将溶液中少量的 Fe2+氧化,下列试剂中可选用的是_____(填字母标号)。
A.新制氯水 B.30 % H2O2溶液 C.FeC13溶液 D.KMnO4溶液
②加入ZnO,调节溶液pH为3.3~6.7;加热到60℃左右并不断搅拌,加热搅拌主要目的是___。
(3)“净化Ⅰ”生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是____。
(4)“净化Ⅱ”中加入过量Zn的目的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1 mol·L-1 NaOH溶液滴定40 mL 0.1 mol·L-1 H2SO3溶液,所得滴定曲线如图所示(忽略混合时溶液体积的变化)。下列叙述错误的是( )
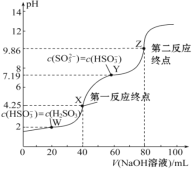
A. Ka2(H2SO3)的数量级为10-8
B. 若滴定到第一反应终点,可用甲基橙作指示剂
C. 图中Z点对应的溶液中:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)
D. 图中Y点对应的溶液中:3c(SO32-)=c(Na+)+c(H+)-c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种元素,已知:
①它们位于三个不同短周期,核电荷数依次增大
②E元素的电离能数据见下表(kJ·mol-1):
I1 | I2 | I3 | I4 | … |
496 | 4562 | 6912 | 9540 | … |
③B与F分别同主族
④A、E分别都能与D按原子个数比1﹕1或2﹕l形成化合物
⑤B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学式_____________、______________
(2)B2A2分子中存在____个σ键,____个π键
(3)E2D2电子式____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(s,mol·L-1)见右图。

(1)pH=3时溶液中铜元素的主要存在形式是:________(化学式)
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,___ (能、不能)通过调节溶液pH的方法来除去,理由是_________。
(4)已知一些难溶物的溶度积常数如下表。
物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的_______除去它们。
A.NaOH B.FeS C.Na2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写正确且对应的△H的数值和意义与括号内表述相符的是( )
A. 2H2 (g) + O2 (g) = 2H2O (l) ΔH=-571.6 kJ/mol(燃烧热)
B. NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l);△H=-57.3kJ/mol(中和热)
C. H2O(g)=H2(g)+1/2 O2(g) ΔH=-242 kJ/mol (反应热)
D. C(s)+ O2 ( g )=CO2(g) ΔH=-393.5 kJ/mol(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烧杯中盛有含0.2 mol NH4Al(SO4)2的溶液,向其中缓缓加入4 mol·L-1的NaOH溶液200 mL,使其充分反应,此时烧杯中铝元素的存在形式为( )
A. Al3+和Al(OH)3 B. AlO2— C. AlO2—和Al(OH)3 D. Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是
A.石油、天然气和煤等化石能源都是一次能源
B.氢能是一种理想的绿色能源,现在的科学技术水平已经那个全面推广使用氢能
C.开发太阳能、水能、风能等新能源,减少使用有害物质对环境的污染
D.2CO(g)+O2(g) ![]() 2CO2(g) ΔH=-566kJ·mol-1 ,CO的燃烧热为283kJ·mol-1
2CO2(g) ΔH=-566kJ·mol-1 ,CO的燃烧热为283kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a g Fe、Mg合金溶解在一定量的稀硝酸中,当合金完全溶解后,收集到标准状况下的NO气体b L(设HNO3的还原产物只有NO)。再向反应后的溶液中加入足量NaOH溶液,得到沉淀物。若用守恒法求沉淀的质量,用到的守恒关系依次是
A. 质量守恒、电子守恒、电荷守恒 B. 电子守恒、质量守恒、电荷守恒
C. 电子守恒、电荷守恒、质量守恒 D. 电荷守恒、质量守恒、电子守恒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com