
【题目】1.92g铜投入一定量的浓硝酸中,铜完全溶解,生成的气体颜色越来越浅,共收集到标况下672mL气体。将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2恰好使气体完全溶于水中,则通入的O2的体积是( )
A.336mLB.168mLC.224mLD.112mL
【答案】A
【解析】
根据电子守恒计算,已知HNO3![]() NO、NO2
NO、NO2![]() HNO3,反应前后HNO3的物质的量不变,而化合价变化的只有铜和氧气,则Cu失去电子数目等于O2得到电子的数目,以此进行计算。
HNO3,反应前后HNO3的物质的量不变,而化合价变化的只有铜和氧气,则Cu失去电子数目等于O2得到电子的数目,以此进行计算。
1.92g Cu的物质的量为n(Cu)=![]() =0.03mol,反应时失去电子数目为2×0.03mol=0.06mol,由反应整个过程为HNO3
=0.03mol,反应时失去电子数目为2×0.03mol=0.06mol,由反应整个过程为HNO3![]() NO、NO2
NO、NO2![]() HNO3可知,反应前后HNO3的物质的量不变,而化合价变化的只有铜和氧气,则Cu失去电子数目等于O2得到电子的数目,所以消耗氧气的物质的量为n(O2)=
HNO3可知,反应前后HNO3的物质的量不变,而化合价变化的只有铜和氧气,则Cu失去电子数目等于O2得到电子的数目,所以消耗氧气的物质的量为n(O2)=![]() =0.015mol,V(O2)=0.015mol×22400mL/mol=336mL,所以通入O2的体积为336mL。
=0.015mol,V(O2)=0.015mol×22400mL/mol=336mL,所以通入O2的体积为336mL。
答案选A。


科目:高中化学 来源: 题型:
【题目】将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,各物质浓度随时间变化的关系如图所示:

计算该反应的平衡常数K=________。反应进行到20 min时,再向容器内充入一定量NO2,10 min后达到新的平衡,此时测得c(NO2)=0.9 mol·L-1。第一次平衡时混合气体中NO2的体积分数为w1,达到新平衡后混合气体中NO2的体积分数为w2,则w1________w2(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氮存在下列平衡2NO2 (g) ![]() N2O4(g);△H<0。在测定NO2 相对分子质量时,下列条件中较为适宜的是
N2O4(g);△H<0。在测定NO2 相对分子质量时,下列条件中较为适宜的是
A.温度130℃,压强3.03×105paB.温度25℃, 压强1.01×105pa
C.温度130℃,压强5.05×104paD.温度0℃, 压强5.05×104pa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知某溶液中只有Na+、CH3COO、H+、OH四种离子。某同学推测该溶液中离子浓度可能有如下四种关系:
A.c(Na+)>c(CH3COO)>c(OH)>c(H+) B.c(Na+)>c(CH3COO)>c(H+)>c(OH)
C.c(Na+)>c(OH)>c(CH3COO)>c(H+) D.c(CH3COO)>c(Na+)>c(H+)>c(OH)
①若溶液中只溶解了一种溶质,该溶质的名称是_________,上述离子浓度大小关系中正确的是(填序号)_____。
②若上述关系中D是正确的,则溶液中溶质的化学式是________。
③若该溶液由体积相等的醋酸与NaOH溶液混合而成,且溶液恰好呈中性,则混合前c(CH3COOH)(填“>”“<”“=”,下同)___________c(NaOH),混合后c(CH3COO)与c(Na+)的关系是c(CH3COO)__________c(Na+)。
(2)Na2S可用于制造硫化染料、沉淀水体中的重金属等。
①Na2S溶液中S2水解的离子方程式为____________________________________。
金属硫化物 | FeS | PbS | CuS | HgS |
Ksp | 6.3×1018 | 1.0×1028 | 6.3×1036 | 1.6×1052 |
②室温时,几种重金属离子的硫化物的溶度积常数如下表:
则:向物质的量浓度相同的Fe2+、Pb2+、Cu2+、Hg2+的混合稀溶液中,逐滴加入Na2S稀溶液,首先沉淀的离子是____;用Na2S溶液沉淀废水中Pb2+,为使Pb2+沉淀完全[c(Pb2+)≤1×106mol/L],则应满足溶液中c(S2)≥_____mol/L;反应Cu2+(aq)+FeS(s) ![]() Fe2+(aq)+CuS(s)的平衡常数K=_______。
Fe2+(aq)+CuS(s)的平衡常数K=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ/mol
1molCO和3molCH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
A.2912kJB.2953kJC.3236kJD.3867kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设X、Y、Z代表3种短周期元素,已知:
①Ym-和Zn-两种离子是有相同的电子层结构
②X与Y可以形成原子个数比为1:1的化合物甲和2:1的化合物乙,甲、乙都是共价化合物
③X与Z形成原子个数比为1:1的化合物丙,其分子与乙的分子所含质子数相同。据此,填写下面空白:
(1)Ym-的离子结构示意图为_________,Z元素是___________
(2)化合物甲的电子式是____________
(3)Z单质与化合物乙反应的化学方程式是________________
(4)化合物丙与氢氧化钠溶液反应的离子方程式是_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是温度和压强对X+Y![]() 2Z反应影响的示意图。图中横坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是 ( )
2Z反应影响的示意图。图中横坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是 ( )
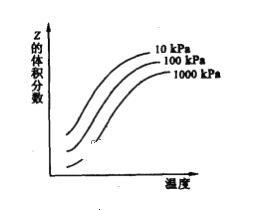
A.X、Y、Z均为气态
B.X和Y中只有一种为气态,Z为气态
C.上述该反应的正反应为放热反应
D.上述反应的逆反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①101kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1
③H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
④H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1
下列结论正确的是( )
A.碳的燃烧热大于110.5kJ·mol-1
B.浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3kJ 热量
C.氢气的燃烧热为241.8kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)的反应热为ΔH=571.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与金属腐蚀有关的说法正确的是( )
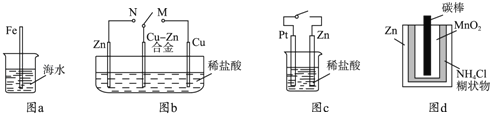
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu﹣Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn﹣MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com