
| A、1molCl2参加的任何反应转移电子数都是2NA |
| B、1mol/L的NaCl溶液中含有NA个Na+ |
| C、标准状况下,22.4ml水中含有的分子数约为1.24NA |
| D、1molFeCl3完全水解生成NA个胶体粒子 |
| m |
| M |
| 22.4g |
| 18g/mol |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、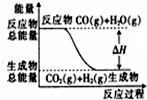 表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”中的△H>0 |
B、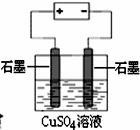 为电解硫酸铜溶液的装置,电解前后溶液的pH几乎不变 |
C、 实验装置可完成比较乙酸、碳酸、硅酸酸性强弱的实验 |
D、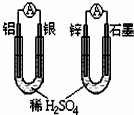 两个装置通过的电量相等时,消耗负极材料的物质的量也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4Cl═NH3↑+HCl↑ |
| B、NH3+CO2+H2O═NH4HCO3 |
| C、2NaOH+Cl2═NaCl+NaClO+H2O |
| D、2Na2O2+2 CO2═2Na2 CO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同周期相邻主族的两元素原子序数均相差1 |
| B、原子最外层有2个电子的元素一定是金属元素 |
| C、第ⅦA族元素从上到下,其氢化物的酸性逐渐增强 |
| D、同主族元素从上到下,单质的熔点逐渐降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
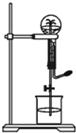 喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?
喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molN2所含分子数约为6.02×1023 |
| B、58.5g NaCl所含离子数约为6.02×1023 |
| C、标准状况下,22.4L H2所含原子数约为6.02×1023 |
| D、常温常压下,分子总数约为6.02×1023的SO2的质量是64 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.03mol/L |
| B、0.3mol/L |
| C、0.05mol/L |
| D、0.04mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
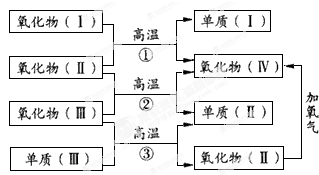
查看答案和解析>>
科目:高中化学 来源: 题型:
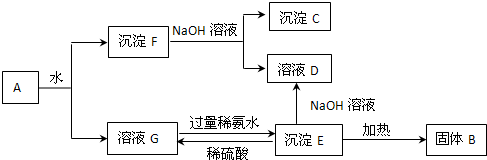
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com