
【题目】设![]() 代表阿伏加德罗常数,下列说法正确的是
代表阿伏加德罗常数,下列说法正确的是 ![]()
![]()
A.![]() 中,生成
中,生成![]() 标准状况
标准状况![]() 转移电子数为
转移电子数为![]()
B.56gFe与一定量的稀硝酸反应,转移电子数可能为![]()
C.足量的![]() 与一定量的浓盐酸反应得到
与一定量的浓盐酸反应得到![]() ,若向反应后的溶液中加入足量的
,若向反应后的溶液中加入足量的![]() ,则生成AgCl的物质的量为2mol
,则生成AgCl的物质的量为2mol
D.标准状况下,![]() 和
和![]() 混合后,原子总数小于
混合后,原子总数小于![]()
【答案】B
【解析】
A.反应![]() 转移5mol电子,生成3mol氯气,故当生成
转移5mol电子,生成3mol氯气,故当生成![]() 氯气即
氯气即![]() 氯气时,反应转移的电子的物质的量为1mol,即
氯气时,反应转移的电子的物质的量为1mol,即![]() 个,故A错误;
个,故A错误;
B.56g铁的物质的量为1mol,而铁和硝酸反应后最终可能变为![]() 价,也可能变为
价,也可能变为![]() 价,故1mol铁反应后转移的电子数介于
价,故1mol铁反应后转移的电子数介于![]() 到
到![]() 之间,故可能为
之间,故可能为![]() 个,故B正确;
个,故B正确;
C.二氧化锰只能与浓盐酸反应,和稀盐酸不反应,故浓盐酸不能反应完全,且由于浓盐酸的物质的量未知,故反应后的溶液中的溶液中氯离子的物质的量无法确定,则生成的氯化银的物质的量无法确定,故C错误;
D.标准状况下,![]() NO和
NO和![]()
![]() 的物质的量均为
的物质的量均为![]() ,且两者均为双原子分子,故共含
,且两者均为双原子分子,故共含![]() 个原子,而反应满足原子个数守恒,故反应后体系中原子数仍为
个原子,而反应满足原子个数守恒,故反应后体系中原子数仍为![]() 个,故D错误;
个,故D错误;
故答案为B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】现有室温下溶质浓度均为![]() 的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
(1)在④溶液中,各离子浓度大小顺序为:____________
(2)将③、⑥混合后,若溶液呈现中性,则消耗量溶液的体积为③____________⑥(填“>”、“=”或“<”),溶液中的离子浓度由大到小的顺序为____________
(3)在常温下,将100mL的②与100mL的⑥溶液混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=____________(已知![]() )
)
(4)在常温下,六种液体的pH由大到小的顺序是____________
(5)若将③溶液和⑥溶液按体积比2:1混合后溶液呈酸性,则混合后溶液中![]() __________
__________![]() (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
(6)常温下将③溶液加水稀释过程中,下列表达式的数据一定变大的是______
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中处处有化学,下列有关说法正确的是( )
A.草木灰与铵态氮肥不能混合施用与盐类水解有关
B.焊接时用NH4Cl溶液除锈与盐类水解无关
C.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂
D.生活中Cl2和NaOH制取消毒液,运用了盐类的水解原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
![]() 与镍反应会造成含镍催化剂的中毒。为防止镍催化剂中毒,工业上常用
与镍反应会造成含镍催化剂的中毒。为防止镍催化剂中毒,工业上常用![]() 将CO氧化,二氧化硫转化为单质硫。
将CO氧化,二氧化硫转化为单质硫。
已知:![]()
![]()
![]()
![]()
![]()
则![]() ______
______![]() ;
;
![]() 时,在2L密闭容器中发生可逆反应:
时,在2L密闭容器中发生可逆反应:![]()
![]()
![]() ,
,![]() 的物质的量浓度随时间变化如图所示。达平衡时,
的物质的量浓度随时间变化如图所示。达平衡时,![]() 的浓度为
的浓度为![]() 的2倍,回答下列问题。
的2倍,回答下列问题。

![]() 时,该反应的平衡常数为
时,该反应的平衡常数为![]() 精确到小数点后两位
精确到小数点后两位![]() ______。
______。
![]() 在温度为
在温度为![]() 、
、![]() 时,平衡体系中
时,平衡体系中![]() 的体积分数随压强变化曲线如图所示。
的体积分数随压强变化曲线如图所示。

下列说法正确的是______
![]() 、C
、C![]()
![]() 、C两点气体的颜色:A深,C浅
、C两点气体的颜色:A深,C浅
![]() 由状态B到状态A,可以用加热的方法
由状态B到状态A,可以用加热的方法
![]() 若反应在398K进行,某时刻测得
若反应在398K进行,某时刻测得![]() ,
,![]() ,则此时
,则此时![]() ______
______![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]()
![]() 在分析试剂、电子工业中用途广泛。现向100mL
在分析试剂、电子工业中用途广泛。现向100mL![]() 溶液中滴加
溶液中滴加![]() 溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,
溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,

![]() 水的电离程度最大的是______;
水的电离程度最大的是______;
![]() 其溶液中
其溶液中![]() 的数值最接近
的数值最接近![]() 的电离常数K数值的是______。
的电离常数K数值的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增加。A、B、C、D均是由这些元素组成的二元化合物,甲是Y的固体单质,常温下0.05mol/L乙溶液的pH为1。A是无色气体,是主要的大气污染物之一,上述物质的转化关系如图所示。下列说法错误的是( )
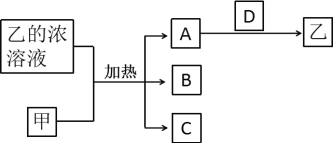
A.原子半径:X<Z<W
B.D中存在极性键和非极性键
C.最高价含氧酸的酸性:W>Y
D.化合物YZW中键角为120°
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2O=H++OH-,下列叙述正确的是( )
A.![]() 表示的粒子不会对水的电离平衡产生影响
表示的粒子不会对水的电离平衡产生影响
B.![]() 表示的物质加入水中,促进水的电离,c(H+)增大
表示的物质加入水中,促进水的电离,c(H+)增大
C.25℃时,CH3COO-加入水中,促进水的电离,Kw不变
D.水的电离程度只与温度有关,温度越高,电离程度越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C和CuO在高温下反应可能生成Cu、![]() 、
、![]() 、CO。现将
、CO。现将![]() 碳粉跟
碳粉跟![]() 混合,在硬质试管中隔绝空气高温加热,将生成的气体全部通入足量NaOH溶液中,并收集残余的气体,测得溶液增加的质量为
混合,在硬质试管中隔绝空气高温加热,将生成的气体全部通入足量NaOH溶液中,并收集残余的气体,测得溶液增加的质量为![]() ,残余气体在标准状况下的体积为
,残余气体在标准状况下的体积为![]() 。下列说法不正确的是
。下列说法不正确的是
A.在硬质试管中隔绝空气高温加热固体混合物时,有![]() 碳参加了反应
碳参加了反应
B.试管中发生的所有氧化还原反应共转移电子![]()
C.反应后试管中剩余的固体混合物的总质量为![]()
D.反应生成铜和氧化亚铜的总物质的量为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温时HClO的Ka=3.0×10-8,HF的Ka=3.5×10-4。现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是( )
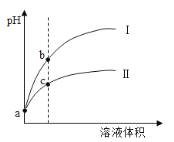
A.曲线I为次氯酸稀释时pH变化曲线
B.b点溶液中水的电离程度比c点溶液中水的电离程度小
C.a点时,若都加入相同大小的锌粒,此时与氢氟酸反应的速率大
D.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗次氯酸的体积较小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.标准状况下2.24L氯气与水充分反应转移电子数为0.1NA
B.标况下,2.24LNO2分子总数小于0.1NA
C.标准状况下2.24L的CCl4中含有的C—Cl键数为0.4NA
D.6.8g液态KHSO4中含有0.1NA个阳离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com