
【题目】微生物燃料电池的研究已成为治理和消除环境污染的重要课题,利用微生物电池电解饱和食盐水的工作原理如下图所示。下列说法正确的是
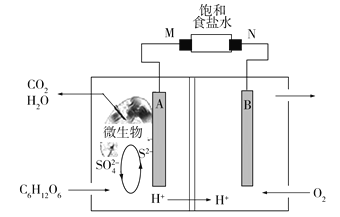
A.电池正极的电极反应:O2+2H2O+4e![]() 4OH
4OH
B.电极M附近产生黄绿色气体
C.若消耗1 mol S2,则电路中转移8 mol e
D.将装置温度升高到60 ℃,一定能提高电池的工作效率
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】已知热化学方程式C2H2(g)+![]() O2(g)=2CO2(g)+H2O(g) ΔH=-1256kJ·mol-1,下列说法正确的是( )
O2(g)=2CO2(g)+H2O(g) ΔH=-1256kJ·mol-1,下列说法正确的是( )
A.乙炔的燃烧热为-1256kJ·mol-1
B.若转移10mol电子,则消耗2.5molO2
C.若生成2mol液态水,则ΔH=-2512kJ·mol-1
D.若形成4mol碳氧共用电子对,则放出的热量为2512kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢、氮、氧、硫、镁、铁、铜、锌等元素及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
(1)某同学根据已学知识,推断 Mg 基态原子的核外电子排布为,![]() 该同学所画的电子排布图违背了____
该同学所画的电子排布图违背了____
(2)Cu 位于____族____区,Cu+价电子排布式为____。
(3)MgCO3的分解温度____ BaCO3(填“>” 或、“<”)
(4)Ge、As、Se 元素的第一电离能由大到小的顺序为____
(5)已知 H3BO3 是一元酸,1molH3BO3 在水中完全电离得到的阴离子中含有σ键的数目为____
(6)下列有关说法不正确的是____。
A.热稳定性:NH3 >PH3,原因是NH3分子间存在氢键,而PH3分子间存在范德华力
B.SO2 与 CO2 的化学性质有些类似,但空间结构与杂化方式不同
C.熔、沸点: SiF4< SiCl4< SiBr4 <SiI4 ,原因是分子中共价键键能逐渐增大
D.熔点: CaO > KCl > KBr,原因是晶格能逐渐减小
(7)晶体 Cu 的堆积方式如图所示,其中Cu原子在二维平面里放置时的配位数为_________,设Cu原子半径为a,晶体的空间利用率为______。(用含π,a、的式子表示,不必化简)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(NaAlH4)是有机合成的一种重要还原剂。一般的制备方法是将AlC13溶于有机溶剂,再把所得溶液滴加到NaH粉末上,可制得铝氢化钠。实验要求和装置如下,回答下列问题:
(1)制取铝氢化钠要在非水溶液中进行,主要原因是_______(用化学方程式表示)。用下列装置制取少量铝氢化钠(含副产物处理)较为合理的是__________。

(2)对于原料A1C13的制取,某兴趣小组设计了如下装置:
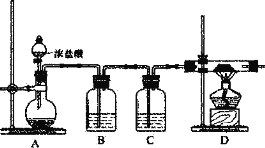
①连接好装置后,应进行的第一步操作是_________;为保证产物的纯净,应待D中__________(填现象)再加热酒精灯。
②B装置中盛装饱和NaCl溶液,实验开始后B中产生的现象是_________,选择饱和NaCl溶液的理由是_____。
③C装置的作用是_________;若无C装置,试预测实验后D中生成物除A1C13外可能还含有_________。(填化学式)
④上述装置存在的明显缺陷是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习小组进行实验测定H2C2O4·xH2O 中x值。已知:M(H2C2O4)=90 g·mol-1
①称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液;
②取25.00mL 待测液放入锥形瓶中,再加入适量稀H2SO4;
③用浓度为 0.05 000 mol·L-1的 KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式__________。
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是__________(选填 a、b)。
a. 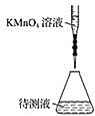 b.
b. 
(3)由图可知消耗KMnO4溶液体积为_______mL。

(4)滴定过程中眼睛应注视________。
(5)通过上述数据,求得x=______。以标准KMnO4溶液滴定样品溶液的浓度,未用标准KMnO4溶液润洗滴定管,引起实验结果______ (偏大、偏小或没有影响) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班学生对BeCl2是离子化合物还是共价化合物进行集体探究,从经验看铍是金属元素,易失去电子,氯元素易得到电子,请回答以下问题:
(1)Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为_________化合物。
(2)工业上制取BeCl2方法是:将得到的BeCl2溶液在HCl气流中蒸干灼烧,防止BeCl2水解,请写出BeCl2水解的化学方程式__________________。
(3)经实验验证,熔融的BeCl2不能导电,说明它是_______化合物;BeCl2能溶于水,水溶液能导电,因它在溶液中能电离,写出它的电离方程式_________。
(4)在周期表中,铍元素和铝元素恰好处于对角线位置,根据对角线法则,判断BeCl2应与_____(填MgCl2或AlCl3)化学性质更相似。
(5)0.1mol氢氧化铍恰好能和100mL0.2mol/L的氢氧化钠溶液发生反应,写出反应的化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于电影《我不是药神》中对抗癌药物格列卫的关注,我国政府在2018年已经将格列卫等部分抗癌药物纳入医保用药,解决了人民群众用药负担。格列卫在其合成过程中的一种中间产物结构表示如下: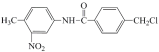 。下列有关该中间产物的说法不正确的是()
。下列有关该中间产物的说法不正确的是()
A. 该药物中间体属于芳香烃
B. 该药物中间体中含有三种官能团
C. 该药物中间体的所有碳原子可能共面
D. 该药物中间体可以发生加成反应和取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a,b,c,d为四种由短周期元素构成的中性粒子,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是单核粒子,a单质可用作半导体材料,a原子核外电子排布式为______________。
(2)b是双核化合物,常温下为无色无味气体。b的化学式为________。人一旦吸入b气体后,就易引起中毒,是因为__________而中毒。
(3)c是双核单质,写出其电子式____________。c分子中所含共价键的类型为_______(填“极性键”或“非极性键”)。c单质常温下性质稳定,不易起反应,原因是________________________。
(4)d是四核化合物,其结构式为______________;d分子内所含共价键有________个σ键,________个π键;σ键与π键的强度大小关系为σ___π(填“>”、“<”或“=”),原因是:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体。下面是它的一种实验室合成路线:
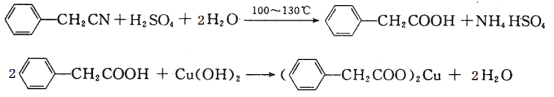
制备苯乙酸的装置示意图如下(加热和夹持装置等略):
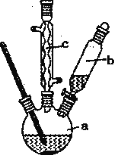
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
实验步骤:
Ⅰ.制苯乙酸粗品
在250 mL三颈瓶a中加入70 mL70%硫酸,加入碎瓷片,将a中的溶液加热至100 ℃,通过仪器b缓缓滴加40 g 苯乙腈到硫酸溶液中,然后升温至130℃继续反应。反应结束后加适量冷水,立即析出苯乙酸晶体,再分离出苯乙酸粗品。
Ⅱ.提纯苯乙酸 Ⅲ.制苯乙酸铜
将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30 min,过滤,滤液静置一段时间,析出苯乙酸铜晶体。
回答下列问题:
(1)配制70%硫酸时,加入蒸馏水与浓硫酸的先后顺序是_____________。
(2)加入碎瓷片的作用是____________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是____________(填答案标号)。
A 立即补加 B 冷却后补加 C 不需补加 D 重新配料实验
(3)仪器c的名称是 ______ ,其作用是__________ 。
(4)下列仪器中,不能用于分离苯乙酸粗品的是____________ (填标号) 。
A 蒸馏烧瓶 B 漏斗 C 烧杯 D 直形冷凝管 E 玻璃棒
(5)提纯粗苯乙酸操作的方法名称是_____ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com