
����Ŀ���������۵�ߡ�Ӳ�ȴ������õĿ����Ժ͵��¿���ʴ��.��ҵ���÷�¯��(��Ҫ��FeO��V2O3����������Al2O3��CuO������)��ȡ��������������ͼ��

��֪:
I.���ж��ּ�̬������+5�����ȶ�.������Һ����Ҫ��VO2+��VO3-����ʽ���ڣ�����ƽ�⣺VO2++H2OVO3+2H+.
��.�������ӵij���pH��
Cu2+ | Fe2+ | Fe3+ | |
��ʼ����PH | 5.2 | 7.6 | 2.7 |
��ȫ����PH | 6.4 | 9.6 | 3.7 |
�ش���������
(1)������������ѡ��______________(����ĸ)
a. NaOH��Һ b.��ˮc.������Һ
(2)���յ�Ŀ���ǽ�FeO��V2O3ת��Ϊ������NaVO3��������Ԫ��ȫ��ת��Ϊ+3�۵������д���÷�Ӧ�Ļ�ѧ����ʽ___________________________________
(3)��Һ1����Һ2�Ĺ����У�����pH��8������Ŀ�ģ�һ�dz�ȥ________���ӣ����Ǵ�ʹ_________.
(4)���������еõ�NH4VO3������Ҫϴ�ӣ�д��ʵ����ϴ�ӵIJ�������____________________.
(5)�������ȷ�Ӧ����V2O5ұ������������д����Ӧ�Ļ�ѧ����ʽ____________________________.
(6)���Ļ�����Ҳ�й㷺����;����һ�����������ӿɳ���صĽṹ��ͼ��ʾ.
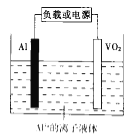
��֪�ŵ�ʱ��ط�ӦΪxAl+VO2=AlxVO2������ŵ�ʱ�����ĵ缫��ӦʽΪ_____________________.
���𰸡�a 4FeO��V2O3+4Na2CO3+5O2![]() 8NaVO3+2Fe2O3+4CO2 Fe3+��Cu2+ VO2+ת��ΪVO3- ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2
8NaVO3+2Fe2O3+4CO2 Fe3+��Cu2+ VO2+ת��ΪVO3- ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2![]() 3�� 10Al+3V2O5
3�� 10Al+3V2O5![]() 5Al2O3+6V VO2+xAl3++3xe-=AlxVO2
5Al2O3+6V VO2+xAl3++3xe-=AlxVO2
��������
���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ�á�
������Ҫ����FeO��V2O3��Al2O3��CuO�����м�����������ܽ��γ�ƫ�����Σ����˺���Һ1����ƫ�����Σ�ͨ�������̼�õ����������������������ȷֽ�ɵõ�������������1���������б��գ����������������ܽ⣬��Һ1�к���ͭ���ӡ������ӣ�����pHֵ��8��ͭ���ӡ������ӳ�����ȫ�����˵�����2ӦΪ������ͭ������������ͬʱ������Һ�д���ƽ��VO2++H2OVO3-+2H+������������Ƶ�����NH4VO3������Ҫ������Һ��pHֵ�����˵���Һ2����Ҫ����Ԫ����VO2+��VO3-����ʽ���ڣ��ټ��������ת��ΪNH4VO3�� NH4VO3���յõ�V2O5��V2O5���������ȷ�Ӧ�õ�V���ݴ˽��
������Ҫ����FeO��V2O3��Al2O3��CuO�����м�����������ܽ��γ�ƫ�����Σ����˺���Һ1����ƫ�����Σ�ͨ�������̼�õ����������������������ȷֽ�ɵõ�������������1���������б��գ����������������ܽ⣬��Һ1�к���ͭ���ӡ������ӣ�����pHֵ��8��ͭ���ӡ������ӳ�����ȫ�����˵�����2ӦΪ������ͭ������������ͬʱ������Һ�д���ƽ��VO2++H2OVO3-+2H+������������Ƶ�����NH4VO3������Ҫ������Һ��pHֵ�����˵���Һ2����Ҫ����Ԫ����VO2+��VO3-����ʽ���ڣ��ټ��������ת��ΪNH4VO3�� NH4VO3���յõ�V2O5��V2O5���������ȷ�Ӧ�õ�V��
��1����������ķ�����֪�����Ҫʹ�������ܽ⣬����ֻ����ǿ���ѡa����С���Ϊ��a��
��2�����յ�Ŀ���ǽ�FeO��V2O3ת��Ϊ������NaVO3��������Ԫ��ȫ��ת��Ϊ+3�۵���������ݴ���Ϣ��֪����ʽΪ4FeO��V2O3+4Na2CO3+5O2![]() 8NaVO3+2Fe2O3+4CO2����С���Ϊ��4FeO��V2O3+4Na2CO3+5O2
8NaVO3+2Fe2O3+4CO2����С���Ϊ��4FeO��V2O3+4Na2CO3+5O2![]() 8NaVO3+2Fe2O3+4CO2��
8NaVO3+2Fe2O3+4CO2��
��3����Һ1����Һ2�Ĺ����У�����pH��8һ����ʹͭ���ӡ������ӳ�����ȫ������������Һ�д���ƽ��VO2++H2OVO3-+2H+������������Ƶ�����NH4VO3����С���Ϊ��Fe3+��Cu2+��VO2+ת��ΪVO3-��
��4�����������еõ�NH4VO3������Ҫϴ�ӣ�ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2![]() 3�Ρ���С���Ϊ��ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2
3�Ρ���С���Ϊ��ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2![]() 3�Ρ�
3�Ρ�
��5�����ȷ�Ӧ��V2O5ұ���������Ļ�ѧ����ʽΪ10Al+3V2O5![]() 5Al2O3+6V����С���Ϊ��10Al+3V25
5Al2O3+6V����С���Ϊ��10Al+3V25![]() 5Al2O3+6V��
5Al2O3+6V��
��6���õ�صĸ���Ϊ����ʧ���ӷ���������Ӧ���缫��ӦʽΪAl-3e-=Al3+����ص��ܷ�ӦΪxAl+VO2=AlxVO2������������ӦΪ�ܷ�Ӧ��ȥ������Ӧ�������缫��ӦʽΪVO2+xAl3++3xe-=AlxVO2����С���Ϊ��VO2+xAl3++3xe-=AlxVO2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����ƺ��ռ��ԭ�����£�����������Ȼ������ƣ�2NaCl(����) ![]() 2Na��Cl2��������ⱥ��ʳ��ˮ���ռ2NaCl��2H2O
2Na��Cl2��������ⱥ��ʳ��ˮ���ռ2NaCl��2H2O ![]() 2NaOH��H2����Cl2���������й�˵����ȷ���ǣ�������
2NaOH��H2����Cl2���������й�˵����ȷ���ǣ�������
A.�ڷ�Ӧ�������У��Ȼ��ƾ����������������ǻ�ԭ��
B.�ڷ�Ӧ���������ǻ�ԭ����ڷ�Ӧ���������ǻ�ԭ����
C.����״�������ɵ���������壬��Ӧ��������ת�Ƶ����������
D.�����ĵ��������Ȼ��ƣ���Ӧ�ٺ͢���ת�Ƶ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Է�ˮ�е�����Ԫ�ص�ȥ���Ѿ������������Ա�Ĺ㷺��ע���������������ϵ�Է�ˮ����̬�������н���ʵ��ȡ�������õ�ȥ��Ч����װ����ͼ��ʾ����ƽ��缫(����ʱa��Ϊ���缫��b��Ϊ�ѵ缫������ʱa��Ϊ����b��Ϊ�Ѱ�)���ɶ�ά������ⷴӦ��������˵���������

A. a�缫�ϵĵ��Ʊ�b�缫�ϵĵ��Ƹ�
B. ����ʱ��b���ĵ缫��ӦʽΪ![]()
C. �����ܷ�Ӧ����Ϊ![]() ��
��![]()
D. �Ѽ������������ܷ����������ã�ʹ��Һ�п�����Ư����������ȥ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����������л�����ԭ��֮һ����ҵ�Ͽ��ö�����̼��������Ӧ�������״���
��1����֪��̬�״���ȼ����Ϊa kJ/mol��2H2(g)+O2(g) = 2H2O(g) ��H= -bkJ/mol��H2O(g)=H2O(l) ��H= -ckJ/mol�� ��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)����H=_________��
CH3OH(g)+H2O(g)����H=_________��
��2��ij�¶��£���2 L�ܱ������У�����2.4 mol CO2��4.4 mol H2�������ϳɼ״��ķ�Ӧ����ü״������ʵ�����ʱ��ı仯ͼ����ͼ�е�����I����ǰ4������(CO2)=__________������1 minʱ���ı�ijһ��Ӧ����������I��Ϊ����II����ı������Ϊ___________�����¶��·�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ___________��

��3������һ�¶��·����ϳɼ״��ķ�Ӧ����ͼ�ر�K����A�����г���1 mol CO2��4 mol H2����B�����г���1.2 mol CO2��4.8 mol H2���������ֱ���������Ӧ����֪��ʼʱ����A��B�������Ϊa L����Ӧ�ﵽƽ��ʱ����B�����Ϊ0.9a L��ά�������������䣬����Kһ��ʱ������´ﵽƽ�⣬����B�����Ϊ______L(�������¶ȵı仯��PΪ�����ɻ��������������ǻ�����Ħ����)��

��4��һ�������¼״��ɽ�һ������ת��Ϊ���ᡣ�����£���amol/L�ļ�����bmol/L��NaOH��Һ�������ϣ���ϵ�д���c(Na+)=c(HCOO-)�����ú�a��b�Ĵ���ʽ��ʾ����ĵ��볣��Ϊ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ҵ�Ͻ�����ͨ��ʯ����[Ca(OH)2]��ȡƯ�ۣ���Ӧ�Ļ�ѧ����ʽ_____________Ư�۵���Ч�ɷ���__________���ѧʽ����
��2��ʵ������ȡ�����Ļ�ѧ����ʽ��__________________________________
��3��1.2gRSO4�к�0.01molR2+����RSO4��Ħ��������______________��
��4��ʵ������Fe(OH)2һ�㿴������ɫ��Fe(OH)2������ԭ��___________________�����ǣ�_________________________ ����Ӧ�Ļ�ѧ����ʽ��__________________________________
��5��̼����ˮ�ⷴӦ�����ӷ���ʽ����һ������_________________________ ��
��6��Ǧ���صĸ�����Ӧʽ��_________________________ ��
��7�����ᱵ�ij����ܽ�ƽ�⣺__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ƥ���Ǵ����Ƥ�з�������л��ᣬ�㷺Ӧ���ھ�ϸ����Ʒ����������Ƥ���һ����·�����£�������Ҫ���Լ���������ȥ��

��֪��

(1)D�й���������Ϊ___________________����ӦIV�ķ�Ӧ����Ϊ______________________��
(2)д����ӦI�Ļ�ѧ����ʽ__________________________________________
(3)д����Ƥ��Ľṹ��ʽ____________________________________________
(4)Ϊ����D�Ƿ��Ѿ���ȫת��Ϊ��Ƥ�ᣬ�����Լ���ʵ��������_________________________��
(5)д��ͬʱ������������������C��ͬ���칹��Ľṹ��ʽ__________________
�����ڷ����廯���� �ں˴Ź�������Ϊ����� ������ NaHCO3��Һ��Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС���ͬѧ��Zn.Cu��ϡ������ɵ�ԭ��ؽ�����̽��,���м�ͬѧ������ͼIװ�ý���̽������ͬѧ�����������Ϻ������ͼIIװ�ý���̽��(�����ں���ij�ֵ���ʵı�����Һ������ͨ��·������)��

��1��ʵ�����,ͼI�������缫�Ͼ������ݲ���,п�缫�������ݲ���,˵����Ӧ����һ���ֻ�ѧ��ת��Ϊ______��;ͭ�缫�������ݲ���,˵����Ӧ����һ���ֻ�ѧ��ת��Ϊ____����
��2��ͼII�е�X��Y��ZnSO4��Һ��ϡ�����е�һ��,ʵ�������ֻ�������ϲ������ݣ���X��_________�������ϵĵ缫��ӦʽΪ__________��
��3����ͼIװ�õ���Һ��������63gʱ,���ɵ���������______L(��״��);��ͼII��п�缫��������65gʱ,��·��ת�Ƶĵ�����Ϊ______NA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ܰ뵼�����Ҫԭ�ϡ���ҵ�ϳ���п��ұ���ķ����л����ء���֪ijп������Ҫ��Zn��Si��Pb��Fe��Ga����������øÿ������صĹ����������£�

��֪��������Ԫ�����ڱ���λ�ڵ������ڵڢ�A����ѧ�����������ơ�
��lg2=0.3��lg3=0.48��
�۲������ʵ�Ksp��F����ʾ
���� |
|
|
|
|
Ksp |
|
|
|
|
��1������1����Ҫ�ɷ���_________��д��ѧʽ����
��2������H2O2��Ŀ����(�����ӷ���ʽ��ʾ)___________��
��3����pH��Ŀ����______�����������£�������Һ�и������ӵ�Ũ�Ⱦ�Ϊ0.01 mol/L������Һ��ij������Ũ��С��![]() mol/Lʱ����Ϊ����������ȫ��ȥ����pHӦ���ڵķ�ΧΪ_______��
mol/Lʱ����Ϊ����������ȫ��ȥ����pHӦ���ڵķ�ΧΪ_______��
��4������D������__________���ˡ�ϴ�ӡ����
��5���Ʊ�����������Ga��
�ٵ�ⷨ�Ʊ������ء��ö��Ե缫���![]() ��Һ�����Ƶý����أ�д�������缫��Ӧʽ_________��
��Һ�����Ƶý����أ�д�������缫��Ӧʽ_________��
�ڵ�ⷨ���������أ����غ�Zn��Fe��Cu�����ʣ���֪������:![]()
�����йص�⾫�������ص�˵����ȷ����_______������ĸ��ţ���
A .��⾫����ʱ�������Դ����������
B. ��⾫�������У����������ļ����������������������
C. ����Cu��Fe�����ڵ��۵ײ��γ�������
D. ���ü���ȼ�ϵ�ص�⾫�������أ���������56.0 g������ʱ����ظ���������ı�״���µ�![]() 6.72 L
6.72 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�Ksp(CaSO4)=9��10-6,������CaSO4��ˮ�еij����ܽ�ƽ������ͼ������˵����ȷ����( )

A.CaSO4��ϡ�����е��ܽ��Ա��ڴ�ˮ�е��ܽ���ǿ
B.b�㽫�г������ɣ�ƽ�����Һ��c(SO42-)һ������3��10-3 mol/L
C.d����Һͨ���������Ա䵽c��
D.a���Ӧ��Ksp����c���Ӧ��Ksp
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com