
【题目】Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用图装置可以探究![]() 与
与![]() 反应生成
反应生成![]() 沉淀的条件。下列判断正确的是( )
沉淀的条件。下列判断正确的是( )
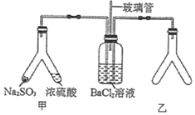
A.玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
B.使用Y形管甲时,应将![]() 固体转移到浓硫酸中
固体转移到浓硫酸中
C.Y形管乙中产生的为氧化性气体,将![]() 氧化为
氧化为![]() 沉淀
沉淀
D.Y形管乙中的试剂可以分别是浓氨水和NaOH固体
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
Ⅰ. [查阅资料]
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水。其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得产品中常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
(4)硫代硫酸钠与碘反应的离子方程式为:2![]() +I2=
+I2=![]() +2I
+2I
Ⅱ. [制备产品]实验装置如图所示(省略夹持装置)
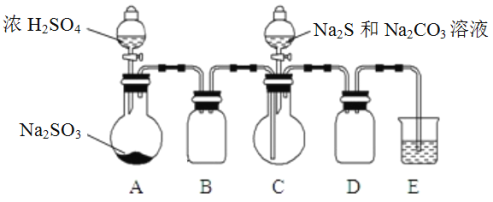
实验步骤:
(1)按如图所示组装好装置后,应先_________________________________________(填操作名称),再按图示加入试剂。仪器B和D的作用是__________________________________________;
(2)先向烧瓶C中加入Na2S和Na2CO3混合溶液,再向烧瓶A中滴加浓H2SO4。C中反应生成Na2S2O3和CO2,化学方程式为____________________________________________________________________。
(3)待Na2S和Na2CO3完全消耗后,结束反应。过滤C中混合液,滤液经蒸发、结晶、过滤、洗涤、干燥、得到产品。
Ⅲ. [探究与反思]
(4)用I2的标准溶液测定产品的纯度。取10.0g产品,配制成100mL溶液,配制溶液的蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除_______________________________及二氧化碳。取10.00mL溶液。以________________________________溶液为指示剂,用浓度为0.10 mol/L I2的标准溶液进行滴定,相关数据记录如下表所示。
编号 | 1 | 2 | 3 |
溶液的体积/mL | 10.00 | 10.00 | 10.00 |
消耗I2标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |
滴定时,达到滴定终点的现象是___________________________。Na2S2O3·5H2O在产品中的质量分数是____________________________________(用百分数表示,且保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种无机物具有如图所示的转化关系(反应条件及反应中的水均略去),且A、B、C含有同一种元素。下列说法错误的是
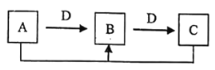
A.若A的溶液显碱性,则D可能是单质
B.A与C的反应可能是非氧化还原反应
C.A或D可能是目前使用最广泛的金属单质
D.若C是能使澄清石灰水变浑浊的气体,则A一定是单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置制备FeCO3,提取出的FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。已知:葡萄糖酸亚铁(C6H11O7)2Fe是常用的补铁剂,易溶于水。回答下列问题:
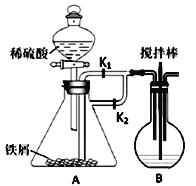
Ⅰ(1)B中加入药品Na2CO3,要使A中制得的FeSO4溶液进入B中发生反应,实验开始时,应打开分液漏斗的活塞、______,关闭______,一段时间后,关闭_______,打开________ (填旋塞的编号)。
(2)将葡萄糖酸与碳酸亚铁混合,反应的化学方程式为(有机物用分子式表示)________________。
(3)从环境保护的角度分析,该装置存在不足之处是:_____________。
Ⅱ.某补铁剂的主要成分是硫酸亚铁,用氧化还原滴定法可测定该补铁剂中铁元素的含量,实验的主要步骤如下:
①取10片补铁剂样品,溶解除去不溶物(不损耗铁元素),并配成100mL待测溶液。
②量取25.00mL待测液于锥形瓶中。
③用c mol·L1的酸性KMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积,重复两次实验,平均消耗KMnO4溶液体积为V mL。
(4)该滴定原理的离子方程式为______________________
(5)上述实验中应该用稀硫酸酸化KMnO4溶液,如果用硝酸对KMnO4溶液进行酸化,对测定结果的影响是________(填“偏大”“偏小”或“无影响”)。滴定终点的实验现象为______。
(6)每片补铁剂含铁元素的质量为__________g(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境问题越来越受到人们的重视,“绿水青山就是金山银山”的理念已被人们认同。运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染具有重要意义。回答下列问题:
(1)亚硝酰氯(Cl—N=O)气体是有机合成中的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为______________________。相关化学键的键能如下表所示:
化学键 | Cl—Cl | N≡O(NO气体) | Cl—N | N=O |
键能/(kJ·mol-1) | 243 | 630 | 200 | 607 |
(2)有人设想采用下列方法减少SO2、NO2对环境的污染:用CH4还原SO2,从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NO2。这种含硫化合物和NO2反应的化学方程式为______________________。
(3)用NaOH溶液吸收SO2也是减少大气污染的一种有效方法。25℃时,将一定量的SO2通入到NaOH溶液中,两者完全反应,若溶液中![]() ,则该混合溶液的pH=___________(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。
,则该混合溶液的pH=___________(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将锌片和铜片按图示方式插入柠檬中,电流计指针发生偏转。下列针对该装置的说法正确的是( )
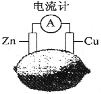
A.将电能转换为化学能
B.电子由铜片流出经导线到锌
C.一段时间后,锌片质量减轻
D.铜片一侧柠檬变蓝色,产生Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、W为前四周期中原子序数依次增大的元素。X原子的2p能级上有两个未成对电子,且无空轨道。Y原子K层的电子数与M层的电子数的乘积等于其L层的电子数;Z与X同族,Q位于第ⅠB族;W元素最高正价和最低负价的代数和为4。根据以上信息,回答下列问题。
(1)W元素的名称是:___________;其简化的电子排布式为___________________;X的基态原子核外最高能级上有_____种不同空间运动状态的电子;已知高温下4QX→2Q2X+X2,从Q原子价层电子结构的角度分析,能生成Q2X的原因是__________________________________。
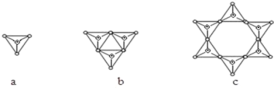
(2)Y与X可以形成多种复杂阴离子,如下图所示,若其中a对应的阴离子化学式为YX![]() ,则c对应的阴离子的化学式为_________________(圆圈代表X原子,黑点代表Y原子)。
,则c对应的阴离子的化学式为_________________(圆圈代表X原子,黑点代表Y原子)。
(3)向盛有含Q2+的溶液中加入氨水至过量,沉淀溶解的离子方程式为___________________。写出最后所得配离子的结构式____________________________________(配位键须注明)。
(4)W、Y均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,VSEPR构型____________(填“相同”或“不相同”),若“YH”中共用电子对偏向氢元素,氢气与W反应时单质W是氧化剂,则W与Y的电负性相对大小为______________(用元素符号作答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiBH4为近年来储氢材料领域的研究热点。
(1)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L H2(标准状况)时,转移电子的物质的量为____mol。
(2)下图是2LiBH4/MgH2体系放氢焓变示意图,则:
Mg(s)+2B(s)=MgB2(s) △H=________。

(3)采用球磨法制备Al与LiBH4的复合材料,并对Al-LiBH4体系与水反应产氢的特性进行下列研究:
①如图为25℃水浴时每克不同配比的Al-LiBH4复合材料与水反应产生H2体积随时间变化关系图。由图可知,下列说法正确的是____(填字母)。

a.25℃时,纯铝与水不反应
b.25℃时,纯LiBH4与水反应产生氢气
c.25℃时,Al-LiBH4复合材料中LiBH4含量越高,1000s内产生氢气的体积越大
②如图为25℃和75℃时,Al-LiBH4复合材料[ω(LiBH4)=25%]与水反应一定时间后产物的X-射线衍射图谱(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。

从图中分析,25℃时Al-LiBH4复合材料中与水完全反应的物质是___________(填化学式),产生Al(OH)3的化学方程式为_________________。
(4)如图是直接硼氢化钠-过氧化氢燃料电池示意图。该电池工作时,正极附近溶液的pH________(填“增大”、“减小”或“不变”),负极的电极反应式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图中的实验方案,能达到实验目的是( )
A.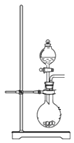 可用于制取少量NH3或用MnO2和浓盐酸制取Cl2
可用于制取少量NH3或用MnO2和浓盐酸制取Cl2
B.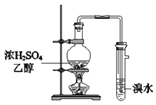 可用于制取乙烯并检验乙烯
可用于制取乙烯并检验乙烯
C.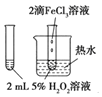 可以验证FeCl3对H2O2分解反应有催化作用
可以验证FeCl3对H2O2分解反应有催化作用
D.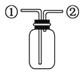 先从
先从![]() 口进气集满CO2,再从
口进气集满CO2,再从![]() 口进气,可用于收集NO
口进气,可用于收集NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com