
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
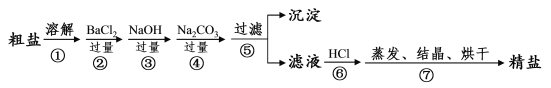
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是___。
(2)第②步操作的目的是除去粗盐中的___(填化学式,下同),第⑥步操作的目的是除去滤液中___。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、___、___(填化学式),写出操作②和操作③的相关化学方程式___、___。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是___。
【答案】加速溶解 Na2SO4 NaOH、Na2CO3 CaCO3 BaCO3 BaCl2+Na2SO4=BaSO4↓+2NaCl MgCl2+2NaOH=Mg(OH)2↓+2NaCl 会引入新的杂质,在后面的操作中无法除去
【解析】
实验流程为:粗盐样品含有Na2SO4、MgCl2、CaCl2等杂质,加入过量的氯化钡,可以将硫酸根离子除去,但是会引入钡离子杂质离子,加入过量氢氧化钠溶液的目的是除去氯化镁,加入过量的碳酸钠溶液的目的除去杂质CaCl2和加入的过量试剂BaCl2,过滤,将得到的沉淀全部滤出,得到的滤液是含有氯化钠、碳酸钠、氢氧化钠等的混合物,加入足量的盐酸,可以出去碳酸根离子、氢氧根离子等杂质离子,最后即可获得较为纯净的氯化钠,据此分析解题。
(1)第①步粗盐溶解操作中用玻璃棒搅拌,可加速粗盐的溶解;
(2)第②步加入氯化钡溶液可以除去杂质Na2SO4;第⑥步盐酸酸化的目的是除去滤液中的NaOH、Na2CO3;
(3)第⑤步通过过滤可把溶液中的不溶物除去,则可以除去的物质有泥沙、BaSO4、Mg(OH)2、BaCO3和CaCO3;操作②滴加BaCl2时发生反应的化学方程式为BaCl2+Na2SO4=BaSO4↓+2NaCl,操作③滴加NaOH溶液时发生反应的化学方程式为MgCl2+2NaOH=Mg(OH)2↓+2NaCl;
(4)目标产物为NaCl,在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,否则会引入新的杂质离子K+,在后面的操作中无法除去,最终所得NaCl不纯。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】在空气中,有下列反应发生: ①N2 + O2 = 2NO;②2NO+O2=2NO2;③3NO2 + H2O = 2HNO3 + NO;④ 2SO2+O2 = 2SO3;⑤ SO3 + H2O = H2SO4; ⑥SO2+H2O![]() H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
A. ①②③④ B. ①②③④⑦ C. ①②④⑦ D. ①②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2SO2+O2![]() 2SO3的叙述不正确的是( )
2SO3的叙述不正确的是( )
A.该反应是可逆反应,在相同条件下,反应可同时向两个方向进行
B.1mol氧气与2mol二氧化硫混合发生反应能生成2mol三氧化硫
C.在该反应中二氧化硫作还原剂,氧气作氧化剂
D.该反应有0.4mol电子发生转移时,生成三氧化硫0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.4.0g金属钙变成钙离子时失去的电子数为0.1NA
B.46gNO2和N2O4的混合气体含有的原子数为3NA
C.3.01×1023个氮分子中含有的原子数为2NA
D.0.1molOH-中含有的电子数为0.9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的数值,下列说法正确的( )
A. 常温常压下,22.4L的O2含有分子数为NA
B. 标准状况下,22.4L的SO3含有分子数为NA
C. 标准状况下,17gNH3含有的电子数为8 NA
D. 常温常压下,14gC2H4和C3H6的混合物含原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经研究发现白蚁信息素有:A. ![]() ; B.
; B. ![]() ;家蚕的信息素为:CH3(CH2)2CH=CH-CH=CH(CH2)8CH3。试回答下列问题:
;家蚕的信息素为:CH3(CH2)2CH=CH-CH=CH(CH2)8CH3。试回答下列问题:
(1)下列说法正确的是________(填序号)。
A.信息素A、B互为同系物
B.以上三种信息素均能使溴的四氯化碳溶液褪色
C.信息素A、B互为同分异构体
D.1mod家蚕信息素与1molBr2加成产物只有一种
(2)用系统命名法命名:信息素A的名称为___________________;信息素B与氢气加成产物的名称为_____________________________。
(3)烯烃C是信息素A的一种同分异构体,C与足量氢气加成得到烷烃D,D的一氯代物只有2种,则D的结构简式为_________________________________。
(4)写出信息素B与溴水发生反应的化学方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是
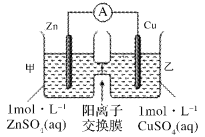
A. 该装置中电子的流动方向为:铜电极→锌电极
B. 电池工作一段时间后,甲池溶液的总质量不变
C. 电池工作一段时间后,乙池的c(SO42-)不变
D. 溶液中阳离子通过交换膜从负极区向正极区移动保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题:
(1)氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。已知:2C(s)+O2(g)=2CO(g)△H=-22lkJ/mol,
C(s)+O2(g)=CO2(g)△H=-393.5 kJ/mol,
N2(g)+O2(g)=2NO(g)△H=+181 kJ/mol,
则:2CO(g)+2NO(g)![]() N2(g)+2CO2(g)△H=__kJ/mol;
N2(g)+2CO2(g)△H=__kJ/mol;
下列措施能够增大此反应中NO的转化率的是___(填字母序号)
a.增大容器的体积 b.降低温度 c.增大CO的浓度 d.增大NO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g)△H=-574.5kJ/mol;NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g)△H=-574.5kJ/mol;NO和N2的物质的量变化如下表所示。
物质的量/mol | T1/℃ | T2/℃ | |||||
0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
NO | 2.0 | 1.20 | 0.70 | 0.70 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.40 | 0.65 | 0.65 | 0.75 | 0.80 | 0.80 |
①0~5min内,以NO表示的该反应速率υ(NO)=__________,该条件下的平衡常数K=___________(保留2位小数)。
②第15min后,温度调整到T2,数据变化如上表所示,则T1___________T2(填“>”、“<”或“=”)。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与CrO42-生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-6mol·L-1)时,溶液中c(Ag+)为__mol·L-1,此时溶液中c(CrO42-)等于____mol·L-1。(已知Ksp(Ag2CrO4)=2.0×10-12,Ksp(AgCl)=2.0×10-10)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关NaHCO3和Na2CO3的性质,以下叙述错误的是
A.等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下Na2CO3产生的CO2体积小
B.等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3的两倍
C.等质量NaHCO3和Na2CO3与盐酸完全反应,前者消耗盐酸较多
D.等物质的量的NaHCO3和Na2CO3与足量盐酸反应产生CO2一样多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com