
����Ŀ������β���е���Ҫ��Ⱦ����NO�Լ�ȼ�ϲ���ȫȼ����������CO��Ϊ�˼��������Ⱦ���������ͨ�����·�Ӧ����������β����2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) ��H = a kJ��mol-1��Ϊ�˲ⶨ��ij�ִ��������¸÷�Ӧ�ķ�Ӧ���ʣ�t1���£���һ���ݵ��ܱ������У�ij���л��������崫��������˲�ͬʱ���NO��CO��Ũ�����±���CO2��N2����ʼŨ�Ⱦ�Ϊ0����
2CO2(g)+N2(g) ��H = a kJ��mol-1��Ϊ�˲ⶨ��ij�ִ��������¸÷�Ӧ�ķ�Ӧ���ʣ�t1���£���һ���ݵ��ܱ������У�ij���л��������崫��������˲�ͬʱ���NO��CO��Ũ�����±���CO2��N2����ʼŨ�Ⱦ�Ϊ0����
ʱ�� (s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/10-4mol/L | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/10-3mol/L | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
�ش��������⣺
��1�������������¸÷�Ӧ���Է����У�������Ӧ��Ȼ��_______��Ӧ��������������������������
��2��ǰ3s�ڵ�ƽ����Ӧ������(N2)=___________��t1��ʱ�÷�Ӧ��ƽ�ⳣ��K=________��
��3���������ܱ������з���������Ӧ���ﵽƽ��ʱ�ı����������������NOת���ʵ���_______��
A��ѡ�ø���Ч�Ĵ��� B�����߷�Ӧ��ϵ���¶�
C�����ͷ�Ӧ��ϵ���¶� D����С���������
��4����֪��N2(g)+O2(g)=2NO(g) ��H1=��180.5 kJ��mol-1
2C(s)+O2(g)=2CO(g) ��H2����221.0 kJ��mol-1
C(s)+O2(g)=CO2(g) ��H3����393.5 kJ��mol-1
��������β����Ӧ�е�a=__________��
��5���û���̿��ԭ��Ҳ���Դ�����������йط�ӦΪ��C(s)+2NO(g) ![]() CO2(g)+N2(g) ��H4����ij�ܱ���������һ�����Ļ���̿��NO����t2���·�Ӧ���й��������±���
CO2(g)+N2(g) ��H4����ij�ܱ���������һ�����Ļ���̿��NO����t2���·�Ӧ���й��������±���
NO | N2 | CO2 | |
��ʼŨ��/mol��L-1 | 0.10 | 0 | 0 |
ƽ��Ũ��/mol��L-1 | 0.04 | 0.03 | 0.03 |
ƽ��������¶ȣ��ٴδﵽƽ����������NO��N2��CO2��Ũ��֮��Ϊ5:3:3������H4_______0������ >������=������<������
���𰸡�����1.42��10-4 mol ��L-1��s-15000C D-746.5<
��������
(1)�ɷ�Ӧ�ܹ��Է����У�����H-T��S��0���ɷ���ʽ��֪��S��0����ֻ�и÷�Ӧ����H��0ʱ�����÷�Ӧһ���Ƿ��Ȳ��п����Է����У��ʴ�Ϊ�����ȣ�
(2)ǰ3s�ڵ�ƽ����Ӧ����v(N2)=![]() v(NO)=
v(NO)=![]() ��
��![]() =1.42��10-4 molL-1s-1���ɱ����е����ݿ�֪��4sʱ�ﵽ��ѧƽ�⣬��
=1.42��10-4 molL-1s-1���ɱ����е����ݿ�֪��4sʱ�ﵽ��ѧƽ�⣬��
2NO + 2CO![]() 2CO2 + N2��
2CO2 + N2��
��ʼ��molL-1��1.00��10-3 3.60��10-3 0 0
ת����molL-1�� 9��10-4 9��10-4 9��10-4 4.50��10-4
ƽ�⣨molL-1��1.00��10-4 2.70��10-3 9��10-4 4.50��10-4
�� K=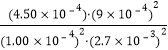 =5000���ʴ�Ϊ��1.42��10-4molL-1s-1��5000��
=5000���ʴ�Ϊ��1.42��10-4molL-1s-1��5000��
(3)A��ѡ�ø���Ч�Ĵ���������ʹƽ�ⷢ���ƶ�����A����B�����߷�Ӧ��ϵ���¶ȣ���Ӧ���ȣ���ƽ�������ƶ���ת���ʼ�С����B����C�����ͷ�Ӧ��ϵ���¶ȣ�ƽ�������ƶ���ת��������C��ȷ��D����С�����������ƽ�������ƶ���ת��������D��ȷ���ʴ�Ϊ��CD��
(4)��֪����N2(g)+O2(g)=2NO(g)��H1=+180.5kJmol-1����2C(s)+O2(g)=2CO(g) ��H2=-221.0kJmol-1����C(s)+O2(g)=CO2(g) ��H3=-393.5kJmol-1��������2-��-�ڿɵ�2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ��H=2��(-393.5kJmol-1)-(-221.0kJmol-1) -(+180.5kJmol-1) =-746.5kJmol-1���ʴ�Ϊ��-746.5��
2CO2(g)+N2(g) ��H=2��(-393.5kJmol-1)-(-221.0kJmol-1) -(+180.5kJmol-1) =-746.5kJmol-1���ʴ�Ϊ��-746.5��
(5)ƽ��ʱ������NO��N2��CO2��Ũ��֮��Ϊ4:3:3�������¶ȣ��ٴδﵽƽ����������NO��N2��CO2��Ũ��֮��Ϊ5:3:3��˵�������¶�ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ���ʴ�Ϊ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ƶ����������ٳ�ŵ�������ܵ����й����ߵ����ӣ�ij�������ѻ���ص�ؽṹ��ͼ��ʾ�������Ϊ�������ӵĸ߾����֪��صķ�Ӧ����ʽΪ2NaxCn+xNaTi2(PO4)3![]() 2nC+ xNa3Ti2(PO4)3�����й��ڸõ��˵����ȷ����
2nC+ xNa3Ti2(PO4)3�����й��ڸõ��˵����ȷ����

A. �ŵ�ʱ�������ΪNaxCn B. �ŵ�ʱNa+��缫���ƶ�
C. ���ʱ������Ӧ��NaxCn-xe-=nC+xNa+ D. ���ʱ�缫�������Դ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������þ��Ϊԭ����ȡ������þ������ӡȾ����ֽ��ҽҩ�ȹ�ҵ����þ����һ�ֹ�ҵ���ϣ���Ҫ�ɷ���MgO(ռ40%)������CaO��MnO��Fe2O3��FeO��Al2O3��SiO2�����ʡ�����þ������ȡMgSO4��7H2O���������£�

(1)ʵ��������3 mol��L��1������500 mL������98%��Ũ����(����1.84 g��mL��1)�����ƣ���ȡŨ����ʱ����ʹ�õ���Ͳ�Ĺ��Ϊ ________(����ĸ)��
A��10 mL B��20 mL C��50 mL D��100 mL
(2)�����NaClO����Mn2����Ӧ������ʽΪMn2����ClO����H2O===MnO2����2H����Cl��,
��ʹ2moL Mn2����������������Ҫ������NaClO����Ϊ______g;����һ������Ҳ�ᱻNaClO�������÷�Ӧ�����ӷ���ʽΪ______________________________________��
(3)��������Ҫ�ɷֳ�����Fe(OH)3��Al(OH)3�⣬������________��_________��
(4)�ڡ����ơ�����ǰ����Ҫ������Һ���Ƿ���Fe2�����������鷽����_____________________________________��
(5)��֪MgSO4��CaSO4���ܽ�����±�(�ܽ�ȵ�λΪg/100 gˮ)��
�¶�/�� | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
�����ơ��ǽ�MgSO4��CaSO4�����Һ�е�CaSO4��ȥ�������ϱ����ݣ���Ҫ˵�����ƵIJ������裺����Ũ����_________�����������ǽ���Һ��������Ũ������ȴ�ᾧ��__________����õ���MgSO4��7H2O��
(6)��ʵ�����ṩ����þ�100 g���õ���MgSO4��7H2OΪ86.1 g����MgSO4��7H2O�IJ���Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ��һ���ܴ����������
A. ʹ���ȳʺ�ɫ����Һ�У�Na+��Ba2+��Cl-��NO3-
B. c( OH-) <![]() ����Һ�У�Na+��Ca2+��ClO-��NO3-
����Һ�У�Na+��Ca2+��ClO-��NO3-
C. ���д���Fe( NO3)2 ����Һ�У�H+��NH4+��Cl-��SO42-
D. ˮ�����c( H+)= 1�� 10 -13mol/L����Һ�У�K+��Mg2+��Br-��CH3COO-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O������������ȷ���ǣ�������
5NaCl+NaClO3+3H2O������������ȷ���ǣ�������
A. Cl2����������������ԭ��
B. ����������ԭ�Ӻͱ���ԭ����ԭ�ӵ����ʵ���֮��Ϊ5��1
C. Cl2����������NaOH�ǻ�ԭ��
D. �������õ������뻹ԭ��ʧ������֮��Ϊ5��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������SiO2��Ӧ����
��ŨH2SO4 ��H2O ������ ��HF ��KOH��Һ ��������
A. �٢ڢ� B. �ڢ� C. �ܢݢ� D. �ۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ��̽���������Ļ����ԣ������ͼ��ʾװ�ã������ƶϺ������ǣ� ��
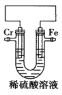
A. �����������ã�����Ӿ����·�����缫������缫
B. �����ȸ����ã�����Һ��H+�����缫Ǩ��
C. �����������ã������缫��ӦʽΪ2H����2e����H2��
D. �����缫������ҺpH���������ȸ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�Ļ���ԭ�ϣ�Ҳ��һ����Ҫ���ܼ�����ش��������⣺

��1����ͼ��ijЩ�л���Ľṹģ�ͣ����б�ʾΪ������_____��
��2����2mL���м���1mL��ˮ�������ã�ʵ������Ϊ_____��
��3����һ�������£����ܷ�������ȡ����Ӧ��д���������������Ļ�ѧ����ʽ____��
��4����һ�������£�����������Ȳ�Ƶã�д����Ȳ��������H2�ڼ��ȼ�ѹ��Ni�������������·�Ӧ��������Ļ�ѧ����ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1mol CH2=CH��CH2CH3��Cl2��ȫ�����ӳɷ�Ӧ������Cl2����ȡ���������̹�����Cl2�����ʵ���Ϊ�� ��
A. 9mol B. 5mol C. 7mol D. 8mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com