
【题目】铂钴合金是以铂为基含钴二元合金,在高温下,铂与钴可无限互溶,其固体为面心立方晶格。铂钴合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过____方法区分晶体准晶体和非晶体。
(2)基态F原子的价层电子排布图(轨道表达式)为______。
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为______,与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是______(各举一例)。
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是______;氟化铵中存在______(填字母)。
A.离子键B.σ键C.π键D.氢键
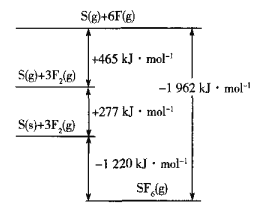
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为______kJmol-1,S-F键的键能为______kJmol-1。
(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1gcm-3。
①CuF的熔点比CuCl的高,原因是______
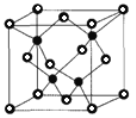
②已知NA为阿伏加德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=______nm(列出计算式)。
【答案】X-射线衍射 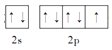 V形 H2O、NH2- sp3 AB 155 327 CuCl为分子晶体,CuF为离子晶体
V形 H2O、NH2- sp3 AB 155 327 CuCl为分子晶体,CuF为离子晶体 ![]() ×107
×107
【解析】
(1)晶体对X射线发生衍射,非晶体不发生衍射,准晶体介于二者之间;
(2)F的原子序数为9,价电子排布式为2s22p5;
(3)根据等电子体原理分析解答;
(4)NH4+的N原子形成4个σ键,没有孤电子对;氟化铵为离子化合物,含有离子键和共价键;
(5)由图象可知,断裂3molF-F键,吸收465kJ能量,形成6molS-F键,放出1962kJ能量,据此计算;
(6)①CuCl熔化时几乎不导电,应为分子晶体,而CuF为离子晶体;②根据均摊法计算晶胞中含有的Cu、F的数目,再结合晶体的密度列式计算。
(1)从外观无法区分晶体、准晶体和非晶体,但用X光照射会发现:晶体对X射线发生衍射,非晶体不发生衍射,准晶体介于二者之间,因此通过X-射线衍射实验可区分晶体、准晶体和非晶体,故答案为:X-射线衍射;
(2)F的原子序数为9,价电子排布式为2s22p5,因此基态F原子的价电子排布图为 ,故答案为
,故答案为 ;
;
(3)[H2F]+与H2O、NH2-等互为等电子体,结构相似,为V形,故答案为:V形;H2O、NH2-;
(4)NH4+的N原子形成4个σ键,没有孤电子对,采用sp3杂化,氟化铵为离子化合物,含有离子键和共价键,即σ键,故选AB,故答案为:sp3;AB;
(5)由图象可知,断裂3molF-F键,吸收465kJ能量,则F-F键的键能为155kJmol-1,形成6molS-F键,放出1962kJ能量,则S-F的键能为![]() kJmol-1=327kJmol-1,故答案为:155;327;
kJmol-1=327kJmol-1,故答案为:155;327;
(6)①CuCl的熔点为426℃,熔化时几乎不导电,应为分子晶体,而CuF为离子晶体,一般,离子晶体的熔沸点比分子晶体高,则CuF比CuCl熔点高,故答案为:CuCl为分子晶体,CuF为离子晶体;
②CuF的密度为7.1gcm-3,晶胞中Cu、F的个数分别为4,(其中○为8×![]() +6×
+6×![]() =4),则晶胞的密度=
=4),则晶胞的密度= gcm-3=7.1gcm-3,a=
gcm-3=7.1gcm-3,a=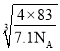 ×107nm,故答案为:
×107nm,故答案为: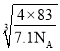 ×107。
×107。


科目:高中化学 来源: 题型:
【题目】①一种二肽的结构简式为: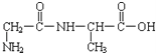 ,合成这种二肽的氨基酸是___和___;
,合成这种二肽的氨基酸是___和___;
②生活中有大量的铝制品。家用铝锅不能用热碱水洗涤去污,原因是(用离子方程式表示)____;
③大量使用塑料制品产生的污染称之为_____,防治该污染的有效措施之一是进行回收利用,将回收后的塑料进行____,可以获得乙烯、丙烯等化工原料;
④传统生产水泥的原料中除了石灰石、粘土外,还经常添加____,以调节水泥的硬化速度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的气化和液化是现代能源工业中重点考虑的综合利用技术。最常见的气化方法是用煤作原料生产水煤气,而比较流行的液化方法是煤在催化剂等条件下生产CH3OH。
已知制备甲醇的有关化学反应如下:
①CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H1=-90.8 kJmol-1
②CO(g)+H2O(g)CO2(g)+H2(g)△H2=-412 kJmol-1
③CO(g)+2H2(g)CH3OH(g)△H3
I.回答下列问题:
(1)欲提高甲醇的产率,可以采取的措施有______(填字母序号)。
A.升高温度
B.增大压强
C.降低温度
D.降低压强
(2)提高甲醇反应选择性的关键因素是______。
(3)保持温度和容积不变,下列描述能说明反应③达到平衡状态的是______(填字母序号)。
A.v(CO):v(H2):v(CH3OH)=1:2:1
B.混合气体的压强不再随时间的变化而变化
C.单位时间内断裂2 mol H-H键,同时生成3mol C-H键
D.一段时间内的平均反应速率等于0
E.混合气体的平均摩尔质量保持不变
Ⅱ.在一密闭容器中投入1mol CO和2molH2发生反应③,实验测得平衡时甲醇的物质的量随温度、压强变化关系如图1所示:

(1)压强P1______P2(填“>”、“<“或”=”)。
(2)M、N两点的化学反应速率:vM______vN(填“>”、“<“或“=”)
(3)对于气相反应,用某组分B的平衡压强P(B)代替物质的量浓度c(B)也可表示平衡常数(Kp),则M点时,平衡常数Kp=______(P1=5 MPa)。
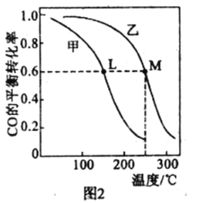
(4)甲、乙两个恒容密闭容器的体积相同,向甲中加入 1molCO和 2mol H2,向乙中加入2mol CO和4molH2,测得不同温度下CO的平衡转化率如图2所示,则L、M两点容器内压强:P(M)______2P(L),平衡常数:K(M)______K(L)(填“>”、“>”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A、B、C和D互为同分异构体,分子量为136,分子中只含碳、氢、氧,其中氧的含量为23.5%。实验表明:化合物A、B、C和D均是一取代芳香化合物,其中A、C和D的芳环侧链上只含一个官能团。4个化合物在碱性条件下可以进行如下反应:
A![]() E(C7H6O2)+F
E(C7H6O2)+F
B![]() G(C7H8O)+H
G(C7H8O)+H
C![]() I(芳香化合物)+J
I(芳香化合物)+J
D![]() K+H2O
K+H2O
请回答下列问题:
(1)写出A、B、C和D的分子式:__,C的结构简式:__,写出H分子中官能团的名称:__。
(3)按要求写出下列化学反应方程式及反应类型:
①E和G反应:__,反应类型__。
②I和浓溴水反应:___。
(4)A的同分异构体有多种,写出符合下列条件的A的所有同分异构体的结构简式__。
①遇FeCl3溶液显紫色;②可发生银镜反应;③苯环上仅含两个支链。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B. CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol
C. 需要加热才能发生的反应一定是吸热反应
D. 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]环丙贝特(H)是一种降血脂药物,可明显降低极低密度和低密度脂蛋白水平,并升高高密度脂蛋白,通过改善胆固醇的分布,可减少CH和LDL在血管壁的沉积,还有溶解纤维蛋白和阻止血小板凝聚作用。如图是合成环丙贝特的一种新方法:
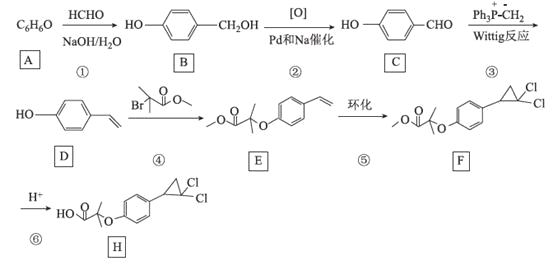
回答下列问题:
(1)C的化学名称为______________________
(2)F中含氧官能团的名称为______________
(3)H的分子式为________________________
(4)反应①的反应类型为___________,反应④的化学方程式为______________________
(5)M为![]() 的同分异构体,能与NaHCO3溶液反应产生气体,则M的结构共有种____(不考虑立体异构);其中1HNMR中有3组峰,且峰面积之比为6:2:1的结构简式为_______
的同分异构体,能与NaHCO3溶液反应产生气体,则M的结构共有种____(不考虑立体异构);其中1HNMR中有3组峰,且峰面积之比为6:2:1的结构简式为_______
(6)利用Wittig反应,设计以环己烷为原料(其他试剂任选),制备![]() 的合成路线:______________________。
的合成路线:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3DZn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3DZn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。下列说法错误的是
ZnO(s)+2Ni(OH)2(s)。下列说法错误的是
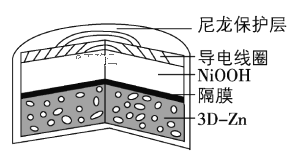
A.三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B.放电过程中OH通过隔膜从负极区移向正极区
C.充电时阴极反应为ZnO(s)+H2O(l) +2e= Zn(s)+2OH(aq)
D.放电时正极反应为NiOOH(s)+H2O(l) +e =Ni(OH)2(s)+OH(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科研人员借助太阳能,将H2S转化为可再利用的S和H2的工作原理如图所示。下列叙述错误的是( )

A.该电池能实现将光能转化为化学能
B.a电极的电极反应:2H++2e-=H2↑
C.光照后,b电极的电极反应:H2S-2e-=2H++S
D.a电极区溶液的pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性硼化钒(VB2)-空气电池工作时反应为:4VB2 +11O2![]() 4B2O3 +2V2O5 。用该电池为电源,选用惰性电极电解一定量的硫酸铜溶液,实验装置如图所示。当电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标况),则下列说法中正确的是
4B2O3 +2V2O5 。用该电池为电源,选用惰性电极电解一定量的硫酸铜溶液,实验装置如图所示。当电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标况),则下列说法中正确的是

A. VB2电极发生的电极反应为: 2VB2+11H2O – 22e![]() V2O5+2B2O3+22H+
V2O5+2B2O3+22H+
B. 外电路中电子由c电极流向VB2电极
C. 电解过程中,b电极表面先有红色物质析出,然后有气泡产生
D. 若B装置内的液体体积为200mL,则CuSO4溶液的浓度为0.05mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com