
【题目】已知伞形酮可用雷琐苯乙酮和苹果酸在一定条件下反应制得

下列说法中正确的是( )
A.1mol雷琐苯乙酮最多能与3mol氢气发生加成反应
B.两分子苹果酸的一种缩合产物是:![]()
C.1mol产物伞形酮与溴水反应,最多可消耗3mol Br2,均发生取代反应
D.反应中涉及到的三种有机物都能跟FeCl3溶液发生显色反应
 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.电解精炼铜时,阳极泥中含有![]() 等金属
等金属
B.![]() 通入足量水中,转移电子的数目为
通入足量水中,转移电子的数目为![]()
C.反应![]() 在常温下不能自发进行,说明该反应的
在常温下不能自发进行,说明该反应的![]()
D.等质量的硫蒸气和硫粉分别在空气中完全燃烧,前者放出热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】疫情期间某同学尝试在家自制含氯消毒剂。用两根铅笔芯(C1和C2)、电源适配器和水瓶组装如图所示的装置。接通电源观察到:C1周围产生细小气泡,C2周围无明显现象;持续通电一段时间后,C2周围产生细小气泡。此时停止通电,拔出电极,旋紧瓶塞,振荡摇匀,制备成功。关于该实验的说法不正确的是

A.C1电极产生气泡原因:2H2O+2e-= H2↑+2OH-
B.自制消毒剂的总反应为:NaCl+H2O![]() NaClO+H2↑
NaClO+H2↑
C.可以用两根铁钉代替铅笔芯完成实验
D.实验过程中要注意控制电压、开窗通风、导出氢气,确保安全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗肿瘤药物7–氟喹啉衍生物的前体Q的合成路线如下:
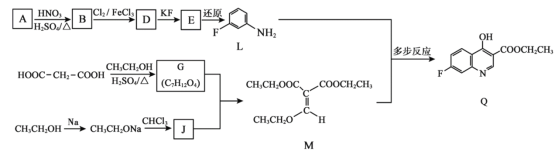
已知:R1ONa+R2C1→R1OR2+NaCl(R1、R2代表烃基)
(1)A属于芳香烃,A的名称是_______。
(2)B→D的化学方程式是_______。
(3)D→E的反应类型是_______。
(4)G的结构简式是_______。
(5)下列关于M的说法正确的是_______(填序号)。
a.M含有两种不同的官能团 b.M存在顺反异构体
c.M和G能用Br2的CCl4溶液鉴别 d.M能与NaOH溶液反应
(6)已知:G + J → M + 2CH3CH2OH。J的结构简式是_________。
(7)L与M反应生成Q的过程如下:

已知:上述异构化反应中,只存在氢原子和不饱和键的位置变化。Y的分子中含有两个六元环。Y的结构简式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习小组探究AgNO3、Ag2O(棕黑色固体,难溶于水)对氯水漂白性的影响。
实验记录如下:
| 实验 | 方案和现象 |
ⅰ | 加入1mL蒸馏水,再滴加1滴品红溶液,品红溶液较快褪色 | |
ⅱ | 加入少量Ag2O固体,产生白色沉淀a。再加入1mL蒸馏水和 1滴品红溶液,品红溶液褪色比i快 | |
ⅲ | 加入1mL较浓AgNO3溶液,产生白色沉淀b。再滴加1滴品红溶液,品红溶液褪色比i慢 |
(1)用离子方程式表示i中品红溶液褪色的原因:______。
(2)经检验,ii中的白色沉淀a是AgCl。产生AgCl的化学方程式是_______。
(3)ⅰ是iii的对比实验,目的是排除iii中______造成的影响。
(4)研究白色沉淀b的成分。进行实验iv(按实验iii的方案再次得到白色沉淀b,过滤、洗涤,置于试管中):
实验iv:
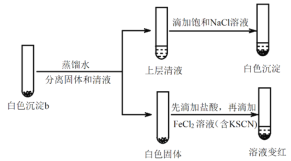
①设计对比实验证实白色沉淀b不只含有AgCl,实验方案和现象是_______。
②FeCl2溶液的作用是_______。由此判断,白色沉淀b可能含有AgClO。
(5)进一步研究白色沉淀b和实验iii品红溶液褪色慢的原因,进行实验v:
实验v:

①结合离子方程式解释加入饱和NaCl溶液的目的:_______。
②推测品红溶液褪色的速率:实验iii比实验v______(填“快”或 “慢”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,三个容积相同的烧瓶内分别充满了干燥的NH3、HCl、NO2气体,然后分别用水作喷泉实验,假设烧瓶内的溶质不散逸,则三种溶液的物质的量浓度之比为 ( )
A. 无法比较B. 2∶2∶3C. 3∶3∶ 2D. 1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设nA为阿伏伽德罗常数的数值,下列说法正确的是
A. 23g Na 与足量H2O反应完全后可生成nA个H2分子
B. 1 molCu和足量热浓硫酸反应可生成nA个SO3分子
C. 标准状况下,22.4L N2和H2混合气中含nA个原子
D. 3mol单质Fe完全转变为Fe3O4,失去8nA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。
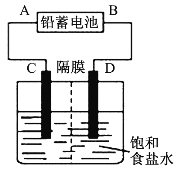
铅蓄电池充、放电时的电池反应为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O
2PbSO4+2H2O
(1)铅蓄电池放电时的正极反应为___。
(2)请写出电解饱和食盐水的化学方程式:____。
(3)若在电解池C极一侧滴入几滴酚酞溶液,电解一段时间后溶液变红色,说明铅蓄电池的A极为___极。
(4)用铅蓄电池电解1L饱和食盐水(食盐水足量、密度为1.15g·cm-3)时,
①若收集到11.2L(标准状况下)氯气,则至少转移电子____mol。
②若铅蓄电池消耗2molH2SO4,则可收集到H2的体积(标准状况下)为___L。
③若蓄电池消耗amol硫酸,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气和氢气全部排出)___(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置.下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C. 无论a和b是否连接,铁片均会溶解
D. a和b用导线连接后,Fe片上发生还原反应,溶液中的Cu2+向铜电极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com