
【题目】某小组设计如图装置,用![]() 与
与![]() 反应制取氢化钙
反应制取氢化钙![]() 。下列有关该实验的说法不正确的是( )
。下列有关该实验的说法不正确的是( )
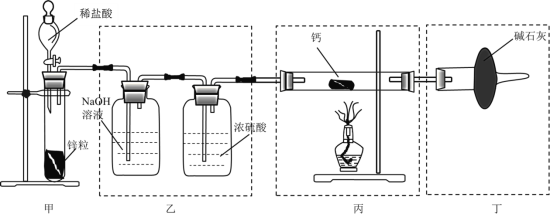
A.甲中若将稀盐酸改为稀硫酸,装置乙中装![]() 溶液的洗气瓶可舍去
溶液的洗气瓶可舍去
B.装置丁中碱石灰的作用是防止外界的水蒸气与二氧化碳进入
C.实验时应先通一段时间氢气,检验尾气纯度后再点燃酒精灯加热
D.取少量反应后固体与水反应,通过观察是否有气体产生来判断产物是否为![]()
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】某学生课外活动小组利用下图所示装置分别做如下实验:
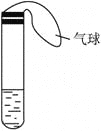
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________溶液;加热时溶液由红色逐渐变浅的原因是________________。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________溶液;加热时溶液由无色变为红色的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有原子序数依次增大的a、b、c、d四种元素,最外层电子数分别为4、1、x、7,已知c原子的电子层数等于x,d-的电子层结构与Ar元素相同。下列说法错误的是( )
A.元素a与氢形成原子比为1:1的化合物有多种
B.元素b的单质能与水、无水乙醇反应
C.c的简单离子与d-的简单离子最外层电子数和电子层数都不相同
D.元素a与元素d可形成既含有极性共价键又含非极性共价键的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥司他韦是一种高效、高选择性神经氨酸酶抑制剂,是目前治疗流感的最常用药物之一,是公认的抗禽流感、甲型H1N1等病毒最有效的药物之一。其合成路线如图所示:
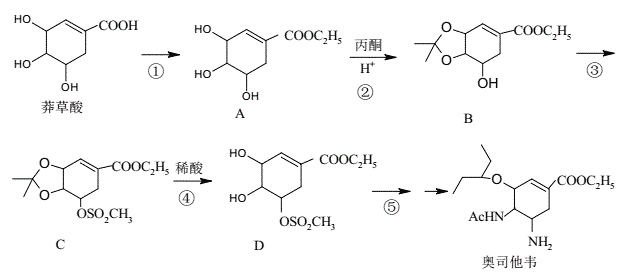
回答下列问题:
(1)莽草酸的含氧官能团名称有__;反应③的反应类型__。
(2)反应①的反应试剂和反应条件__。
(3)1molB最多可以消耗___molNaOH溶液。
(4)请写出反应②的化学方程式__。
(5)芳香化合物X是B的同分异构体,则符合官能团只含酚羟基的X有___种。
(6)设计由对甲基苯甲醛制备对醛基苯甲酸![]() 的合成路线__。
的合成路线__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将![]() 和
和![]() 两种酸溶液分别加水稀释至体积为
两种酸溶液分别加水稀释至体积为![]() ,稀释液
,稀释液![]() 与其体积变化的关系如图所示。下列说法正确的是 ( )
与其体积变化的关系如图所示。下列说法正确的是 ( )

A.![]() 和
和![]() 均为一元弱酸
均为一元弱酸
B.常温下,浓度均为![]() 的
的![]() 和
和![]() 溶液,溶液
溶液,溶液![]()
C.![]() 、
、![]() 两点对应溶液中一定存在:
两点对应溶液中一定存在:![]()
D.分别往![]() 、
、![]() 两点对应溶液中滴加
两点对应溶液中滴加![]() 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗![]() 溶液的体积相等
溶液的体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吗氯贝胺是新一代缓和的抗抑郁药物,某研究小组设计如图合成路线:
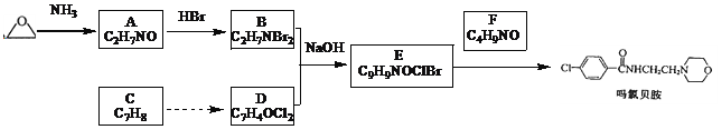
已知:①R-Br![]()
②R-COOH![]() R-COCl
R-COCl![]() R-CONHR′
R-CONHR′
③苯环上连羧基时,苯环上再取代主要生成间位取代产物。
按要求回答下列问题:
(1)化合物![]() 的结构简式________。
的结构简式________。
(2)下列有关说法正确的是________。
A.吗氯贝胺的分子式为![]()
B.在水中溶解能力![]() ,原因是
,原因是![]() 与水分子间可形成氢键
与水分子间可形成氢键
C.![]() 的反应中
的反应中![]() 的作用是反应产生氨基及中和反应产生的酸
的作用是反应产生氨基及中和反应产生的酸
D.![]() 吗氯贝胺的反应类型为取代反应
吗氯贝胺的反应类型为取代反应
(3)写出![]() 的反应方程式________。
的反应方程式________。
(4)![]() 与
与![]() 反应制备吗氯贝胺中加适量碳酸钾或过量
反应制备吗氯贝胺中加适量碳酸钾或过量![]() 均有利于提高产率,用反应方程式解释加过量
均有利于提高产率,用反应方程式解释加过量![]() 有利于提高产率的原因________。
有利于提高产率的原因________。
(5)设计![]() 的合成路线(用流程图表示,无机试剂任选)________。
的合成路线(用流程图表示,无机试剂任选)________。
(6)写出化合物![]() 同时符合下列条件的同分异构体的结构简式________。
同时符合下列条件的同分异构体的结构简式________。
①![]() 谱检测表明:分子中有3种氢原子;
谱检测表明:分子中有3种氢原子;
②![]() 谱检测表明:分子中存在
谱检测表明:分子中存在![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在中和热测定的实验中,以下操作正确的是:( )
①只在大烧杯底部垫泡沫塑料,使放入的小烧杯杯口与大烧杯杯口相平,再盖上硬纸板
②温度计测量过盐酸的温度后,立即插入![]() 溶液中测量
溶液中测量![]() 溶液的温度
溶液的温度
③将量筒中的![]() 溶液慢慢加入到小烧杯的盐酸中,边加边搅拌
溶液慢慢加入到小烧杯的盐酸中,边加边搅拌
④读取混合溶液的最高温度和最低温度,以其平均值记为最终温度.
A.只有①正确B.只有②正确
C.只有①④正确D.都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是一种丰富的资源,工业上可从海水中提取多种物质,广泛应用于生活、生产、科技等方面。如图是某工厂对海水资源进行综合利用的示意图。

回答下列问题:
(1)流程图中操作a的名称为____。
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。
①气体A、B是CO2或NH3,则气体A应是_____(填化学式)
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品NH4Cl晶体,则通入NH3的作用是____。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_____。
②操作b是在___氛围中进行,若在空气中加热,则会生成Mg(OH)Cl,写出有关反应的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子、元素、核素、同位素等都属于重要的化学基本概念。下列八种化学符号:![]() H、
H、![]() H、
H、![]() C、
C、![]() Li、
Li、![]() Na、
Na、![]() N、
N、![]() Li、
Li、![]() Mg
Mg
(1)涉及的核素共有__种;
(2)互为同位素的是__、__;
(3)质量数相等,但不能互称为同位素的是__;
(4)中子数相等,但质子数不相等的是__。
(5)氢的三种同位素是__,它们与氯的同位素35Cl、37Cl相互结合为氯化氢,可得氯化氢分子的种数为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com