
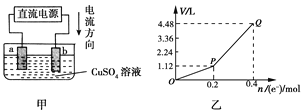
����Ŀ���ö��Ե缫���һ����������ͭ��Һ��ʵ��װ������ͼ�ס��������е�ʵ����������ͼ�ң��������ʾ��������ת�Ƶ��ӵ����ʵ������������ʾ�������в������������ ��(��״��)��������˵������ȷ����
A. �������У�a�缫�������к�ɫ�����������������ݲ���
B. b�缫�Ϸ�����Ӧ�ķ���ʽΪ��4OH����4e��=2H2O��O2��
C. ����O��P�α�ʾO2������仯
D. �ӿ�ʼ��Q��ʱ�ռ����Ļ�������ƽ��Ħ������Ϊ12 g/mol
���𰸡�D
����������ͼ��֪��������������������bΪ������aΪ���������Ե缫���һ����������ͭ��Һ������2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4�����ͼ2��֪��ͨ��0.2mol����ʱ�������ͭ��Ȼ����������Һ������2H2O
2Cu+O2��+2H2SO4�����ͼ2��֪��ͨ��0.2mol����ʱ�������ͭ��Ȼ����������Һ������2H2O![]() 2H2��+O2����
2H2��+O2����
A��aΪ�������ȷ���Cu2++2e���TCu������2H++2e���TH2����a�缫�������к�ɫ�����������������ݲ�������A��ȷ��
B��bΪ��������Һ�е����������ӷŵ磬��b�缫�Ϸ����ķ�Ӧ����ʽΪ��4OH����4e���TH2O+O2����B��ȷ��
C��������������֪������0��P�α�ʾO2������仯������P��Q�α�ʾH2��O2������������仯����C��ȷ��
D������0��P�α�ʾO2������仯��P��1.12LΪO2�������ʵ���Ϊ0.05mol��PQ��3.36L�����У��ɵ��ˮ��Ӧ��֪0.2mol����ͨ��ʱ����0.1mol H2��0.05mol O2����ӿ�ʼ��Q���ռ����Ļ��������O2Ϊ0.1mol��HΪ0.1mol���ʻ�������ƽ��Ħ������Ϊ![]() =17gmol��1����D����ѡ��D��
=17gmol��1����D����ѡ��D��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��DΪ������Ԫ�أ��˵��������������A��B��C����Ԫ�ص�ԭ�Ӻ�����Ӳ���֮��Ϊ5����֪A��ԭ�ӽṹ���Ԫ�أ�BԪ��ԭ��������ϵĵ�����������Ӳ�����2����A��C֮����γ�A2C��A2C2���ֻ����D��ͬ��������Ԫ����ԭ�Ӱ뾶�����ش��������⡣
(1)CԪ����Ԫ�����ڱ��е�λ����____________��C��D����Ԫ�����γɵļ����ӣ����Ӱ뾶�ɴ�С��˳����________________��(�����ӷ��ű�ʾ)
(2)д��A2C2�ĵ���ʽ__________��
(3)�ں����£����Ϊ2 L�ĺ��������м���һ������B���ʺ�1 mol A2C������������B(s)��A2C(g) BC(g)��A2(g)��2 min��������ѹǿ������20%����2 min��A2C�ķ�Ӧ����Ϊ________��һ��ʱ���ﵽƽ�⣬����˵����ȷ����__________��
A.����B���ʵ�������Ӧ���ʼӿ�
B.���º���ʱ�ڸ�������ͨ��Ar����Ӧ���ʼӿ�
C.������ܶȲ��ٱ仯�����жϸ÷�Ӧ�ﵽ��ƽ��
D.2 minʱ��A2C��ת����Ϊ80%
E.�����ƽ��Ħ����������ʱ���÷�Ӧ�ﵽƽ��
(4)BC��C2��DCA��Һ�п��γ�һ��ȼ�ϵ�ء��õ�صĸ�����ӦʽΪ��___________��
(5)��0.2 mol D2C2Ͷ�뵽����0.1 mol FeCl2��ˮ��Һ��ǡ�ó�ַ�Ӧ����Ӧ���ܻ�ѧ����ʽΪ��______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ� ��
A.���ʵ����������ʵ�����
B.���ʵ����������ʵ�����
C.���ʵ�������Ħ��
D.���ʵ����ĵ�λ��Ħ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ӫ��Ԫ��֮һ������������Ȼ���й㷺���ڣ�ѭ����ϵ����ͼ��ʾ:
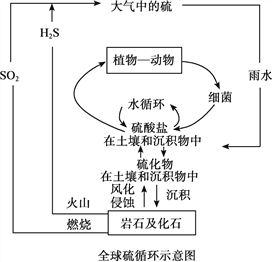
��1����ɽ�緢����H2S�ڴ������з������·�Ӧ��
��2H2S��g��+O2��g��=2S��g��+2H2O��g�� ��H=��442.38kJ/mol
��S(g)+O2(g)=SO2(g) ��H=��297.04kJ/mol��
H2S��g����O2(g)��Ӧ����SO2(g)��H2O��g�����Ȼ�ѧ����ʽ��__________��
��2����Ȼ��ر���ԭ��ͭ�����ᆳ�������������ú���CuSO4��Һ�������������������ܵ�ZnS������ת��Ϊͭ����CuS������ӳ����ܽ�ƽ��ĽǶȽ�����ZnSת��ΪCuS�Ĺ���__________��
��3����ʯȼ��ȼ��ʱ�������SO2�ķ��������������Ⱦ�������ж��ַ���������SO2���ѳ���
�ٰ������÷�����һ�ָ�Ч�ͺ��ܵ�ʪ������ʽ�����ð�ˮ���շ����е�SO2�����ڸ�������������Ϊ����泥��õ����ʲ�Ʒ����Ӧ�Ļ�ѧ����ʽ��__________��
��NaClO������Һ���շ�����ҵ�Ͽ���NaClO������Һ����SO2����Ӧ���ӷ���ʽ��__________��Ϊ���������Ч�ʣ�����Ni2O3��Ϊ�������ڷ�Ӧ�����в������ļ�����ԭ�������м�ǿ����������,�ɼӿ��SO2�����ա��ô����̵�ʾ��ͼ����ͼ��ʾ��
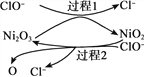
����1��Ni2O3 +ClO- = 2NiO2 +Cl-������2�����ӷ���ʽ��__________��
Ca(ClO)2Ҳ����������������Ч����NaClO���ã�ԭ����__________��
�۵绯ѧ����ij�ֵ绯ѧ����װ������ͼ��ʾ���������ѳ�SO2���ɵõ�Cu���������з����ܷ�Ӧ�����ӷ���ʽ��__________��
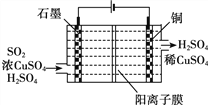
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���Ʊ����跴Ӧ���Ȼ�ѧ����ʽ���£�SiCl4��g��+2H2��g��Si��s��+4HCl��g����H=+QkJ/mol��Q��0��ij�¶ȡ�ѹǿ�£���һ������Ӧ��ͨ���ܱ���������������Ӧ������������ȷ���ǣ�������
A.��Ӧ�����У�������ѹǿ�����SiCl4��ת����
B.����Ӧ��ʼʱSiCl4Ϊ1 mol�����ƽ��ʱ����������ΪQ kJ
C.��Ӧ��4 minʱ����HClŨ��Ϊ0.12 mol/L����H2�ķ�Ӧ����Ϊ0.03 mol/��Lmin��
D.��Ӧ����0.025Q kJ����ʱ�����ɵ�HClͨ��100 mL 1 mol/L��NaOH��Һ��ǡ����ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��a��b������̼��������������ȷ���ǣ������� 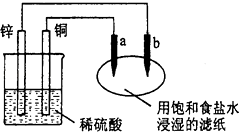
A.a��������������ԭ��Ӧ
B.b�Ǹ���������������Ӧ
C.�μӷ�̪��Һ��b��������Һ��ɫ���
D.ͭƬ�ϵĵ缫��Ӧʽ�ǣ�Cu2++2e��Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϣ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У� ��CH4��g��+H2O��g��CO��g��+3H2��g����H1=206.1kJmol��1
��CH4��g��+CO2��g��2CO��g��+2H2��g����H2=247.3kJmol��1
��CO��g��+H2O��g��CO2��g��+H2��g����H3
��ش��������⣺
��1����һ�ܱ������н��з�Ӧ�٣����CH4�����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ����Ӧ���е�ǰ5min�ڣ�v��H2��=��10minʱ���ı��������������� �� 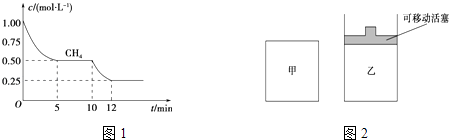
��2����ͼ2��ʾ���ڼס����������зֱ��������ʵ�����CH4��CO2 �� ʹ�ס�����������ʼ�ݻ���ȣ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䣮 �ٿ����жϼ������з�Ӧ�Ѵ�ƽ��״̬���� ��
a������CH4������������CO�����ʵ�2��
b��������ѹǿ���ֲ���
c��������������ܶȱ��ֲ���
d�������ڸ������Ũ�ȱ��ֲ���
�ڼ����������з�Ӧ�ﵽƽ��ʱ������˵����ȷ���� ��
a����ѧ��Ӧ���ʣ�v ���ף���v ���ң�
b�������ת���ʣ������ף��������ң�
c��ѹǿ��P���ף�=P ���ң�
��3����Ӧ���С�H3= kJmol��1 �� 800��ʱ����Ӧ�۵Ļ�ѧƽ�ⳣ��K=1.0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ����������
CO | H2O | CO2 | H2 |
0.5mol | 8.5mol | 2.0mol | 2.0mol |
��ʱ��Ӧ���������淴Ӧ���ʵĹ�ϵ��������ţ���
a��v��������v ���棩 b��v��������v���棩 c��v������=v���棩 d�����жϣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һƿA��B�Ļ��Һ����֪���ǵ����������
���� | �۵�/�� | �е�/�� | �ܶ�/gcm��3 | �ܽ��� |
A | ��11.5 | 198 | 1.11 | A��B���ܣ��Ҿ�������ˮ |
B | 17.9 | 290 | 1.26 |
�ݴ˷�������A��B����ij��÷����ǣ� ��
A.����
B.��Һ
C.����
D.����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com