
����Ŀ��ijʵ��С��������װ�ý����Ҵ���������ʵ�飬��ش��������⣺
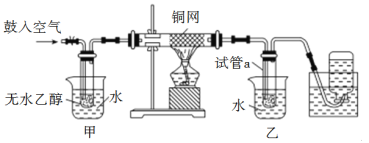
��1����д��ͭ����������Ӧ�Ļ�ѧ��Ӧ����ʽ_____________����Ϩ��ƾ��ƣ����ϵع����������Ӧ���ܼ������У�˵���÷�Ӧ��_______��Ӧ������ȡ����ȡ�����
��2������������ˮԡ�����ò���ͬ����������_____________��
��3����Ӧ����һ��ʱ�����ƿ���ռ������������Ҫ�ɷ���__________��
��4�����Թ�a���ռ�����Һ����ʪ�����ɫʯ����ֽ���飬��ֽ�Ժ�ɫ���Ʋ�ʵ���з�Ӧ��������һ���л�������ø�����Ϊ_______����ṹ��ʽ����Ҫ��ȥ�����ʣ������ڻ��Һ�м���_______������ĸ��ţ���Ȼ����ͨ��_______����������ƣ����ɳ�ȥ��
a���Ȼ�����Һ b���� c��̼��������Һ d�����Ȼ�̼
���𰸡� 2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O ���� ʹҺ̬�Ҵ�ת��Ϊ�Ҵ����� �������� N2�� CH3COOH c ����
2CH3CHO+2H2O ���� ʹҺ̬�Ҵ�ת��Ϊ�Ҵ����� �������� N2�� CH3COOH c ����
��������(1)�Ҵ���ͭ������������������������ȩ,���ڼ�����������Ӧ,����ʽΪ��2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O��Ϩ��ƾ���,��Ӧ���ܼ�������,˵���÷�Ӧ�Ƿ��ȷ�Ӧ��
2CH3CHO+2H2O��Ϩ��ƾ���,��Ӧ���ܼ�������,˵���÷�Ӧ�Ƿ��ȷ�Ӧ��
(2)�����Ҵ�����ȩ���������������߶����ӷ����Ҵ��Ƿ�Ӧ����Ӧת�����Ҵ��������뵽Ӳ���Թ��ڲ��뷴Ӧ����ȩ�Dz���,�����¶�ʹ��ת����Һ̬������ǰ������ˮԡ����������ˮԡ��
(3)���е�ˮΪ��ˮ�ܽ�δ��Ӧ���Ҵ��ͷ�Ӧ���ɵ���ȩ�Լ�ˮ��������ΪҺ̬��������ȴ���������������������뼯��ƿ����
(4)����ʹ��ɫʯ����ֽ�Ժ�ɫ������������ͨ�������ֻ������ʵķ�����Բ���������
���:(1) ͭ�����Ҵ������������Ļ�ѧ����ʽΪ��2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O��Ϩ��ƾ���,��Ӧ���ܼ�������,˵���÷�Ӧʱһ�����ȷ�Ӧ��
2CH3CHO+2H2O��Ϩ��ƾ���,��Ӧ���ܼ�������,˵���÷�Ӧʱһ�����ȷ�Ӧ��
��ˣ�������ȷ������2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O��������
2CH3CHO+2H2O��������
(2)���ݷ�Ӧ���̿���֪��:�ڼ״�����ˮԡ����ʹ�Ҵ��ӷ�������е��������,��������һ����Ӧ��
��ˣ�������ȷ������ʹҺ̬�Ҵ�ת��Ϊ�Ҵ�������
(3) ��Ӧ����һ��ʱ�������δ��Ӧ���Ҵ��ͷ�Ӧ���ɵ���ȩ��װ�����б�����ΪҺ̬�����Լ���ƿ���ռ�����������δ��Ӧ�������Ϳ����еĵ�����������Ҫ�ɷ�Ϊ������
��ˣ�������ȷ�������������� N2����
(4)������ʹ��ɫʯ����ֽ�Ժ�ɫ,����������ͨ��,������̼���������������Ĵ���,���Ƿ������ɫ��ζ����������, Ҫ��ȥ�����ʣ������ڻ��Һ�м���̼��������Һ��������Ӧ��NaHCO3+CH3COOH=CH3COONa+H2O+CO2����Ȼ����������ȩ�ķе�ͣ�ͨ�����ɳ�ȥ��
��ˣ�������ȷ������CH3COOH ��c��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Rn+���Ӻ�����m�����ӣ���ԭ�Ӻ��ڵ�������Ϊ�� ��
A.m + nB.mC.nD.m-n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ���������Ǵ������������Ҫ�ɷ�,�о��仯ѧ��ɶ�������������Ⱦ�����ش����壬ij�������������ᆳ�������Ҫ��Ԥ�������������Һ��������ɫ����ȷ��������������NH4+��Na+��Mg2+��Ca2+��Al3+��SO42-��NO3-��CO32-��Cl-��ijͬѧ�����ٽ������µ�ʵ��:
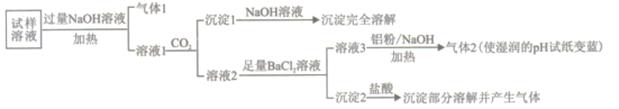
��֪���ڼ�����ǿ����������,�����ʿ��Խ�NO3-��ԭΪ������
�ش���������:
��1��������1���ĵ���ʽΪ_________��
��2������������1�������ӷ���ʽΪ________��
��3��������2���ijɷ���___________(�ѧʽ)��
��4������Һ3![]() ����2�������ӷ���ʽΪ_________��
����2�������ӷ���ʽΪ_________��
��5����������ʵ����ƶϸõ���������������__________�����ϵ�(�����ӷ���)��
��6����֪�����������и�Ԫ�ص���Ⱦ�������±�:
Ԫ�� | N | S | Na��Mg��Cl | Al | Ca |
��Ⱦ���� | ������β�� | ȼú��Ⱦ | �������� | �����ﳾ | �����۳� |
����ʵ�������жϸõ���������������Ⱦ������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧѧϰС���������ʵ�飮
��̽����Ӧ���ʵ�Ӱ�����ء���������µķ�������¼ʵ������������Һ�������� ��������ѡ�Լ���������0.20mol/LH2C2O4��Һ��0.010mol/LKMnO4��Һ�����ԣ�������ˮ���Թܡ���Ͳ�����������ˮԡ��
������ | V��0.20mol/H2 | V������ˮ��/mL | V��0.010mol/L KMnO4��Һ��/mL | T/�� | �� |
�� | 2.0 | 0 | 4.0 | 50 | |
�� | 2.0 | 0 | 4.0 | 25 | |
�� | 1.0 | a | 4.0 | 25 |
��1������ʵ��٢���̽���Ի�ѧ��Ӧ���ʵ�Ӱ�죻������ʵ��ڢ���̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬�� a Ϊ������ʵ����Ҫ����������������� ���С��ҡ�Ӧ��д ��
��2�����ⶨ H2C2O4xH2O �� x ֵ����֪��M��H2C2O4��=90g/mol
�ٳ�ȡ 1.260g �����ᾧ�壬�������Ƴ� 100.00mL ˮ��ҺΪ����Һ��
��ȡ 25.00mL ����Һ������ƿ�У��ټ����ʵ�ϡ H2SO4
����Ũ��Ϊ 0.05000molL��1 �� KMnO ����Һ���еζ���
��д����ζ��йط�Ӧ�����ӷ���ʽ
��3��ijѧ���ĵζ���ʽ���гֲ�����ȥ����ͼ1�������������ѡ�� a��b����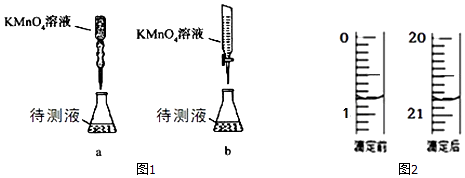
��4����ͼ2��֪���� KMnO4��Һ���ΪmL��
��5���ζ��������۾�Ӧע����
��6��ͨ���������ݣ���� x= �� �Ա� KMnO4��Һ�ζ���Ʒ��Һ��Ũ�ȣ�δ�ñ� KMnO4��Һ��ϴ�ζ��ܣ�����ʵ������ƫ��ƫС��û��Ӱ�죩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H2CO3��H2SO3�ĵ��볣�����±�:
�� | Ka1 | Ka2 |
H2CO3 | 4.27��10-7 | 5.61��10-11 |
H2SO3 | 1.54��10-2 | 1.02��10-7 |
��10mL0.1mol/LNa2CO3��Һ�еμ�0.1mol/LH2SO3��Һ�������ҺpH�����H2SO3��Һ����ı仯��ͼ��ʾ��
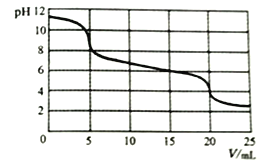
����˵������ȷ����
A. ����H2SO3��Һǰ��Na2CO3��Һ��:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
B. 0<V<5ʱ����Һ�з�ӦΪ:H2SO3+CO32-==HCO3-+HSO3-
C. 15<V<20ʱ����Һ�з�ӦΪ:H2SO3+HCO3-==HSO3-+CO2��+H2O
D. V=15ʱ��������Һ��:(HCO3-)<c(HSO3-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤��������ֵ�������ж���ȷ���ǣ�������
A.2g H2���е���ԭ����ĿΪNA
B.���³�ѹ�£�22.4L O2���еķ�����ĿΪNA
C.1L 1molL��1 KOH��Һ�к��еļ�������ĿΪNA
D.1mol Zn��ΪZn2+ʱʧȥ�ĵ�����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������β�ȡ�ķ�����ȷ���ǣ���ˮ���Ҵ���ֲ���ͺ��Ȼ�����Һ��̼��ƺ��Ȼ��Ƶ���Һ�� ��
A.������������ȡ
B.����Һ������
C.��Һ�����ˡ���������
D.������ȡ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥ�����е�Ca2+��Mg2+��SO42-����ɳ���ɽ���������ˮ��Ȼ������������������������ ���ӹ���NaOH��Һ ������������ ���ӹ���Na2CO3��Һ ���ӹ���BaCl2��Һ������ȷ�IJ���˳����
A.�ݢڢܢ٢�B.�ݢܢڢ٢�C.�ڢݢܢ٢�D.�٢ܢڢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и�����������Ӧ�������¿��ܴ���������ǣ�������
A.pH=2����Һ�У�S2O32����K+��Cl����Na+
B.![]() =10��10 mol/L����Һ�У�Na+��HCO3����Cl����K+
=10��10 mol/L����Һ�У�Na+��HCO3����Cl����K+
C.�� ![]() =1��1012����Һ�У�NH4+��Fe2+��Cl����NO3��
=1��1012����Һ�У�NH4+��Fe2+��Cl����NO3��
D.��ˮ���������c��OH����=1��10��12mol/L����Һ�У�NO3����Mg2+��Na+��SO42��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com