
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
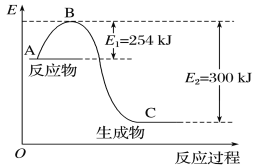
(1)如图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:_______。
(2)若已知下列数据:
化学键 | H—H | N≡N |
键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N—H的键能:___kJ·mol-1。
(3)捕碳技术(主要指捕获CO2在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)=(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)=NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3(aq) ΔH3
请回答下列问题:
ΔH3与ΔH1、ΔH2之间的关系是ΔH3=___。
(4)试比较下列两组△H的大小(填“>”、“<”或“=”)
①H2(g)+![]() O2(g)=H2O(g) △H1 H2(g)+
O2(g)=H2O(g) △H1 H2(g)+![]() O2(g)=H2O(l) △H2
O2(g)=H2O(l) △H2
则△H1____△H2
②S(s)+O2(g)=SO2(g) △H3
Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+10H2O(l)+2NH3(g) △H4
则△H3______△H4
【答案】N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92 kJ·mol-1 390 2ΔH2-ΔH1 > <
2NH3(g) ΔH=-92 kJ·mol-1 390 2ΔH2-ΔH1 > <
【解析】
(1)反应热等于反应物与生成物能量差,且反应物的多少与热量变化相对应,据此书写热化学方程式;
(2)反应热等于反应物总键能与生成物总键能的差,据此计算;
(3)根据盖斯定律,将已知热化学方程式叠加,可得待求反应的热化学方程式;
(4)物质在气态时含有的能量比液态时含有的能量多;放热反应ΔH<0,吸热反应ΔH>0。
(1)由图可知:反应物能量比生成物能量高,反应发生放出热量,每发生反应产生1 mol氨气,放出热量Q=300 kJ-254 kJ=46 kJ,则该反应的热化学方程式可表示为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92 kJ·mol-1;
2NH3(g) ΔH=-92 kJ·mol-1;
(2)N2与H2反应产生NH3,反应的热化学方程式可表示为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92 kJ·mol-1,由于反应热等于反应物总键能与生成物总键能的差,所以943 kJ/mol +3×435 kJ/mol -6×N-H kJ/mol =-92 kJ/mol,解得N-H的键能为:390 kJ/mol;
2NH3(g) ΔH=-92 kJ·mol-1,由于反应热等于反应物总键能与生成物总键能的差,所以943 kJ/mol +3×435 kJ/mol -6×N-H kJ/mol =-92 kJ/mol,解得N-H的键能为:390 kJ/mol;
(3)已知:反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)=(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)=NH4HCO3(aq) ΔH2
根据盖斯定律,将(II)×2-(I),整理可得(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3(aq) ΔH3=2ΔH2-ΔH1;
(4)①由于反应物的能量相同,生成物的状态前者为气态,后者为液态,物质在气态时含有的能量比液态时含有的能量多,所以前者放出能量比后者少,反应放出热量越多,反应热就越小,△H1>△H2;
②S(s)+O2(g)=SO2(g)是放热反应,△H3<0,而反应Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+10H2O(l)+2NH3(g)是吸热反应,△H4>0,故两个反应的反应热:△H3<△H4。


科目:高中化学 来源: 题型:
【题目】将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法不正确的是( )

A.该装置构成了电解池
B.铁腐蚀过程中化学能转化为电能
C.活性炭在该装置中并无实际作用
D.正极电极反应式为O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.用惰性电极电解一定浓度的硫酸铜溶液,一段时间后,加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移电子数为0.4mol
B.磷酸的电离方程式为:H3PO4=H++H2PO4-
C.电镀时保持电流恒定,升温可知加快反应速率
D.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒温密闭容器发生可逆反应Z(?)+W(?)![]() X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是( )
X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是( )
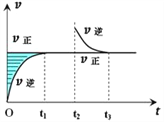
A. Z和W在该条件下一定不为气态
B. t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
C. 若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度相等
D. 若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲乙两容器中发生相同的反应:A(g)+3B(g)![]() 2C(g),甲恒容、乙恒压,温度相同而恒定。起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02mol C,开始时两容器压强相等,最后分别达到平衡。下列有关它们平衡状态的叙述正确的是( )
2C(g),甲恒容、乙恒压,温度相同而恒定。起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02mol C,开始时两容器压强相等,最后分别达到平衡。下列有关它们平衡状态的叙述正确的是( )
A.体积:甲可能小于乙B.C的物质的量:甲一定小于乙
C.压强:甲可能大于乙D.A、C浓度比值![]() :甲一定小于乙
:甲一定小于乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.如图可表示水分解过程中的能量变化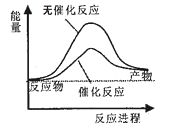
B.若2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol
C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D.已知Ⅰ:反应H2(g)+Cl2(g)=2HCl(g) ΔH=-a kJ/mol,
Ⅱ:键能H-H:b kJ/mol,Cl-Cl:c kJ/mol。则断开1 mol H-Cl键所需能量为![]() kJ
kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.一定条件下,使用催化剂能加快反应速率和提高反应物转化率
B.常温下,向水中滴加少量酸形成稀溶液,溶液中![]() 和水的离子积常数
和水的离子积常数![]() 均不变
均不变
C.在锌与足量稀硫酸反应溶液中加入少量硫酸铜溶液,可以加快反应速率但不影响产生氢气的量
D.在密闭绝热的容器中发生![]() 反应,当反应容器温度恒定时,反应达到平衡
反应,当反应容器温度恒定时,反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同条件下进行化学反应![]() ,B、D起始浓度均为0,反应物A的浓度
,B、D起始浓度均为0,反应物A的浓度![]() 随反应时间的变化情况如下表:下列说法不正确的是( )
随反应时间的变化情况如下表:下列说法不正确的是( )
序号 | 时间 温度 | 0 | 20 | 40 | 50 |
① | 800 |
|
|
|
|
② | 800 | x |
|
|
|
③ | 800 | y |
|
|
|
④ | 820 |
|
|
|
|
A.①中B在![]() min平均反应速率为
min平均反应速率为![]()
![]()
B.②中![]() ,可能使用了催化剂
,可能使用了催化剂
C.③中![]()
![]()
D.比较①④可知,该反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中的SO2是造成酸雨的主要污染物。最新研究表明,离子晶体[N(CH3)4]2SO4(s)能与SO2进行如下可逆反应,使其可能成为绿色的SO2吸收剂:
[N(CH3)4]2SO4(s)+SO2(g)![]() [N(CH3)4]2S2O6(s)
[N(CH3)4]2S2O6(s)
下列说法正确的是
A.[N(CH3)4]+中只含共价键
B.该反应中,SO2作氧化剂
C.SO2漂白品红是利用其强氧化性
D.每吸收标准状况下的SO211.2L,生成15.4g[N(CH3)4]2S2O6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com