
| ||
| ||


科目:高中化学 来源: 题型:
| A、海水 | B、静置后的泥水 |
| C、氢氧化铁胶体 | D、葡萄糖溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | a极板 | b极板 | X电极 | Z溶液 | 装置图 |
| A | 锌 | 石墨 | 负极 | CuSO4溶液 | 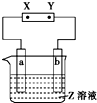 |
| B | 石墨 | 石墨 | 负极 | NaOH溶液 | |
| C | 银 | 铁 | 正极 | AgNO3溶液 | |
| D | 铜 | 石墨 | 负极 | CuCl2溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入少量冰醋酸,溶液的pH减小,CH3COOH的电离度增大 | ||
| B、滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少 | ||
| C、加入少量Na2CO3固体,平衡不移动 | ||
D、加水稀释,可使溶液中
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| K | Na | KCl | NaCl | |
| 熔点/℃ | 63.6 | 97.8 | 770 | 801 |
| 沸点/℃ | 774 | 882.9 | 1500 | 1413 |
| A、低于770℃ |
| B、约850℃? |
| C、高于882.9℃ |
| D、1413~1500℃? |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤⑥ |
| B、①③④⑥⑧ |
| C、①②④⑥⑦ |
| D、③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、烧瓶内气体的颜色不再加深 |
| B、HI的消耗速率与H2的消耗速率之比为2:1 |
| C、I2的生成速率与I2的消耗速率相等 |
| D、烧瓶内气体的质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com