
【题目】据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。 某兴趣小组制备 KH2PO4,流程如下:

已知:
a.KH2PO4 有潮解性,溶于水,不溶于乙醇和醚等有机溶剂。
b.HCl 易溶于乙醇和醚等有机溶剂。
请回答:
(1)步骤Ⅱ的实验操作是_____。
(2)有关步骤Ⅲ,下列说法正确的是_____。
A.有机溶剂 M 可用乙醇
B.步骤Ⅲ与步骤Ⅱ的实验操作基本相同
C.NH4Cl 在水中溶解度明显大于在有机溶剂 M 中
D.有机溶剂 M 可循环使用
(3)试从平衡角度分析,由步骤Ⅰ、Ⅱ得到 KH2PO4 溶液的原理:_____。
(4)在下列仪器中,使用前需进行“检漏”操作的是_____。
A.吸滤瓶 B.球型分液漏斗 C.蒸馏烧瓶 D.碱式滴定管
(5)步骤Ⅳ,包括蒸发浓缩、冷却结晶、过滤、干燥等多步操作。在冷却结晶操作中,为了得到 磷酸二氢钾大晶体,常采取的措施有____________________。某同学发现使用加热浓缩、冷却结晶得到的磷酸二氢钾晶体欠佳,请提出针对性的改进实验方案:_____________,然后经过滤、干燥得到晶体。
【答案】萃取、分液 BCD 步骤Ⅰ.磷酸加入KCl,发生KCl+H3PO4![]() KH2PO4+HCl,步骤Ⅱ.反应产生的HCl易溶于有机萃取剂,经萃取后,水相中HCl浓度降低,平衡正向移动,生成KH2PO4 BD 自然冷却(缓慢冷却) 在磷酸二氢钾溶液中加入乙醇
KH2PO4+HCl,步骤Ⅱ.反应产生的HCl易溶于有机萃取剂,经萃取后,水相中HCl浓度降低,平衡正向移动,生成KH2PO4 BD 自然冷却(缓慢冷却) 在磷酸二氢钾溶液中加入乙醇
【解析】
步骤Ⅰ.磷酸加入KCl,发生KCl+H3PO4![]() KH2PO4+HCl,Ⅱ.反应产生的HCl易溶于有机萃取剂,经萃取后,有机层含有HCl,Ⅲ.用氨水进行反萃取,Ⅴ.可得到氯化铵,Ⅳ.水相经蒸发、浓缩、冷却结晶可得到KH2PO4.
KH2PO4+HCl,Ⅱ.反应产生的HCl易溶于有机萃取剂,经萃取后,有机层含有HCl,Ⅲ.用氨水进行反萃取,Ⅴ.可得到氯化铵,Ⅳ.水相经蒸发、浓缩、冷却结晶可得到KH2PO4.
(1)反应产生的HCl易溶于有机萃取剂,经萃取后,有机层含有HCl,步骤Ⅱ的实验操作是萃取、分液。 故答案为:萃取、分液;
(2)A.乙醇与水互溶,不分层,有机溶剂 M 不可用乙醇,故A错误;
B.步骤Ⅲ与步骤Ⅱ的实验操作基本相同,都是萃取、分液,故B正确;
C.Ⅲ.用氨水进行反萃取,Ⅴ.可得到氯化铵,说明NH4Cl 在水中溶解度明显大于在有机溶剂 M 中 ,故C正确;
D.用氨水进行反萃取,有机溶剂 M 可循环使用,故D正确;
故答案为:BCD;
(3)由步骤Ⅰ、Ⅱ得到 KH2PO4 溶液的原理:步骤Ⅰ.磷酸加入KCl,发生KCl+H3PO4![]() KH2PO4+HCl,步骤Ⅱ.反应产生的HCl易溶于有机萃取剂,经萃取后,水相中HCl浓度降低,平衡正向移动,生成KH2PO4。故答案为:步骤Ⅰ.磷酸加入KCl,发生KCl+H3PO4
KH2PO4+HCl,步骤Ⅱ.反应产生的HCl易溶于有机萃取剂,经萃取后,水相中HCl浓度降低,平衡正向移动,生成KH2PO4。故答案为:步骤Ⅰ.磷酸加入KCl,发生KCl+H3PO4![]() KH2PO4+HCl,步骤Ⅱ.反应产生的HCl易溶于有机萃取剂,经萃取后,水相中HCl浓度降低,平衡正向移动,生成KH2PO4;
KH2PO4+HCl,步骤Ⅱ.反应产生的HCl易溶于有机萃取剂,经萃取后,水相中HCl浓度降低,平衡正向移动,生成KH2PO4;
(4)有活塞的仪器在使用前需进行“检漏”操作,A.吸滤瓶没有活塞,连接好仪器后要检查气密性,故A不选; B.球型分液漏斗有活塞,在使用前需进行“检漏”操作,故B选;C.蒸馏烧瓶没有活塞,连接好仪器后要检查气密性,故C不选;D.碱式滴定管有活塞,在使用前需进行“检漏”操作,故D选;
故答案为:BD;
(5)步骤Ⅳ,包括蒸发浓缩、冷却结晶、过滤、干燥等多步操作。在冷却结晶操作中,为了得到磷酸二氢钾大晶体,常采取的措施有:自然冷却(缓慢冷却)。某同学发现使用加热浓缩、冷却结晶得到的磷酸二氢钾晶体欠佳,请提出针对性的改进实验 方案:在磷酸二氢钾溶液中加入乙醇,然后经过滤、干燥得到晶体。
故答案为:自然冷却(缓慢冷却);在磷酸二氢钾溶液中加入乙醇。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】温度为T时,向2 L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g) ![]() C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量随时间的变化如图所示。下列说法正确的是( )
C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量随时间的变化如图所示。下列说法正确的是( )
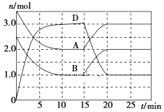
A.反应在前10 min内的平均反应速率v(D)=0.3mol·L-1·min-1
B.若平衡时保持温度不变,压缩容器体积,平衡向逆反应方向移动,平衡常数K值减小
C.反应至15min时,其他条件不变,改变的条件可能是缩小容器体积
D.反应至15min时,其他条件不变,改变的条件可能是降低反应体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下。请回答下列问题。
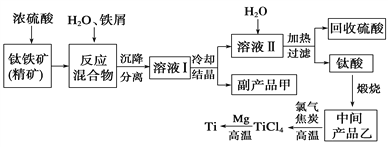
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C═2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为_______________;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为____________________。
(2)上述生产流程中加入铁屑的目的是_________________________,此时溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当溶液的pH等于_______时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为___________________________________________________________。
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为________。Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是_________。除去所得金属钛中少量的金属镁可用的试剂是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式属于水解反应方程式的是( )
A.H2CO3![]() HCO3-+H+B.HCO3-+H2O
HCO3-+H+B.HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
C.HCO3-+OH-=H2O+CO32-D.CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学利用如图装置对电化学原理进行了一系列探究活动。
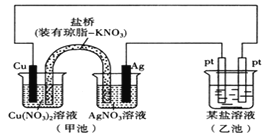
(1)甲池为装置__(填“原电池”或“电解池”)。
(2)甲池反应前,两电极质量相等,一段时间后,两电极质量相差28g,导线中通过__mol电子。
(3)实验过程中,甲池左侧烧杯中NO3-的浓度__(填“变大”、“变小”或“不变”)。
(4)其他条件不变,若用U形铜棒代替“盐桥”,工作一段时间后取出U形铜棒称量,质量___(填“变大”、“变小”或“不变”)。
(5)若乙池中的某盐溶液是足量AgNO3溶液,则乙池中左侧Pt电极反应式为___,工作一段时间后,若要使乙池溶液恢复原来浓度,可向溶液中加入___(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能够正确表示下列变化的离子方程式是
A.醋酸钠的水解:CH3COOH+H2OCH3COO+H3O+
B.电解熔融MgCl2:Mg2++2Cl![]() Mg+Cl2↑
Mg+Cl2↑
C.MnO2 与浓盐酸共热:MnO2+4HCl![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D.K2S溶液中滴加几滴FeCl3溶液:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在 5 L 的恒容密闭容器中发生反应N2(g)+3H2(g)2NH3(g)。反应过程中的部分数据如下表所示:
n/mol t/min | N(N2) | N(H2) | N(NH3) |
0 | a | 24 | 0 |
5 | 13 | 6 | |
10 | 12 | ||
15 | 8 |
下列说法正确的是
A.N2 的初始浓度为16 mol·L1
B.0~5 min 用H2表示的平均反应速率为0.24 mol·L1·min1
C.平衡状态时,c(N2)=2.6 mol·L1
D.N2 的平衡转化率为 25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列变化进行推断:
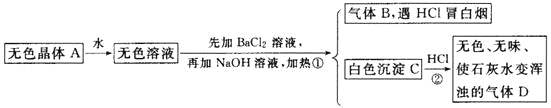
且已知对A加强热产生的气态物质的平均相对分子质量为26.3。
(1)推断A、B、C、D的化学式:A________,B________,C________,D________。
(2)写出①②变化的离子方程式:
①________________________________________________________________;
②________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示。A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素。下列说法错误的是

A. 简单离子的半径大小关系:B>C>E
B. C元素的气态氢化物比D元素的气态氢化物稳定是氢键的缘故
C. 由A、B两种元素组成的离子化合物NH5中,阴、阳离子个数比为1:1
D. 由C、D、E三种元素组成的某种化合物,其水溶液能与盐酸反应产生沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com