
【题目】温度为T时,向2 L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g) ![]() C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量随时间的变化如图所示。下列说法正确的是( )
C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量随时间的变化如图所示。下列说法正确的是( )
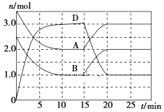
A.反应在前10 min内的平均反应速率v(D)=0.3mol·L-1·min-1
B.若平衡时保持温度不变,压缩容器体积,平衡向逆反应方向移动,平衡常数K值减小
C.反应至15min时,其他条件不变,改变的条件可能是缩小容器体积
D.反应至15min时,其他条件不变,改变的条件可能是降低反应体系温度
【答案】AD
【解析】
由图可知,平衡时A、D的浓度变化量分别为1.5mol/L、3.0mol/L,故1∶x=1.5mol/L∶3mol/L,所以x=2,据此分析解答。
A.由图象可知,10min时反应到达平衡,平衡时D的浓度变化量为3mol/L,故v(D)=![]() =0.3molL-1min-1,故A正确;
=0.3molL-1min-1,故A正确;
B.平衡常数K只与温度有关,温度不变,K不变,故B错误;
C.根据上述分析,x=2,反应后气体的体积不变,增大压强,平衡不移动,但达到新平衡时,浓度均增大,故C错误;
D.由图可知,改变条件瞬间,反应混合物的浓度不变,D的浓度减小,AB的浓度增大,说明平衡向逆反应方向移动,该反应正反应为吸热反应,故改变条件应是降低温度,故D正确;
故选AD。


科目:高中化学 来源: 题型:
【题目】CrCl3·6H2O是中学化学中的常见物质,工业上用铬酸钠(Na2CrO4)来制备。某兴趣小组以实验室中的红矾钠(Na2Cr2O7)为原料来制备CrCl3·6H2O。流程如下:

已知:
a.CrCl3·6H2O不溶于乙醚,易溶于水、乙醇、易水解。
b.CrCl3·6H2O易升华,在高温下能被氧化。
(1)步骤Ⅰ中加入40%NaOH的目的是__________________________。步骤1中甲醇作为还原剂,反应后生成CO2,请写出反应的离子方程式_________________________。
(2)步骤Ⅲ,请补充完整由步骤Ⅱ得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:
ⅰ:将过滤后所得固体溶解于过量的盐酸中,ⅱ: ,ⅲ:过滤,ⅳ:洗涤,ⅴ:干燥,得到CrCl3·6H2O。
①操作ⅱ为_________________________________。
②操作ⅳ最合适的洗涤剂是_____________。
A.乙醇 B.乙醚 C.冷水
③操作ⅴ应选择的干燥方式为_____________。
(3)样品中三氯化铬质量分数的测定
称取样品,加水溶解并定容于容量瓶中。移取一定体积溶液于碘量瓶(一种带塞的锥形瓶)中,加入Na2O2,在一定条件下充分反应后,适当稀释,然后加入过量的稀H2SO4至溶液呈强酸性,此时铬以![]() 存在。充分加热煮沸后,加入KI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用硫代硫酸钠溶液滴定至终点。
存在。充分加热煮沸后,加入KI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用硫代硫酸钠溶液滴定至终点。
①充分加热煮沸的原因是 _______________________。
②在使用硫代硫酸钠溶液滴定过程中使用到碱式滴定管,选出其正确操作并按顺序列出字母:蒸馏水洗涤→加入待量液3~5mL→_____→_____→_____→_____→_____→滴定,进行实验。
a.加液至“0”刻度以上2~3cm
b.倾斜转动滴定管,使液体润湿滴定管内壁,挤压玻璃球,放液
c.调整至“0”或“0”刻度以下,静止1min,读数
d.将滴定管尖端插入锥形瓶内约1cm
e.将滴定管尖端对准锥形瓶,且置于锥形瓶口上方约1cm处
f.右手拿住滴定管使它倾斜30°,左手迅速打开活塞
g.橡皮管向上弯曲,挤压玻璃球,放液
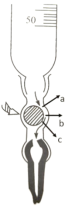
③下图是碱式滴定管的内部构造,滴定时,左手应该捏住乳胶管中玻璃球的______部位(填“a”、“b”或“c”),挤捏乳胶管,使其与玻璃球之间形成一条缝隙,溶液即可流出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼是一种奇特的元素,它来自超新星爆发和宇宙射线的散列辐射。
(1)写出BF3电子式___________,B与F形成共价键时,共用电子对偏向_____原子,判断依据是_________________。
(2)硼酸(H3BO3)在水中电离出阴离子[B(OH)4]-,请写出硼酸的电离方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向10mL0.1molL-1HX溶液中逐滴加入0.2molL-1YOH溶液,混合溶液的pH变化情况如图所示(温度和体积变化忽略不计)。则下列结论错误的是( )
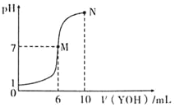
A.HX为一元强酸,YOH为一元弱碱
B.M点水的电离程度大于N点水的电离程度
C.N点对应溶液中粒子浓度:c(YOH)>c(Y+)>c(X-)>c(H+)>c(OH-)
D.25℃时pH=a的YX溶液中水电离出的c(H+)=1.0×10-amolL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池可分为:硅太阳能电池,化合物太阳能电池,如砷化镓(GaAs)、铜铟镓硒(CIGS)、硫化镉(CdS),功能高分子太阳能电池等,Al-Ni常作电极。据此回答问题:
(1)镍(Ni)在周期表中的位置为______;S原子的价电子排布式为________;Ga、As和Se的第一电离能由大到小的顺序是________。
(2)Na3As3中As原子的杂化方式为_____;AsCl3的空间构型为____。
(3)GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN的原因为__________。
(4)写出一种与SO42-互为等电子体的分子_________。
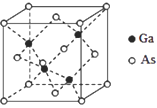
(5)GaAs的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为_____。已知GaAs的密度为ρg/cm3,Ga和As的摩尔质量分别为 MGa g/mol和MAsg/mol,则GaAs晶胞中Ga之间的最短距离为________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酸盐是一种常见的食品添加剂,用如下图实验可检验某食品中亚硫酸盐含量(所加试剂均足量)。下列说法不正确的是

A.亚硫酸盐作为食品添加剂,作用是防腐保鲜
B.反应①过程中通入N2的作用是将装置中空气和生成的气体全部赶出
C.测定样品质量及③中耗碱量,可测定样品中亚硫酸盐含量
D.若仅将②中的氧化剂“H2O2溶液”替换为碘水,对测定结果无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于2—环己基丙烯(![]() )和2—苯基丙烯(
)和2—苯基丙烯(![]() )的说法中正确的是( )
)的说法中正确的是( )
A.二者均可使溴水、高锰酸钾褪色,且褪色原理相同
B.2—苯基丙烯分子中所有碳原子一定共平面
C.二者可与足量的氢气在一定条件下反应得到同一种产物,此产物的一氯代物有5种
D.二者可以通过加成聚合反应形成高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应:aA(g)+bB(g)![]() cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
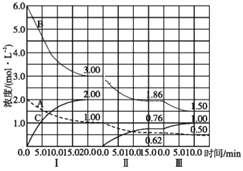
回答下列问题:
(1)反应的化学方程式中,a∶b∶c为___;
(2)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是___;
(3)由第一次平衡到第二次平衡,平衡移动的方向是___,采取的措施是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。 某兴趣小组制备 KH2PO4,流程如下:

已知:
a.KH2PO4 有潮解性,溶于水,不溶于乙醇和醚等有机溶剂。
b.HCl 易溶于乙醇和醚等有机溶剂。
请回答:
(1)步骤Ⅱ的实验操作是_____。
(2)有关步骤Ⅲ,下列说法正确的是_____。
A.有机溶剂 M 可用乙醇
B.步骤Ⅲ与步骤Ⅱ的实验操作基本相同
C.NH4Cl 在水中溶解度明显大于在有机溶剂 M 中
D.有机溶剂 M 可循环使用
(3)试从平衡角度分析,由步骤Ⅰ、Ⅱ得到 KH2PO4 溶液的原理:_____。
(4)在下列仪器中,使用前需进行“检漏”操作的是_____。
A.吸滤瓶 B.球型分液漏斗 C.蒸馏烧瓶 D.碱式滴定管
(5)步骤Ⅳ,包括蒸发浓缩、冷却结晶、过滤、干燥等多步操作。在冷却结晶操作中,为了得到 磷酸二氢钾大晶体,常采取的措施有____________________。某同学发现使用加热浓缩、冷却结晶得到的磷酸二氢钾晶体欠佳,请提出针对性的改进实验方案:_____________,然后经过滤、干燥得到晶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com