
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl﹣、SO42﹣、CO32﹣、AlO2﹣ 中的若干种离子,离子浓度均为0.1 molL﹣1.某同学进行了如下实验:下列说法正确的是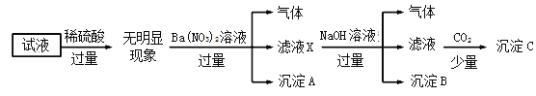
A.无法确定原试液中是否含有SO42﹣
B.滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C.沉淀C为Al(OH)3
D.原试液中一定不含有K+
【答案】D
【解析】
加入过量稀硫酸无明显变化,说明无碳酸根离子;加入硝酸钡有气体,因为前面已经加入了硫酸,硝酸根离子在酸性条件下具有强氧化性,说明有亚铁离子存在且被氧化,沉淀为硫酸钡;因为Fe2+与AlO2﹣不能大量共存,故没有AlO2﹣,加入NaOH有气体,说明存在铵根离子,气体为氨气,沉淀B为红褐色氢氧化铁沉淀;通入少量CO2产生沉淀,先与OH﹣、Ba2+反应,沉淀C为碳酸钡;因为存在的离子浓度均为0.1 molL﹣1,从电荷守恒的角度出发,只能含有NH4+、Fe2+、Cl-、SO42-才能保证电荷守恒,K+必然不能存在;
A. 根据电荷守恒可知必定含有SO42﹣,故A错误;
B. Fe2+已经被氧化成了Fe3+,故B错误;
C.沉淀C为碳酸钡,故C错误;
D. 根据电荷守恒,原试液中一定不含有K+,故D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 植物油的主要成分是高级脂肪酸
B. 异丙苯(![]() )中碳原子可能处于同一平面上
)中碳原子可能处于同一平面上
C. 某些蛋白质可溶于溶剂形成分子胶体,但遇乙醇发生变性
D. 分子式为C4H10O并能与金属钠反应的有机物有5种(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某元素的价类二维图。其中X是一种强碱,G为正盐,通常条件下Z是无色液体,C的相对分子质量比D大16,各物质转化关系如图所示。下列说法正确的是
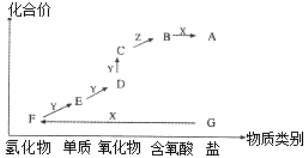
A.A的水溶液显碱性
B.D为一种红棕色气体
C.B 和F能发生复分解反应生成盐
D.F在一定条件下可直接与Y反应生成D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表前四周期A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ms1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有五个未成对电子。
(1)E元素原子的价电子排布式是______,在元素周期表中位置是_____,其最高价氧化物的化学式是__________。
(2)C基态原子的电子排布图为_____,若A为非金属元素,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于_____键(填“σ”或“π”)。
(3)当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是_______。
(4)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,A、B、C、D四种元素的电负性由大到小的顺序是_____(用元素符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同条件下,用O2氧化a mol/L FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测合理的是

A. 由①、②可知, pH越大,+2价铁越易被氧化
B. 由②、③推测,若pH>7,+2价铁更难被氧化
C. 由①、③推测,FeCl2被O2氧化的反应为放热反应
D. 60℃、pH=2.5时, 4 h内Fe2+的平均消耗速率大于 0.15a mol/(L·h)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出一氯甲烷的电子式____,乙烯的结构式____;
(2)乙醇催化氧化的方程式:____;
(3)写出苯和液溴在催化剂作用下生成溴苯的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在体积均为20mL、浓度均为0.1mol·L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加氢氧化钠溶液体积的关系如图所示。
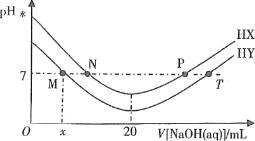
下列推断正确的是
A.HX的电离方程式为HX=H++X-
B.T点时c(Na+)=c(Y-)>c(H+)=c(OH-)
C.常温下用蒸馏水分别稀释N、P点溶液,pH都降低
D.常温下,HY的电离常数![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氯化铜[CuaClb(OH)c·xH2O]是一种重要的无机杀虫剂,它可以通过以下步骤制备。步骤1:将铜粉加入稀盐酸中,并持续通空气反应生成CuCl2。已知Fe3+对该反应有催化作用,其催化原理如下图所示。步骤2:在制得的CuCl2溶液中,加入石灰乳充分反应后即可制备碱式氯化铜。
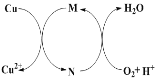
下列有关说法正确的是
A. a、b、c 之间的关系式为:a=b+c
B. 图中M、N分别为Fe2+、Fe3+
C. 步骤1充分反应后,加入少量CuO是为了除去Fe3+
D. 若制备1 mol的CuCl2,理论上消耗11.2 LO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com